贝家智汇 | 石远凯教授:口服PD-L1抑制剂BPI-371153闪耀ESMO Asia,重塑抗肿瘤治疗格局
19小时前 医悦汇 医悦汇 发表于陕西省
本研究旨在评估BPI-371153在晚期实体瘤或复发/难治性(r/r)淋巴瘤患者中的安全性、耐受性、药代动力学特性以及初步疗效。
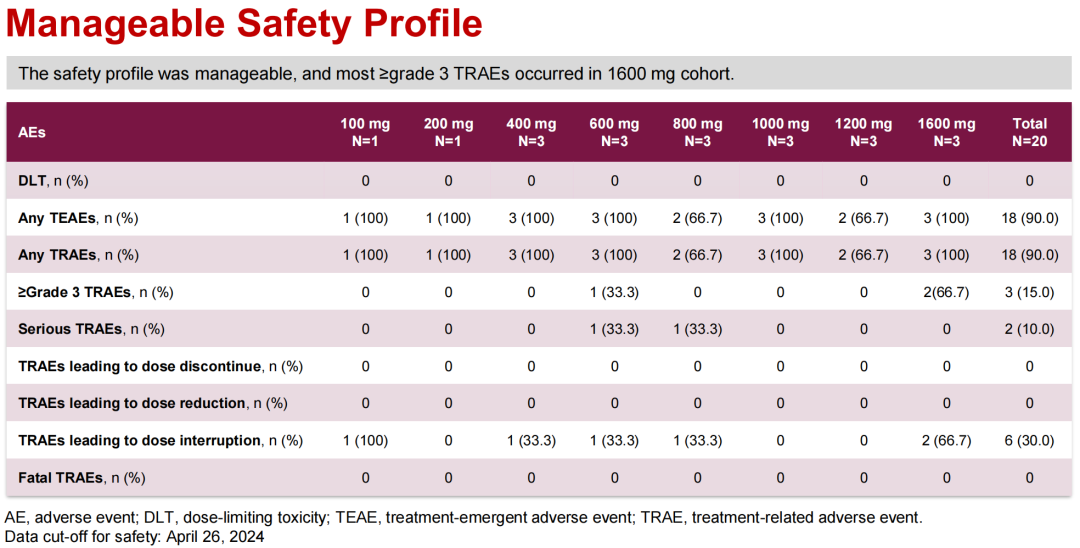
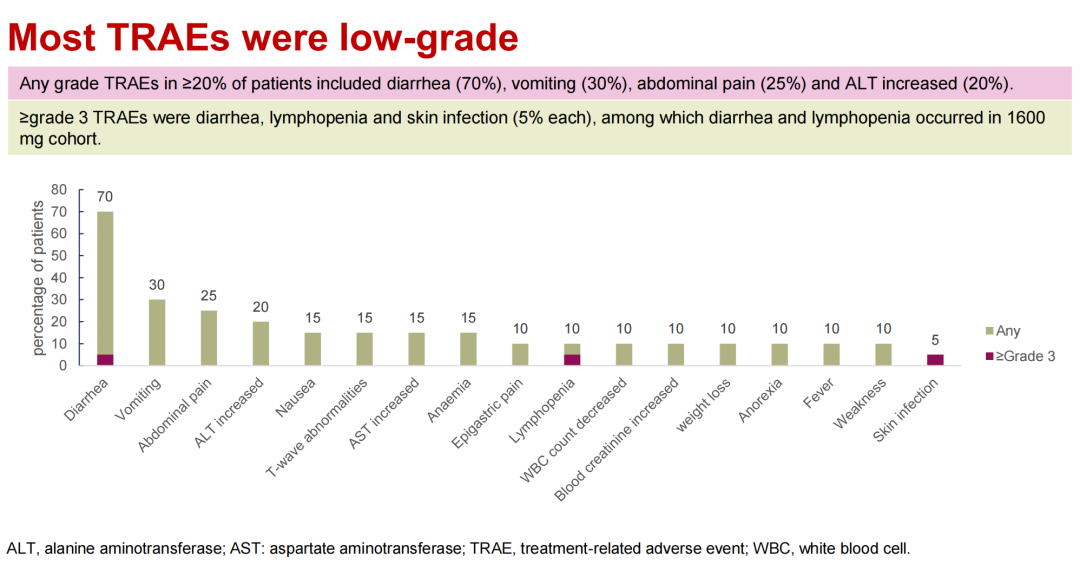
1 新成果 研究全面评估了BPI-371153在安全性、耐受性、药代动力学以及初步疗效方面的表现,更在晚期实体瘤或复发/难治性淋巴瘤中观察到了初步的治疗效果,为后续的深入研究奠定了坚实基础。 2 初步疗效 研究显示,BPI-371153具有良好的药代动力学特性和初步的抗癌活性。 3 安全性 BPI-371153在晚期实体瘤或r/r淋巴瘤患者中表现出良好的耐受性,安全性可管理。 编者按:在2024年欧洲肿瘤内科学会亚洲年会(ESMO Asia)口头报告专场中,中国医学科学院肿瘤医院石远凯教授团队汇报了一种全新的口服小分子PD-L1抑制剂——BPI-371153的I期临床研究结果,首次展示了其人体剂量递增试验的亮眼成果。这项研究不仅全面评估了BPI-371153在安全性、耐受性、药代动力学以及疗效方面的表现,更在晚期实体瘤或复发/难治性淋巴瘤中观察到了令人鼓舞的抗肿瘤治疗效果,为后续的深入研究奠定了坚实基础。 【医悦汇】贝家智汇栏目特别邀请到石远凯教授深入解读这项研究的价值与意义,以供交流! NCT05341557研究发布:新型小分子PD-L1抑制剂BPI-371153在晚期实体瘤或复发/难治性淋巴瘤中的疗效与安全性 研究目的 本研究旨在评估BPI-371153在晚期实体瘤或复发/难治性(r/r)淋巴瘤患者中的安全性、耐受性、药代动力学特性以及初步疗效。 研究方法 NCT05341557研究是一项首次人体、多中心、Ⅰ期临床试验,主要纳入标准包括年龄≥18岁、晚期实体瘤或r/r淋巴瘤、ECOG PS 0-1、标准治疗后疾病进展或不适合/无法耐受标准治疗的患者。研究分为剂量递增和剂量扩展两个阶段,剂量从100 mg QD逐步递增至1600 mg QD。主要终点包括剂量限制性毒性(DLTs)、最大耐受剂量(MTD)和不良事件(AEs),次要终点包括药代动力学(PK)、药效动力学(PD)、客观缓解率(ORR)、疾病控制率(DCR)、缓解持续时间(DOR)、无进展生存期(PFS)和总生存期(OS)。 研究结果 截至2024年4月26日,共有20例患者接受了至少1剂BPI-371153治疗(100-1600mg,每日一次[QD]),包括16例晚期实体瘤(11例NSCLC)和4例复发性/难治性淋巴瘤患者。 有效性方面,在17例疗效可评估受试者中,ORR为23.5%(95% CI:6.8-49.9),DCR为64.7%(95% CI:38.3-85.8)。4例肿瘤缓解的患者中,1例肺腺癌患者达到完全缓解(CR),3例NSCLC或霍奇金淋巴瘤患者达到部分缓解(PR);其中1例为高肿瘤突变负荷(TMB-H),3例为PD-L1高表达。 抗肿瘤活性结果 在安全性方面,BPI-371153展现出了可管理的安全性,未观察到剂量限制性毒性,也未达到最大耐受剂量。无导致剂量降低、永久停药或导致死亡的治疗相关不良事件(TRAEs),大多数TRAEs为1-2级,≥3级TRAEs主要发生在1600 mg剂量组。 安全性结果 药代动力学评估显示,BPI-371153血浆暴露量随剂量增加近似呈线性增长,平均半衰期为20.8-26.2小时,支持每日一次(QD)的给药方案。药效动力学评估表明,BPI-371153能够增加血清中IL-18、IL-2、IL-6、CXCL-9和可溶性PD-L1(sPD-L1)的水平,表明其具有免疫调节作用。 研究结论 BPI-371153在晚期实体瘤或r/r淋巴瘤患者中表现出良好的耐受性,安全性可管理,具有良好的药代动力学特性和初步的抗肿瘤活性。 抗癌新篇!石远凯教授解读 BPI-371153的Ⅰ期临床试验成果 研究PI石远凯教授牵头开展的Ⅰ期研究(NCT05341557)公布了BPI-371153在中国晚期实体瘤或复发/难治性(r/r)淋巴瘤患者中的初步结果,引起了业内的广泛关注。贝家智汇栏目邀请石远凯教授评价BPI-371153的安全性、耐受性、药代动力学特性和初步疗效。 石远凯教授表示,BPI-371153作为一种口服型小分子PD-L1抑制剂,在本次ESMO Asia年会上,首次口头报告了BPI-371153的人体剂量递增试验的结果,以及相关的药代动力学研究数据。本研究旨在全面评估BPI-371153的安全性、耐受性、药代动力学特性以及初步疗效特征。根据目前所取得的临床研究成果,BPI-371153展现出了良好的安全性与耐受性,已观察到令人鼓舞的抗肿瘤活性,并具备优越的药代动力学特性。这些积极的结果为BPI-371153后续的临床研究奠定了坚实的基础。 一个有效的抗癌药物对于治疗癌症至关重要,对于BPI-371153的抗癌活性,石远凯教授认为,在本次报告的I期临床研究中,BPI-371153展现出了令人鼓舞的抗癌活性。在纳入的患者群体中,BPI-371153对复发/难治的经典型霍奇金淋巴瘤、晚期肺癌均表现出有希望的治疗效果,这验证了临床前的理论假设,并为后续的临床研究奠定了坚实的基础。 石远凯教授表示:“PD-1和PD-L1单抗在肿瘤免疫治疗中具有里程碑式的意义。近年来,针对PD-1和PD-L1的大量临床研究已取得了丰硕的成果,但仍有许多问题亟待我们不断探索与解答。因此,BPI-371153的首次人体试验进一步证明,其作为口服剂型的PD-L1小分子抑制剂,在临床上同样表现出有前景的抗肿瘤活性。未来,我们将沿着这一研究方向继续深入探索,以解答更多业界关心的问题。” 前景可期!石远凯教授指明 BPI-371153的未来研究方向 对于BPI-371153未来的临床研究规划,石远凯教授告诉记者:“我们的主要任务是在本药物或免疫治疗已观察到疗效的瘤种中,如肺癌、复发/难治的经典型霍奇金淋巴瘤及软组织肉瘤,开展更深入、更广泛的研究,以进一步验证前期临床研究中观察到的疗效,并探讨如何开展更深入的临床探索。” 石远凯教授表示,接下来的重点开发领域可能主要集中在晚期非小细胞肺癌上,确保能够最大程度地惠及那些最有可能有疗效响应的患者群体。此外,未来还可能探讨BPI-371153联合治疗的疗效与安全性,从而为后续的联合用药策略奠定坚实基础。 据悉,BPI-371153是一种口服的小分子PD-L1抑制剂,可诱导PD-L1的二聚化,随后被肿瘤细胞吞噬,从而降低细胞膜上的PD-L1水平,进而有效破坏PD-1/PD-L1相互作用。相较于传统的单克隆抗体,BPI-371153可能展现出更为卓越的肿瘤组织穿透力。同时,与大分子抗体药物相比,它在生产成本、患者使用便捷性、避免输液相关反应以及免疫相关不良事件的管理灵活性等方面均展现出显著优势。因此,BPI-371153在联合治疗领域凸显出强大的竞争优势,并蕴含着巨大的市场潜力。 参考文献: Yang J, et al. A first-in-human, phase I study of BPI-371153, a novel small-molecule PD-L1 inhibitor, in advanced solid tumors or recurrent/refractory (r/r) lymphoma. ESMO Asia Congress 2024, Abstract 59O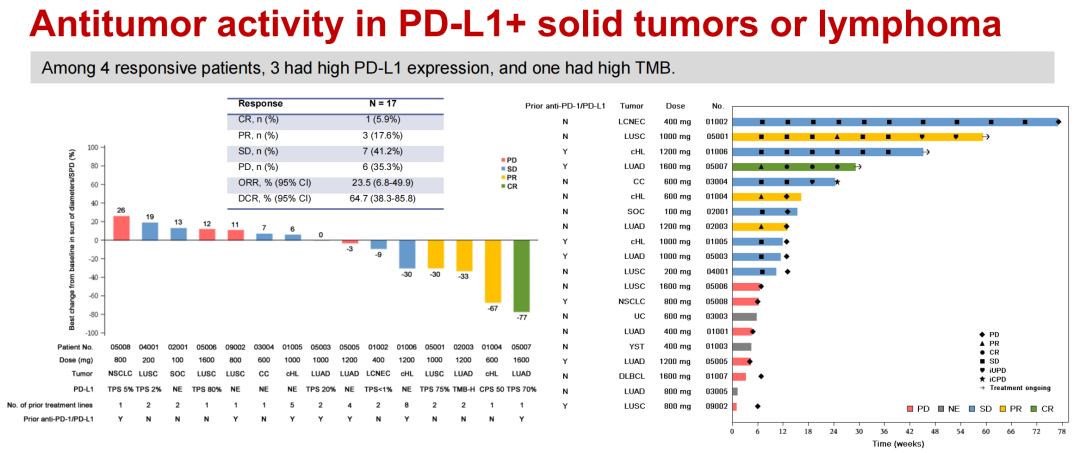
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#PD-L1抑制剂# #复发/难治性淋巴瘤#
3