STTT | SHR-1701联合XELOX和贝伐珠单抗一线治疗不可切除转移性结直肠癌的疗效和安全性
16小时前 daikun MedSci原创 发表于加利福尼亚
该研究旨在评估SHR-1701联合XELOX化疗和贝伐珠单抗作为mCRC患者一线治疗的疗效和安全性,SHR-1701联合XELOX化疗和贝伐珠单抗在不可切除mCRC患者中表现出良好的疗效和可控安全性。
转移性结直肠癌 (mCRC) 是一种高度致命的疾病,预后较差,治疗方法有限,尽管现有的治疗方案,如 FOLFOX、FOLFIRI 和 XELOX 化疗方案,以及与贝伐珠单抗或西妥昔单抗等靶向治疗的联合使用,已经取得了一定的疗效,但 mCRC 患者的中位总生存期仍然只有大约 30 个月。免疫治疗的出现为癌症治疗带来了革命性的变化,也为 mCRC 患者带来了新的希望,免疫检查点抑制剂 (ICI),如帕博利珠单抗和纳武利尤单抗,在具有高微卫星不稳定性 (MSI-H) 或错配修复缺陷 (dMMR) 的肿瘤中表现出显著疗效,然而,这类肿瘤仅占 mCRC 患者的 5% 左右,而大多数 mCRC 患者具有完整的错配修复 (pMMR) 或微卫星稳定 (MSS) 肿瘤,单药 ICI 治疗的效果有限,为了提高 pMMR/MSS mCRC 患者的疗效,近年来研究主要集中在联合治疗策略上,旨在增强 ICI 的疗效。将 ICI 与化疗、靶向治疗或其他免疫调节剂联合使用,可以增加新抗原释放,调节肿瘤微环境,从而增强抗肿瘤免疫反应。SHR-1701 是一种新型的双功能融合蛋白,对 PD-L1 和 TGF-β 具有双重抑制作用,为 MSS/pMMR mCRC 患者提供了一种有潜力的治疗策略,通过同时抑制 PD-L1 介导的免疫检查点信号传导和肿瘤微环境中 TGF-β 配体的隔离,SHR-1701 旨在增强抗肿瘤免疫反应,克服 mCRC 中的免疫抵抗机制。本研究旨在评估 SHR-1701 联合 XELOX 化疗和贝伐珠单抗作为 mCRC 患者一线治疗的疗效和安全性。

方法
这是一项多中心、单臂、II 期临床试验,旨在评估 SHR-1701 联合 XELOX 化疗和贝伐珠单抗作为 mCRC 患者一线治疗的疗效和安全性。该研究共纳入 62 名未经治疗的、组织学确诊的结直肠腺癌患者,且既往未接受过针对转移性疾病的全身治疗。患者年龄在 18-75 岁之间,ECOG 体能状态评分为 0 或 1,至少有一个可测量病灶,预计生存期至少 3 个月,且器官和骨髓功能良好。患者在第 1 天接受 SHR-1701 (30 mg/kg)、贝伐珠单抗 (7.5 mg/kg) 和奥沙利铂 (130 mg/m2) 静脉注射,在第 1-14 天口服卡培他滨 (1 g/m2,每天两次),每个周期为 21 天,最多进行 8 个诱导周期。对于缓解或疾病稳定的患者,进入维持治疗阶段,包括 SHR-1701 (30 mg/kg,第 1 天)、贝伐珠单抗 (7.5 mg/kg,第 1 天) 和卡培他滨 (1 g/m2,每天两次,第 1-14 天)。维持治疗阶段持续至疾病进展、不可耐受的毒性、开始新的抗癌治疗、患者撤回同意或研究者决定,以先发生者为准。主要终点为安全性(治疗相关不良事件)和客观缓解率(ORR),次要终点包括疾病控制率(DCR)、缓解持续时间(DoR)、无进展生存期(PFS)和总生存期(OS)。
研究结果
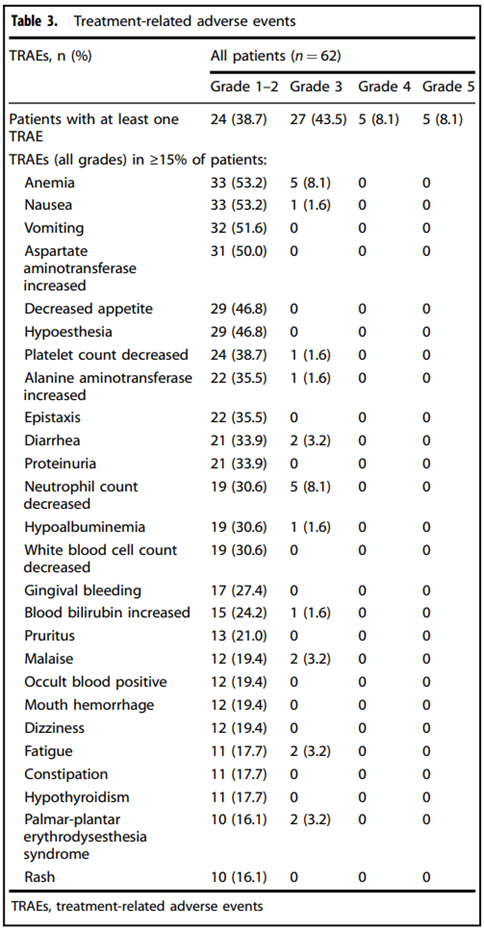
安全性分析:大多数患者 (98.4%) 经历了至少一次治疗相关不良事件 (TRAE),最常见的 TRAE 包括贫血 (61.3%)、恶心 (54.8%)、呕吐 (51.6%) 和天冬氨酸氨基转移酶升高 (50.0%)。59.7% 的患者报告了 3 级或更高级别的 TRAE,最常见的是贫血 (8.1%) 和中性粒细胞计数减少 (8.1%)。21.0% 的患者因 TRAE 而停止治疗。33.9% 的患者经历了免疫相关不良事件 (irAE),9.7% 的患者经历了 3 级或更高级别的 irAE。27.4% 的患者经历了 3 级或更高级别的治疗相关严重不良事件 (SAE),其中 2 例死于肺炎。
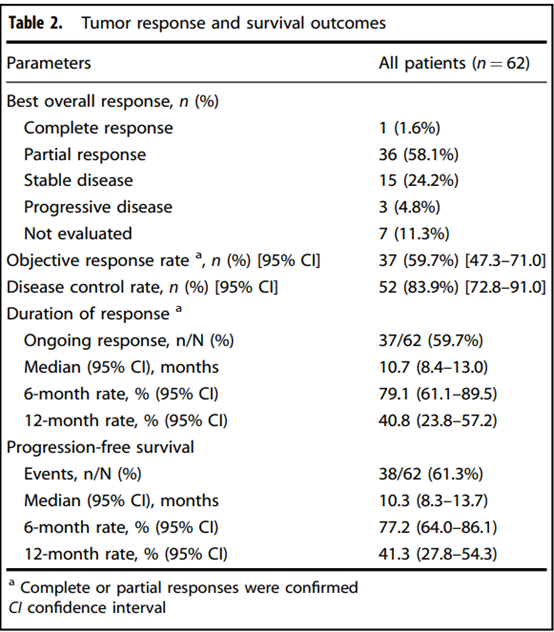
疗效分析:SHR-1701 联合 XELOX 和贝伐珠单抗的 ORR 为 59.7% (37/62),DCR 为 83.9% (52/62),85.5% 的患者在接受基线后扫描时显示靶病灶缩小,缓解持续时间为 10.7 个月,中位 PFS 为 10.3 个月,6 个月和 12 个月 PFS 率分别为 77.2% 和 41.3%,估计 12 个月 OS 率为 67.7%。
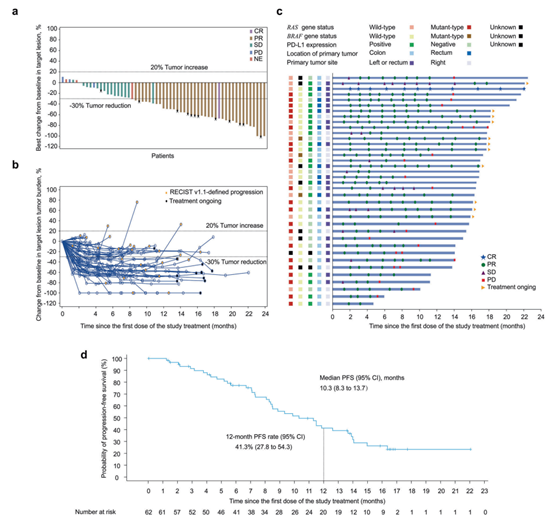
结论
本研究结果显示,SHR-1701 联合 XELOX 化疗和贝伐珠单抗在不可切除的 mCRC 患者中表现出有希望的疗效和可控的安全性。该方案达到了主要终点,ORR 为 59.7%,PFS 为 10.3 个月,OS 估计 12 个月率为 67.7%。本研究结果与其他一线 ICI 联合治疗 mCRC 的研究结果一致,表明 SHR-1701 联合 XELOX 和贝伐珠单抗为 pMMR/MSS mCRC 患者提供了一种有潜力的治疗选择。未来需要进行更大规模、更长时间的随访研究,以进一步验证 SHR-1701 联合 XELOX 和贝伐珠单抗的疗效和安全性,并确定其最佳的治疗人群。
原始出处
Qiu, MZ., Bai, Y., Wang, J. et al. Addition of SHR-1701 to first-line capecitabine and oxaliplatin (XELOX) plus bevacizumab for unresectable metastatic colorectal cancer. Sig Transduct Target Ther 9, 349 (2024). https://doi.org/10.1038/s41392-024-02063-0.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#贝伐珠单抗# #转移性结直肠癌# #XELOX# #SHR-1701#
7