CLIN CANCER RES | 特瑞普利单抗联合贝伐珠单抗作为晚期肝细胞癌一线治疗的II期临床试验
2024-05-06 daikun MedSci原创 发表于上海
该研究旨在评估特瑞普利单抗加贝伐珠单抗一线治疗晚期肝细胞癌的有效性和安全性,特瑞普利单抗加贝伐珠单抗一线治疗晚期肝细胞癌显示出显著的抗肿瘤活性,具有良好的疗效和安全性,支持进一步的临床开发。
晚期肝细胞癌目前仍存在未满足的临床需求,而将程序性死亡配体1抑制剂与抗血管生成药物联合使用能够增强免疫治疗的应答,产生协同治疗效果,前期研究显示,度伐利尤单抗加贝伐珠单抗在不可切除肝细胞癌患者中表现出良好的安全性和有效性,而阿替利珠单抗加贝伐珠单抗与索拉非尼相比,在未经系统治疗的晚期肝细胞癌患者中表现出更长的无进展生存期和总生存期,该研究旨在评估特瑞普利单抗加贝伐珠单抗一线治疗晚期肝细胞癌的有效性和安全性。

方法
该研究是一项前瞻性、单臂、II期临床试验,旨在评估特瑞普利单抗加贝伐珠单抗在未经治疗的晚期肝细胞癌患者中的疗效和安全性,研究在中国6个临床中心进行,入组了54名符合标准的患者,患者接受特瑞普利单抗 240mg加贝伐珠单抗 15mg/kg,每3周一次静脉给药,治疗持续至出现不可接受的毒性或临床获益丧失,主要疗效指标为安全性、耐受性,以及研究者根据RECIST v1.1评估的客观应答率,次要疗效指标包括无进展生存期、疾病控制率、应答时间、应答持续时间、研究者根据RECIST v1.1评估的无进展生存期、独立审查委员会根据mRECIST评估的无进展生存期、独立审查委员会根据mRECIST评估的客观应答率,以及总生存期等。
研究结果
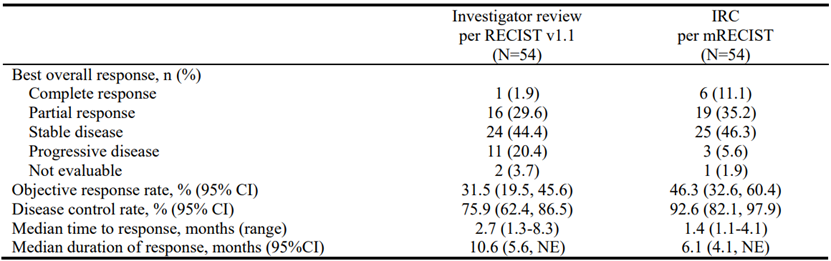
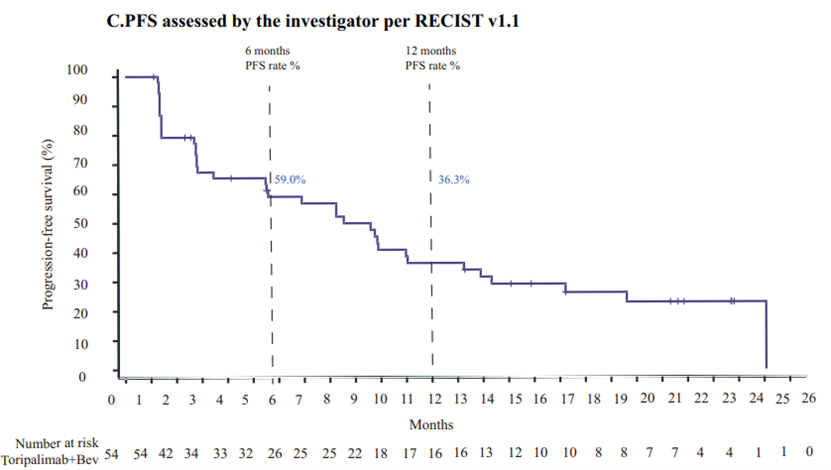
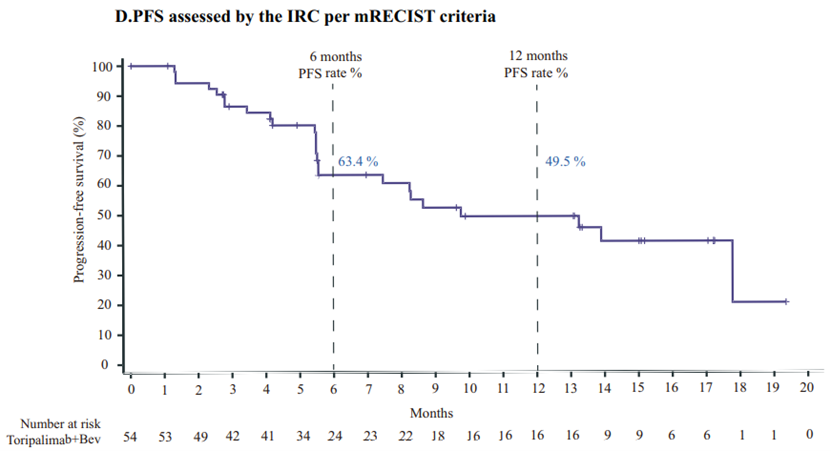
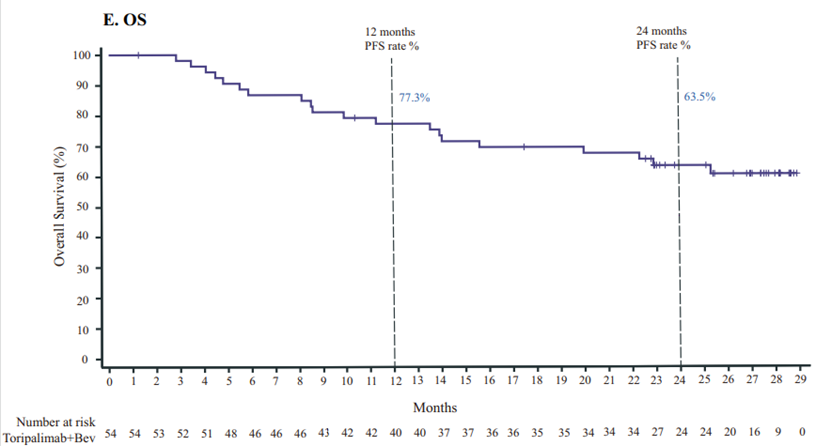
研究者根据RECIST v1.1评估的客观应答率为31.5%(95%CI:19.5-45.6),下限高于预设的10%,独立审查委员会根据mRECIST评估的客观应答率为46.3%(95%CI:32.6-60.4)。研究者评估的中位无进展生存期为8.5个月(95%CI:5.5-11.0),独立审查委员会评估的中位无进展生存期为9.8个月(95%CI:5.6-未评估),总生存期尚未达到,12个月和24个月的总生存率分别为77.3%和63.5%。
安全性
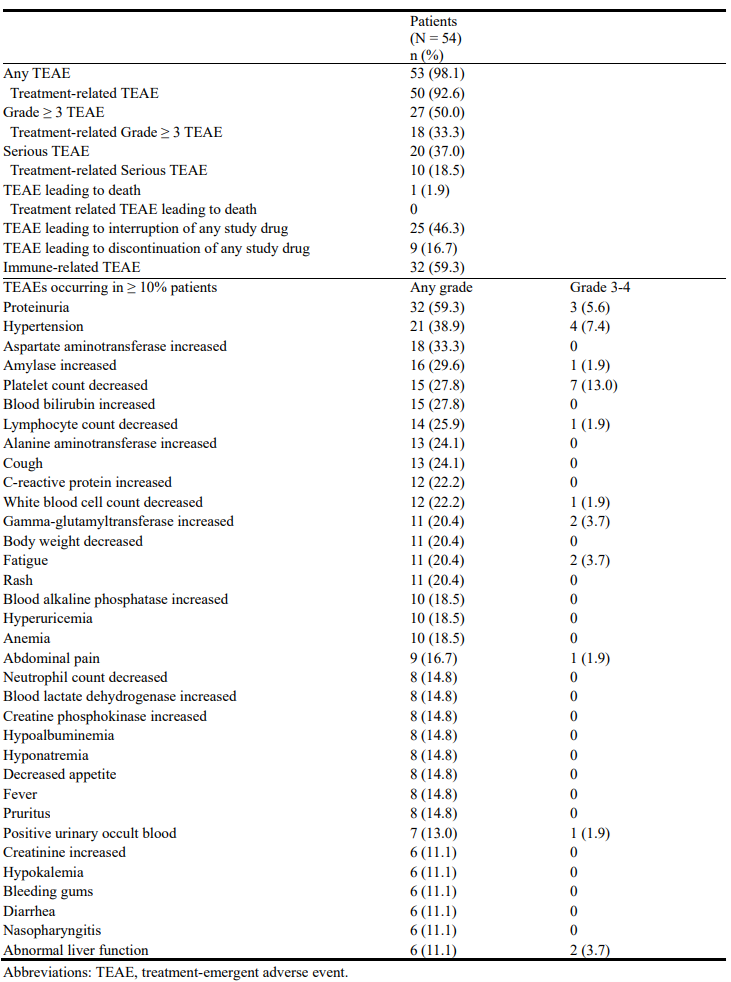
53名(98.1%)患者报告至少一个治疗相关不良事件(TEAE),27名(50.0%)患者报告3级或更高不良事件,18名(33.3%)患者报告与治疗相关的3级或更高不良事件,20名(37.0%)患者报告严重不良事件,10名(18.5%)患者报告与治疗相关的严重不良事件,由于不良事件导致治疗中断的患者有25名(46.3%),由于不良事件导致治疗终止的患者有9名(16.7%),报告了1例不良事件导致死亡,但与研究药物无关,最常见的不良事件包括蛋白尿(59.3%)、高血压(38.9%)、天冬氨酸氨基转移酶升高(33.3%)、淀粉酶升高(29.6%)、血小板减少(27.8%)和胆红素升高(27.8%),32名(59.3%)患者报告免疫相关不良事件(irAE),其中10名(18.5%)为3级或更高。
结论
特瑞普利单抗加贝伐珠单抗一线治疗晚期肝细胞癌显示出显著的抗肿瘤活性,具有良好的疗效和安全性,支持进一步的临床开发,研究结果与其他PD-(L)1抑制剂加贝伐珠单抗联合治疗未经治疗的晚期肝细胞癌患者的结果一致,特瑞普利单抗加贝伐珠单抗的安全性特征与已知各单个药物的已知安全性特征一致,未发现新的安全性信号,但是该研究存在单臂设计和样本量较小等局限性,在积极的结果支持下,特瑞普利单抗加贝伐珠单抗一线治疗晚期肝细胞癌的III期临床试验正在进行中,总体而言,特瑞普利单抗加贝伐珠单抗一线治疗晚期肝细胞癌显示出有利的疗效和安全性,支持进一步的研究。、
原始出处
Yajin Chen, Cheng-You Du, Shunli Shen, Wu Zhang, Yunfeng Shan, Ang Lyu, Jianhui Wu, Changzhen Shang, Xuan Luo, Jinxing Wei, Heng Xiao, Jianguo Qiu, Yunpeng Hua, Shutong Wang, Ting Wang, Shengjie Dai, Shuhao Zhang, Bingying Xie, Yinghao Wu, Chunyi Hao; Toripalimab Plus Bevacizumab as First-line Treatment for Advanced Hepatocellular Carcinoma: A Prospective, Multicenter, Single-Arm, Phase II Trial. Clin Cancer Res 2024; https://doi.org/10.1158/1078-0432.CCR-24-0006.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#贝伐珠单抗# #晚期肝细胞癌# #特瑞普利单抗#
27