PNAS:卢煜明团队最新成果:利用cfDNA片段组学分析组蛋白修饰,为分子诊断工具开发开辟更多可能
2024-10-15 测序中国 测序中国 发表于上海
香港中文大学团队开发 FRAGHA 方法,利用 cfDNA 片段化模式推断组蛋白修饰信号,用于组织起源分析和癌症检测等,为无创分析提供基础。
血浆中细胞游离DNA(cfDNA)的片段化模式已被证明与cfDNA的起源组织密切相关,并与核小体结构有关。已有研究利用血浆染色质免疫沉淀测序(cfChIP-seq)证明了细胞游离核小体(cf-核小体)存在组蛋白修饰(组蛋白H3赖氨酸4三甲基化,H3K4me3)。据报道,分析cf-核小体的组蛋白修饰可以帮助检测转移性结直肠癌(CRC)和肺癌患者;使用基于免疫沉淀的方法靶向组蛋白修饰(例如组蛋白H3赖氨酸27乙酰化,H3K27ac)和DNA甲基化,可以推断诊断标记物和药物靶点的表达水平。然而,免疫沉淀增加了实验的复杂性和分析的周转时间。此外,免疫沉淀过程中可能有DNA丢失。因此,在利用片段组学特征分析cfDNA起源组织以及评估各种组织对血浆的贡献方面,仍有很大的发展空间。

为了探索利用cfDNA分子的片段化模式来推断组蛋白修饰相关信号的可行性,香港中文大学卢煜明教授团队开发了一种方法——FRAGHA(基于片段组学的组蛋白修饰分析),通过识别与选定组蛋白修饰相关的特征片段模式,分析来自不同组织的cfDNA对血浆的相对贡献。研究团队利用FRAGHA分析了不同组织特异性区域的H3K27ac相关组蛋白修饰信号,揭示了这些信号的组织起源。此外,利用组织特异性H3K27ac区域的片段化模式,研究开发了一种机器学习算法来增强肝细胞癌(HCC)检测,曲线下面积(AUC)高达0.97。该研究揭示了cfDNA片段组学与组蛋白修饰之间的关系,为基于cfDNA的无创分析推断与生理或病理过程相关的组蛋白修饰提供了基础,扩大了液体活检的诊断范围。该研究成果已发表在PNAS上,文章题为“Histone modifications of circulating nucleosomes are associated with changes in cell-free DNA fragmentation patterns”。
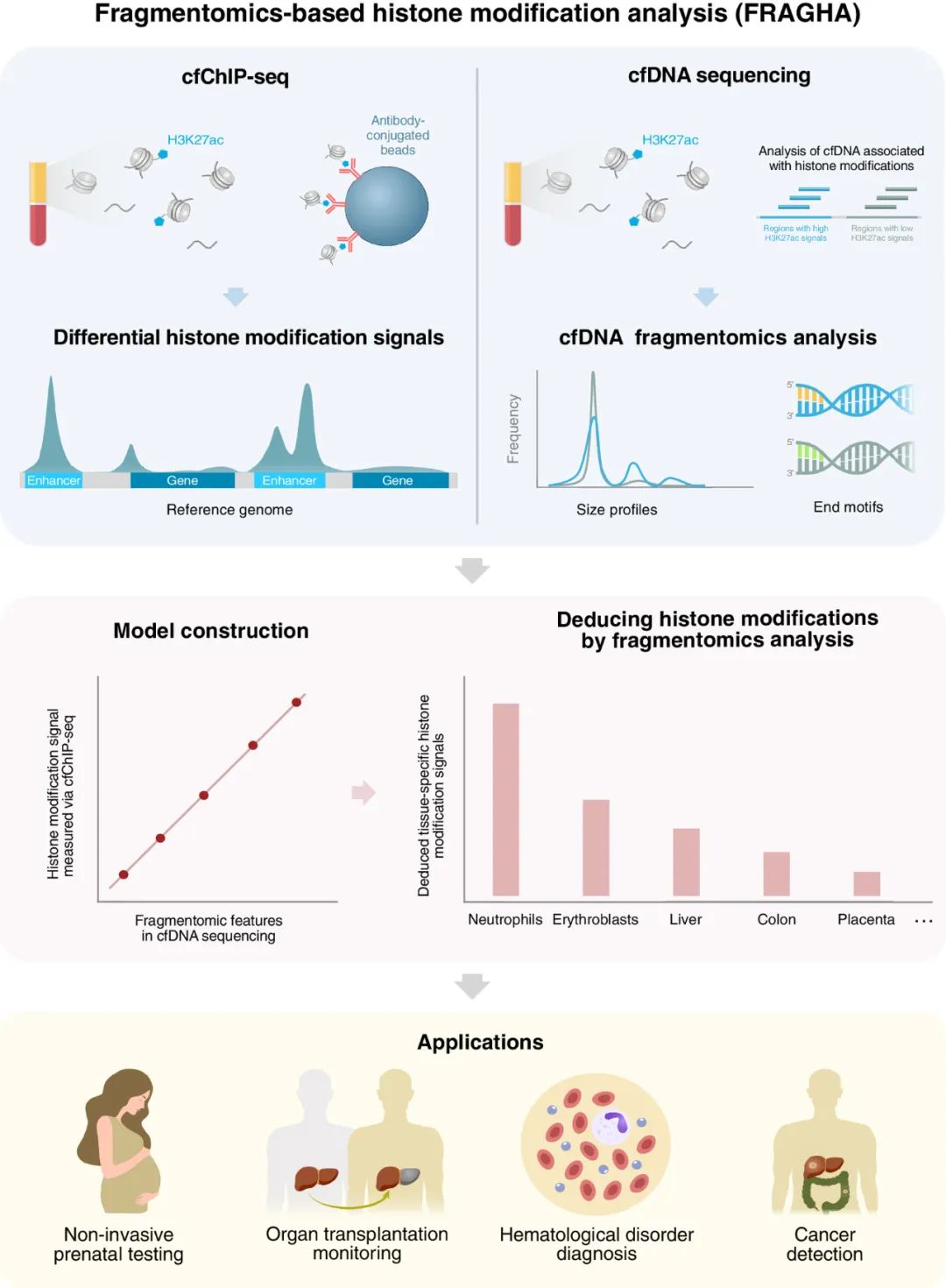
图1.FRAGHA分析示意图。
主要研究内容及结果
1.H3K27ac水平与cfDNA片段大小的关系
为了分析H3K27ac组蛋白修饰水平与cfDNA片段大小之间的关系,研究团队根据cf-核小体的染色质免疫沉淀对H3K27ac信号相关的基因组区域进行了分类,并研究了未进行免疫沉淀样本中cfDNA在这些分类区域的片段大小模式。
通过cfChIP-seq从18个健康对照样本中检测H3K27ac信号,研究团队获得了549个显示不同H3K27ac信号水平的类别。如图2A所示,随着H3K27ac信号水平的增加,在50~150bp大小范围内的分子频率逐渐增加。在230~350bp和420~500bp的范围内也观察到类似的变化模式,但160~225bp和360~400bp范围内的分子频率呈现相反的模式。以上结果强调,片段大小谱可能暗示了H3K27ac信号。
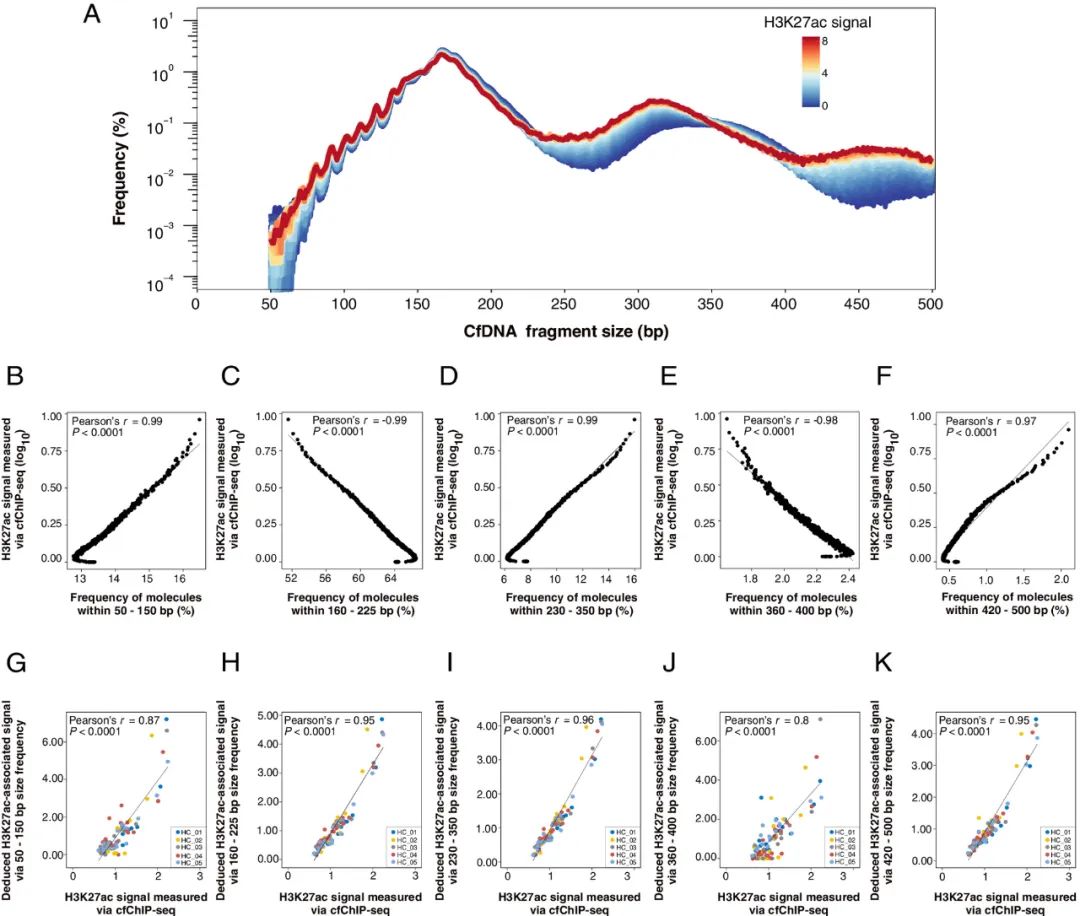
图2.使用配对样本通过cfChIP-seq检测循环核小体的cfDNA片段大小模式和H3K27ac信号之间的相关性。
随后,研究团队构建了一个线性回归模型,可根据cfDNA片段大小模式推断血浆中H3K27ac水平(称为H3K27ac相关信号)。分析发现,当使用160~225bp、230~350bp和420~500bp的血浆DNA频率时,推导出的H3K27ac相关信号与cfChIP-seq测定的H3K27ac相关信号一致(图2H、I和K)。在50~150bp和360~400bp观察到中度相关性(图2G、J)。值得注意的是,使用230~350 bp范围内的血浆DNA分子频率可以提供对实际H3K27ac信号最准确的预测(图2I)。因此,由230~350bp片段频率推断出的H3K27ac相关信号可以作为反映血浆cfDNA中H3K27ac修饰量的代表。
2.推断H3K27ac相关信号用于组织起源分析
研究团队推测,在组织特异性区域推断出的H3K27ac相关信号可能会提供组织对cfDNA的贡献。在妊娠模型中,通过分析ChIP-seq在多种组织和细胞类型(包括B细胞、T细胞、自然杀伤细胞、肝脏、脑、胎盘、心脏、肺等)中检测的H3K27ac信号,发现具有胎盘特异性H3K27ac修饰的基因组区域与基于单核苷酸多态性(SNP)的方法测定的胎儿DNA片段呈强正相关(图3A)。相比之下,与H3K27ac相关的其他17种组织特异性信号没有观察到正相关,从随机选择的基因组区域推断的信号也没有这种相关性。进一步分析肝移植受者样本发现,通过基于SNP方法推断出的肝脏特异性H3K27ac相关信号与供体来源的DNA片段(即肝脏DNA片段)呈正相关(图3B)。但当使用其他类型的组织特异性区域或随机选择的基因组区域时,未发现这种正相关。以上数据支持了利用cfDNA片段模式推断H3K27ac相关信号进行组织起源分析的可行性。此外,研究通过另外的健康受试者血浆中的多种组织特异性H3K27ac相关信号(图4),进一步验证了推断出的H3K27ac相关信号可以告知cfDNA分子的起源组织。
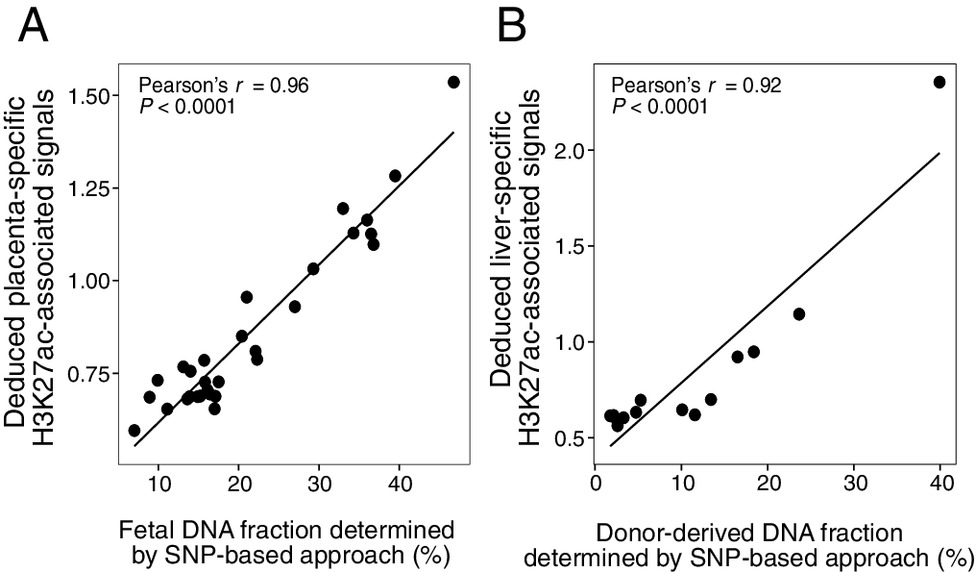
图3.推断的组织特异性H3K27ac相关信号反映了妊娠和肝移植模型的血浆中组织DNA的贡献。
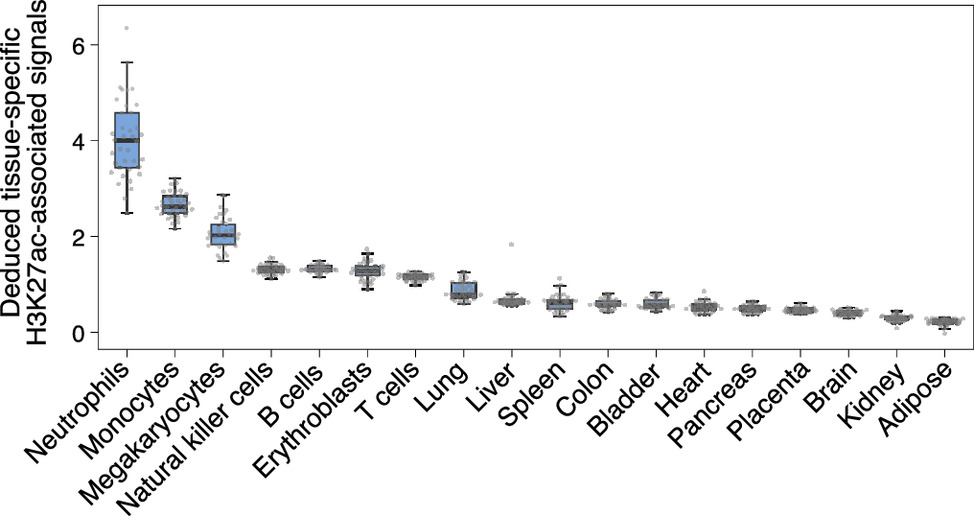
图4.利用来自组织特异性组蛋白修饰区域的片段大小推断出H3K27ac相关信号的分布。测序后的cfDNA分子来自38名健康对照者。H3K27ac相关信号是利用分子的大小频率在230 ~ 350bp范围内推断的。
3.血浆H3K27ac相关信号的临床应用
研究团队分析了推断的H3K27ac相关信号的潜在临床应用。通过对10名β-地中海贫血患者和25名健康受试者的血浆DNA样本进行测序,并将其与之前38名健康对照者的测序结果进行了比较,根据H3K27ac修饰分析了源自红母细胞特异性区域的cfDNA分子。结果显示,与健康受试者相比,推断的与红母细胞特异性区域相关的H3K27ac相关信号在β-地中海贫血患者中显著升高(图5)。因此,推断的H3K27ac在红细胞特异性区域的相关信号可用于反映骨髓中的红细胞生成活性,从而为监测血液病提供了潜在工具。
此外,研究还检测了63名健康受试者、17名慢性乙型肝炎病毒(HBV)感染但未发生肝细胞癌(HCC)的个体(即HBV携带者)和34名不同阶段HCC患者。分析显示,与两名健康受试者和HBV携带者相比,HCC患者中肝脏特异性H3K27ac相关信号显著升高(图4B);在局部结直肠癌(CRC)患者和肝转移CRC患者中,与结肠特异性区域相关的H3K27ac相关信号更高(图5C)。重要的是,与健康受试者相比,推断的肝脏特异性H3K27ac相关信号仅在肝转移CRC患者中升高,没有肝转移的CRC患者未升高(图5D)。以上结果表明,cfDNA片段组学推断出的组织特异性H3K27ac相关信号可以用于检测癌症的存在,以及癌症的起源组织。
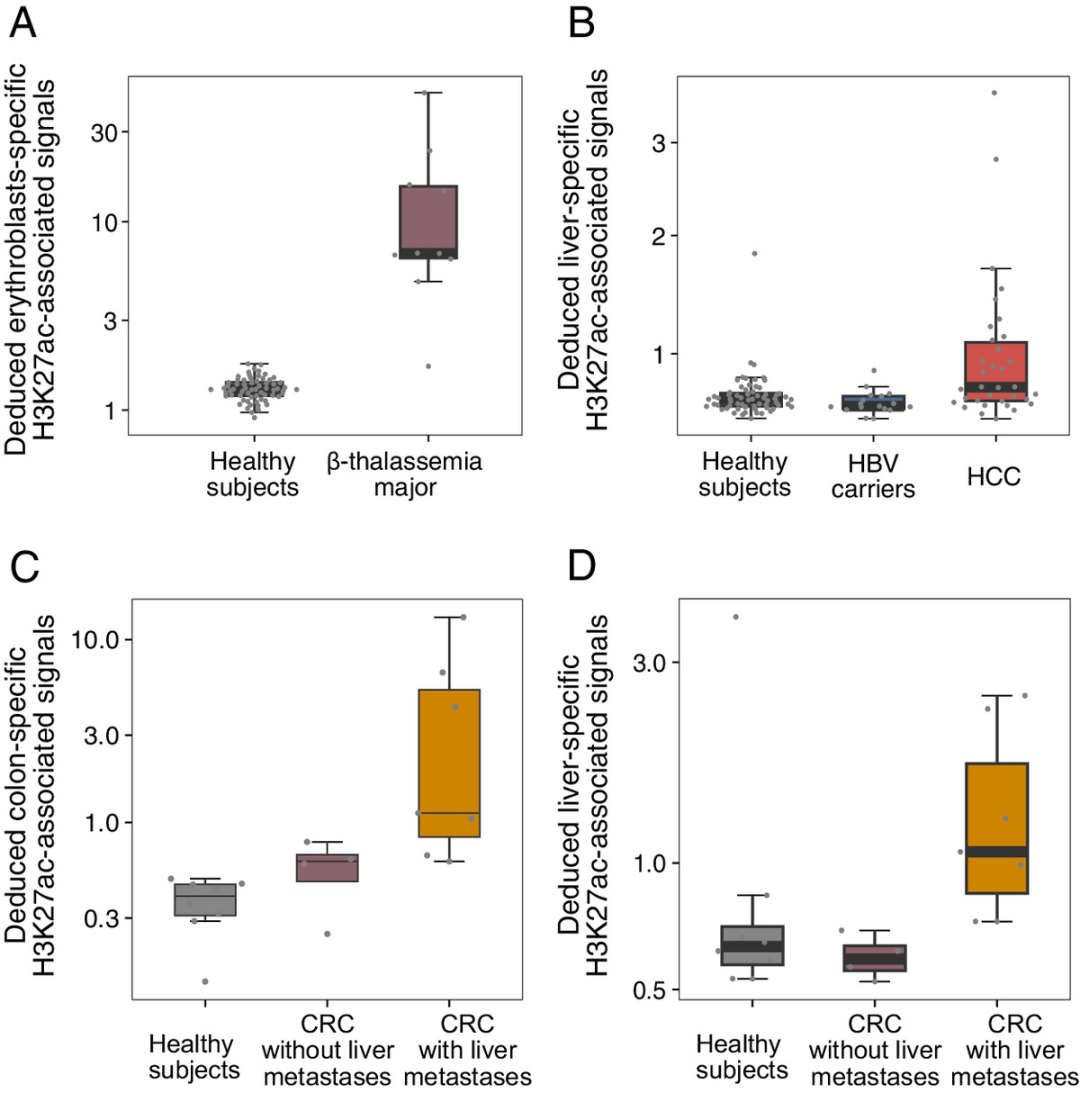
图5.cfDNA片段模式推断H3K27ac相关信号的临床应用。
4.cfDNA末端基序与H3K27ac相关信号
研究团队分析了cfDNA的片段末端基序能否用于推断H3K27ac水平。与基于大小的H3K27ac相关信号推断类似,研究检测了H3K27ac信号最高和最低的基因组区域之间的4-mer片段末端基序频率,共发现了7个信息丰富的4-mer末端基序(即CCGG、CCGC、TCGG、GCGG、CCGA、TCGC、CCCG)。这些信息丰富的末端基序可能提示H3K27ac的存在,以推断H3K27ac相关信号。
如图6A所示,通过末端基序推断出的胎盘特异性H3K27ac相关信号与母体血浆中胎儿DNA组分呈显著正相关。在肝移植模型中,推断出的肝脏特异性H3K27ac相关信号与基于SNP方法确定的供体来源DNA片段具有良好的相关性(图6B)。因此,cfDNA分子的片段末端基序可用于估计组织特异性H3K27ac相关信号。
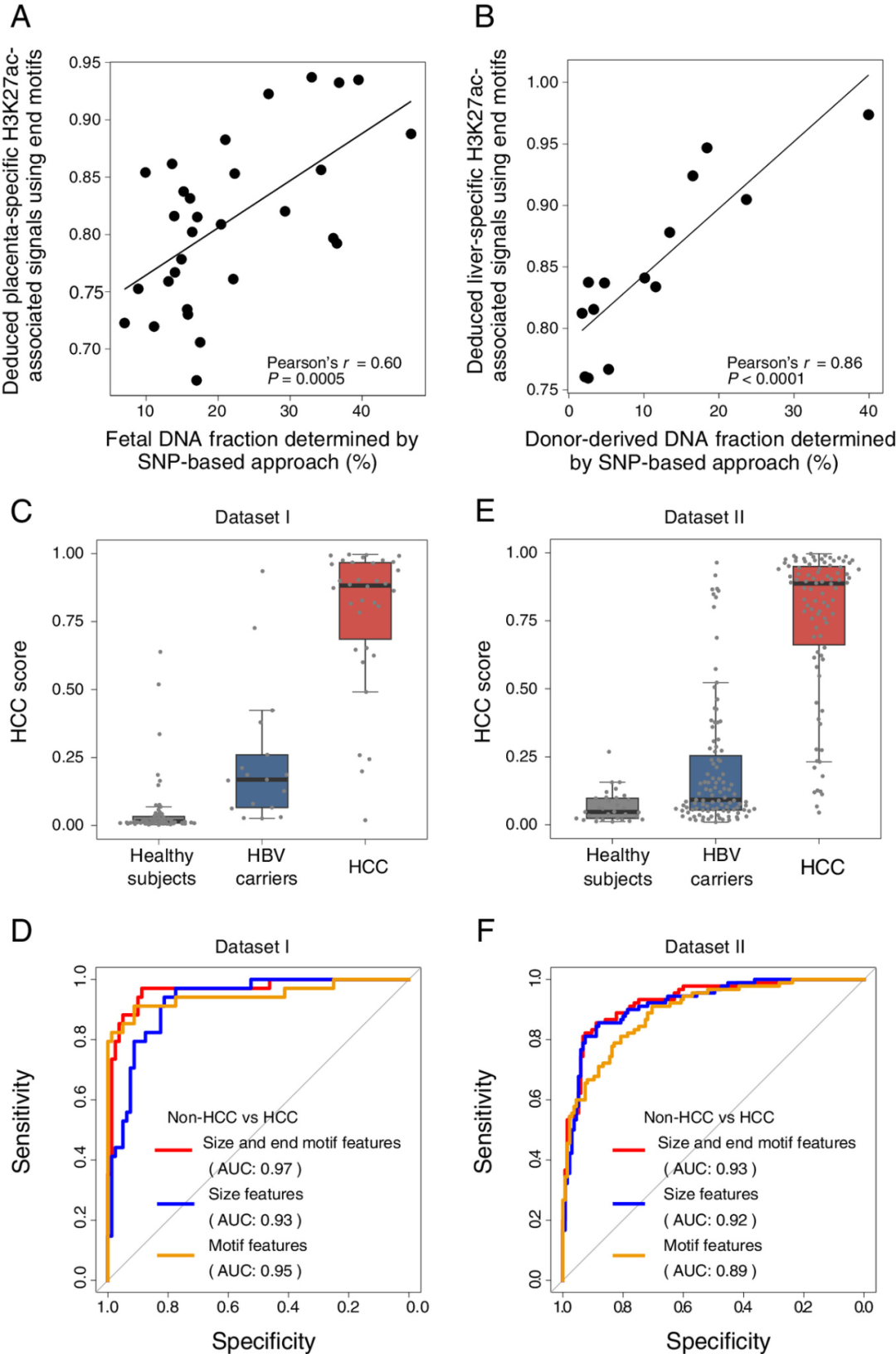
图6.通过cfDNA末端基序分析H3K27ac相关信号。
5.联合分析用于癌症检测
研究团队进一步分析了是否可以利用与组织特异性H3K27ac修饰相关的cfDNA片段大小和末端基序信息来改善癌症检测,并开发了一个支持向量机(SVM)模型来整合230-350bp大小的每个片段以及与组织特异性H3K27ac相关区域相关片段的7个信息丰富的4-mer末端基序。组织特异性H3K27ac相关区域包括肝脏特异性、中性粒细胞特异性、单核细胞特异性和巨核细胞特异性区域,用于区分HCC患者和非HCC患者。
分析显示,根据SVM模型(图6D),使用预测的肝癌发生概率来区分非HCC和HCC病例,AUC为0.97。研究证明了结合cfDNA片段大小和末端基元的模型优于用于检测HCC患者的数据集I和II的单个片段组学特征(图6D和F)。值得注意的是,该联合分析明显优于先前建立的基于片段组学的癌症检测(定向感知血浆cfDNA片段化(OCF)分析)。
此外,研究团队还利用cfChIP-seq分析了H3K4me3的修饰,发现230~350bp范围内分子频率推断出的组织特异性H3K4me3相关信号通常与靶组织DNA对血浆的贡献相关,这在孕妇中得到了证实。与非HCC患者相比,HCC患者血浆中推断出的肝脏特异性H3K4me3相关信号显著升高;与健康对照组相比,有肝转移和无肝转移的CRC患者血浆中推断出的结肠特异性H3K4me3相关信号均升高;与健康对照组相比,β-地中海贫血重症患者血浆中推断的红母细胞特异性H3K4me3相关信号显著升高。因此,疾病状况可能通过与受影响组织相关的组织特异性组蛋白修饰来反映。
结 语
综上所述,该研究证明了利用血浆中cfDNA的片段组学特征来推断血浆中组蛋白修饰水平的可行性。利用源自组织特异性H3K27ac区域的片段组学特征,可以推断出组织特异性H3K27ac相关信号,可用于反映组织对血浆的相对贡献,追溯组织起源。进一步分析证明,血浆中组织特异性H3K27ac相关信号可以作为血液系统疾病和癌症的生物标志物。使用基于与组织特异性H3K27ac相关区域相关的片段组学特征的机器学习模型(例如SVM)可以增强癌症检测。因此,通过血浆中cfDNA片段组学分析组蛋白修饰相关信号显示了无创性产前检测、器官移植监测、血液病诊断和癌症检测的潜力,为开发分子诊断工具开辟了不同的可能性,
论文原文:
https://www.pnas.org/doi/10.1073/pnas.2404058121
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#cfDNA# #癌症检测# #组蛋白修饰# #FRAGHA#
56