指南推荐|美国肝病学会/美国感染病学会丙型肝炎指导意见:HCV感染的检测、管理和治疗(2023年更新)
2023-12-28 临床肝胆病杂志 临床肝胆病杂志 发表于上海
对于HCV的检测,指南小组建议首先筛查HCV抗体,然后触发HCV RNA的检测,以确定是否存在活动性感染,还是出现病毒自发性或治疗后清除。
美国感染病学会(IDSA)和美国肝病学会(AASLD)于2013年联合启动了HCV感染指导意见的制定工作,为临床医生提供循证、公正、及时的HCV感染的诊断、治疗和管理指导。世界卫生组织(WHO)认识到病毒性肝炎构成与人类免疫缺陷病毒(HIV)、疟疾和结核病一样的公共卫生威胁,于2016年6月发布了首份全球卫生部门战略,并确定了到2030年消除病毒性肝炎这一重要公共卫生危害的目标。消除丙型肝炎公共卫生危害的具体目标包括:HCV感染的发病率和流行率降低90%,对80%的符合条件的慢性感染者进行治疗,将HCV相关死亡减少65%,以及普遍获得关键的预防和治疗服务。为响应WHO的行动呼吁,美国国家科学院、工程院和医学院制定了一项消除病毒性肝炎的美国战略计划。美国疾病控制和预防中心、美国卫生与公众服务部随后制定了与WHO制定的目标相称的国家实施战略和目标。自2013年以来,HCV指导意见持续在更新。与2020年发布的指导意见相比,2023年更新的主要内容包括:继续强调HCV的普遍筛查;针对治疗依从性不佳的管理提出新的建议;更新了采用最低限度监测的简化治疗的建议,并扩大了适应人群;实体器官移植受者的管理和治疗建议;扩大了针对儿童和青少年的治疗和再治疗建议;以及针对特殊和重点人群的筛查、管理和治疗建议。2023年版HCV指导意见具体的更新要点如下:(1)进行HCV的普遍筛查;(2)包括HIV合并感染人群在内的简化治疗策略;(3)直接抗病毒药物(DAA)漏服少于7天的依从性不佳患者的管理建议;(4)监狱内的HCV感染者应积极抗病毒治疗;(5)实体器官移植者使用DAA抗HCV治疗是安全有效的。
1HCV普遍筛查的检测、评估和监测
1.1 HCV普遍筛查的实施
HCV指导意见2019年首次建议对所有≥18岁成人进行HCV普遍筛查,同时美国预防服务工作组和疾病防治中心也提出了一致的建议草案。美国预防服务工作组随后于2020年3月建议对18~79岁成人进行HCV普遍筛查。2020年4月,美国疾病防治中心建议对所有≥18岁的成人和每次妊娠期间的所有孕妇至少进行一次HCV筛查,HCV感染率小于0.1%的地区除外。
进行HCV普遍筛查的理由包括成本效益;提高了HCV病例的发现率;HCV感染的流行病学发生了变化,新发感染主要发生在年轻人中;以及安全、经济有效的DAA的可及性。普遍筛查是任何丙型肝炎消除策略的关键和必要组成部分,是进入丙型肝炎抗病毒治疗的切入点。对于HCV的检测,指南小组建议首先筛查HCV抗体,然后触发HCV RNA的检测,以确定是否存在活动性感染,还是出现病毒自发性或治疗后清除。
1.2 DAA治疗依从性不佳的处理
对接受格卡瑞韦/哌仑他韦,或索磷布韦/维帕他韦治疗的无肝硬化或代偿期肝硬化的初治患者,DAA治疗中断的管理建议。
1.2.1 DAA治疗少于28天的处理
(1)漏服时间≤7天:立即重新开始DAA治疗,完成初始计划的治疗疗程(8或12周)。
(2)漏服时间≥8天:①立即重新开始DAA治疗,重启DAA治疗优先于检测HCV RNA水平。②尽快进行HCV RNA检测,最好是重启DAA治疗的同时进行。
如果HCV RNA阴性(未检测到),完成初始计划的治疗疗程,8或12周,用完总的计划剂量,即延长治疗的持续时间,使患者获得计划的总剂量,例如如果患者错过了计划的8周疗程的10天,治疗将延长到8周加10天。基因3型和/或代偿期肝硬化的患者,建议额外增加4周的疗程。
如果HCV RNA阳性(>25 IU/mL),或者未进行HCV RNA的检测,额外增加4周的疗程。
1.2.2 DAA治疗超过28天的处理
(1)漏服时间≤7天:立即重新开始DAA治疗,完成初始计划的治疗疗程(8或12周)。
(2)漏服时间连续8~20天:①立即重新开始DAA治疗,重启DAA治疗优先于检测HCV RNA水平。②尽快进行HCV RNA检测,最好是重启DAA治疗的同时进行。
如果HCV RNA阴性(未检测到),完成初始计划的治疗疗程(8或12周,总的计划剂量)。基因3型和/或代偿期肝硬化的患者,建议额外增加4周的疗程。
如果HCV RNA阳性(>25 IU/mL),或者未进行HCV RNA的检测,立即停止治疗,按照经治患者的方案再次开始新的治疗。
(3)漏服时间连续超过21天:立即停止治疗,评估是否获得12周持续病毒学应答(SVR12)。如果没有获得SVR12,按照经治患者的方案再次开始新的治疗。
2初治患者的治疗
2.1 适用于HCV简化治疗的患者
以下情况的慢性HCV感染的成年人,包括HIV感染者:(1)感染任何基因型。(2)既往未接受过抗病毒治疗。(3)无肝硬化或有代偿期肝硬化(Child-Pugh A):①FibroScan显示肝硬度>12.5 kPa;②FIB-4>3.25;③无创血清学检测(包括HCV FibroSure或增强型肝纤维化检测);④肝活检;⑤肝结节或脾肿大的影像学表现;⑥血小板计数<150 000/mm3。
2.2 不适用于HCV简化治疗的患者
以下情况的慢性HCV感染的成年人:(1)既往接受过抗病毒治疗;(2)HBsAg阳性;(3)代偿期肝硬化(Child-Pugh A)伴终末期肾病[估计肾小球滤过率(eGFR)<30 mL·min-1·m-2];(4)当前或既往失代偿期肝硬化:Child-Pugh评分≥7[基于腹水、肝性脑病、TBil>2.0 mg/dL、Alb≤3.5 g/dL或国际标准化比值(INR)≥1.7的Child-Pugh评分];(5)当前妊娠;(6)已知或疑似肝细胞癌;(7)既往肝移植。
2.3 无肝硬化患者简化治疗的评估及监测
简化治疗方案推荐的DAA方案包括:8周的格卡瑞韦(300 mg)/派仑他韦(120 mg)与食物一起服用,或12周的索磷布韦(400 mg)/维帕他韦(100 mg)。
2.3.1 抗病毒治疗前的评估
(1)计算FIB-4,评估肝硬化程度。FIB-4是肝纤维化的无创评估方法,其计算公式为:[年龄(年)×AST(U/L)]÷[PLT(109/L)×ALT(U/L)的平方根]。如果患者的FIB-4评分>3.25,或者之前进行的测试中有以下任何一项,则认为患有肝硬化:瞬时弹性成像显示肝硬化(即肝硬度>12.5 kPa),非侵入性血清学测试高于专有阈值显示肝硬化(如FibroSure,增强型肝纤维化测试),肝硬化的临床证据(如肝脏结节和/或脾肿大,血小板计数<15万/mm3),或既往肝活检显示肝硬化。(2)检测全血细胞计数。(3)检测肝功能:TBil、DBil、Alb、ALT、AST。(4)评估eGFR。(5)记录合并用药(当前处方药、非处方药和草药/膳食补充剂),评估药物-药物相互作用(DDI),使用HCV指南网站监测部分的表格或利物浦大学药物相互作用检查器进行评估。(6)HCV RNA定量检测。(7)HIV抗体检测。(8)HBsAg检测。(9)血清妊娠检测,并且提供妊娠期间使用DAA风险的咨询。(10)进行DAA使用注意事项和依从性教育,以及预防再次感染,避免过量饮酒的教育。
2.3.2 治疗期间的监测
(1)监测糖尿病治疗患者的低血糖;(2)监测使用华法林抗凝治疗患者的INR;(3)其他患者不需要进行实验室指标的监测;(4)如需要,可进行面诊、远程医疗或电话访问提供治疗支持及症状评估。
2.3.3 治疗结束后治愈(SVR)的评估
(1)停止治疗12周以后,进行HCV RNA定量及肝功能检测,确认是否获得病毒的清除(HCV RNA检测不到)以及肝功能是否复常;(2)获得SVR以后,ALT和/或AST仍升高患者,需要评估是否存在其他肝病病因。
2.3.4 治疗后的随访
(1)无论是否获得治愈,建议不过量饮酒。(2)如果获得治愈:①非肝硬化患者不建议随访;②如果有再次感染的风险,进行预防再次感染的健康教育,每年定期监测HCV RNA,或者出现ALT/AST升高时进行HCV RNA检测。(3)如果没有获得治愈:①转诊到专科进行HCV的再次治疗;②再次治疗前,每6~12个月评估一次病情进展,检测肝功能、全血细胞计数和INR。
2.4 代偿期肝硬化患者简化治疗的评估及监测
简化治疗方案推荐的DAA方案包括:基因1~6型,8周格列卡韦(300 mg)/派仑他韦(120 mg)与食物一起服用,或基因1、2、4、5或6型,12周索磷布韦(400 mg)/维帕他韦(100 mg)。
2.4.1 抗病毒治疗前评估
(1)计算Child-Pugh评分,Child-Pugh评分基于腹水、肝性脑病、TBil>2.0 mg/dL、Alb≤3.5 g/dL或INR≥1.7。Child-Pugh评分≥7(即Child-Pugh B或C)的患者患有失代偿性肝硬化;这种简化的治疗方法不推荐用于失代偿期肝硬化患者。(2)肝脏超声,在开始抗病毒治疗前6个月内进行肝脏超声检查,以排除肝细胞癌和亚临床腹水。这种简化的抗病毒治疗方法不建议用于肝细胞癌和/或失代偿期肝硬化患者。(3)检测全血细胞计数。(4)检测INR。(5)检测肝功能(TBil、DBil、Alb、ALT、AST)。(6)评估eGFR。(7)记录合并用药评估DDI。(8)HCV RNA定量检测。(9)HIV抗体检测。(10)HBsAg检测。(11)HCV基因型检测(如果使用索磷布韦/维帕他韦治疗)。(12)血清妊娠检测,并且提供妊娠期间使用DAA风险的咨询。(13)进行DAA使用注意事项及依从性,预防再次感染,避免过量饮酒的教育。
2.4.2 治疗期间的监测
(1)治疗期间监测肝损伤,肝硬化患者使用DAA很少发生肝功能失代偿。如果发展为黄疸、腹水、自发性细菌性腹膜炎、静脉曲张出血或肝性脑病可能提示肝脏失代偿。如果患者出现肝功能指标恶化(如TBil、AST、ALT、INR)、黄疸、腹水、肝性脑病或新的肝脏相关症状,应转诊至肝病专科治疗。(2)监测糖尿病治疗患者的低血糖。(3)监测使用华法林抗凝治疗患者的INR。(4)如需要,可进行面诊、远程医疗或电话访问以提供治疗支持及症状评估。
2.4.3 治疗结束后治愈(即SVR)的评估
(1)停止治疗12周以后,进行HCV RNA定量及肝功能检测,确认是否获得病毒的清除(HCV RNA检测不到)以及肝功能是否复常。(2)获得SVR以后,ALT和/或AST仍升高患者的其他肝病病因。
2.4.4 治疗后的随访
(1)无论是否获得治愈,每6个月行肝脏超声和AFP检测,筛查HCC;建议严格不饮酒;遵循AASLD的指南评估静脉曲张。(2)如果获得治愈,如果有再次感染的风险,进行预防再次感染的健康教育,每年定期监测HCV RNA,或者出现ALT/AST升高时进行HCV RNA检测。(3)如果没有获得治愈,转诊到专科进行HCV的再次治疗,再次治疗前,每6~12个月评估一次病情的进展,检测肝功能、全血细胞计数和INR。
2.5 成人初治丙型肝炎患者治疗方案(表1)
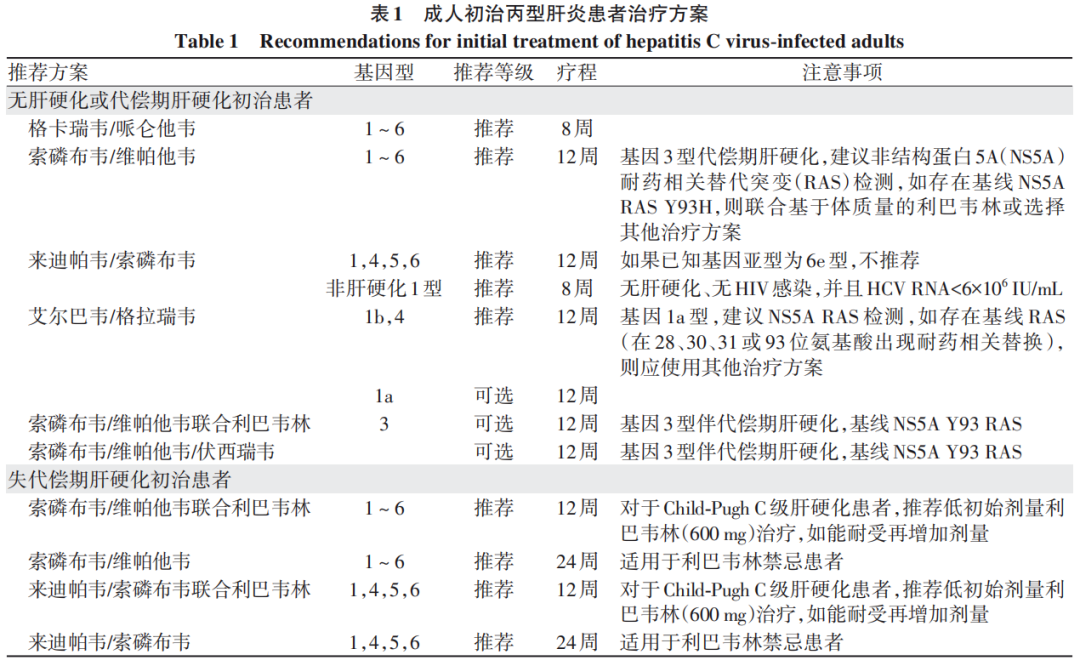
3经治患者的治疗
成人经治丙型肝炎患者治疗方案见表2。
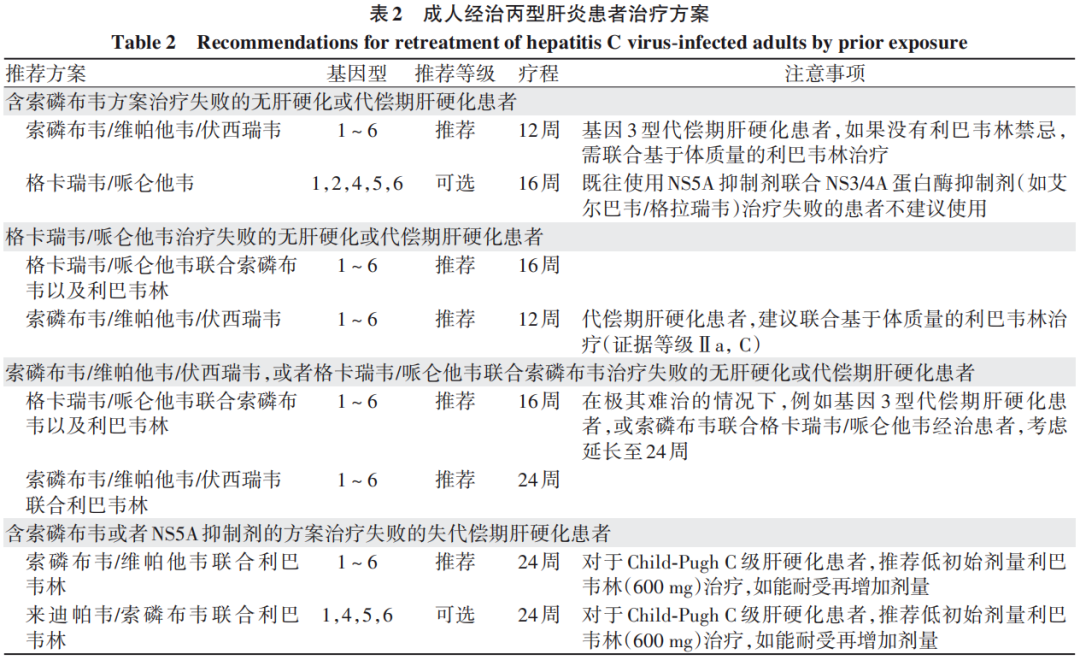
4特殊患者的治疗
4.1 儿童初治患者的治疗方案(表3)

4.2 儿童经治患者的治疗方案(表4)
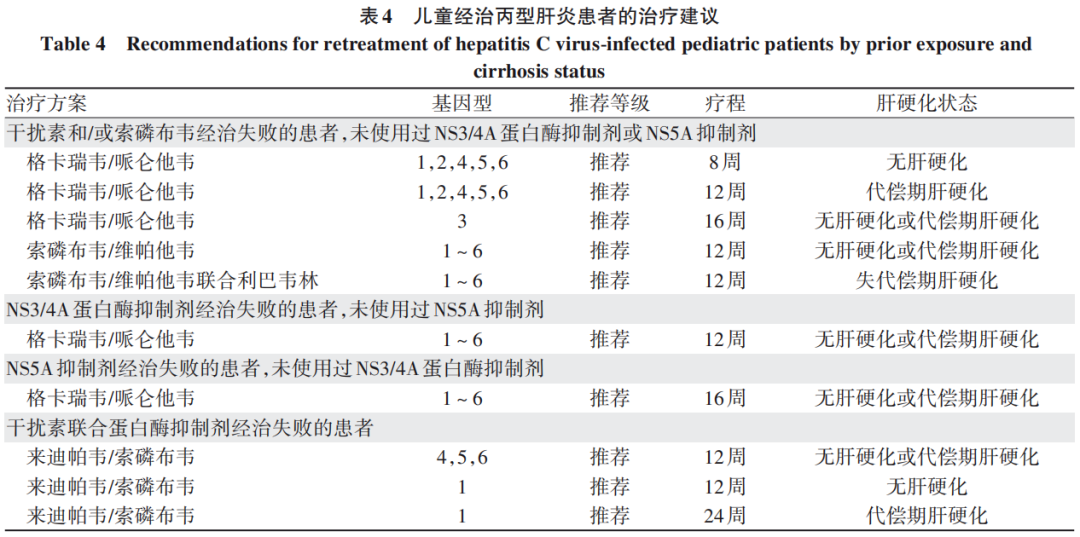
4.3 丙型肝炎移植后的治疗方案(表5)
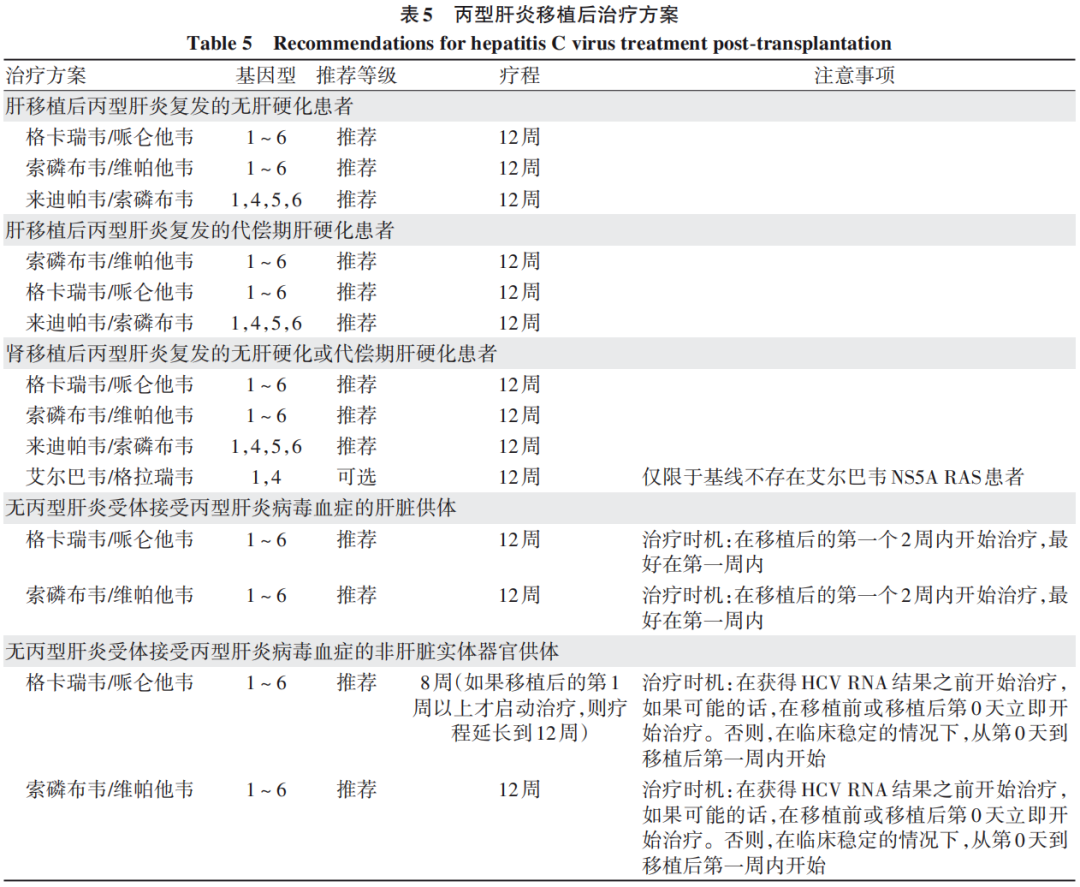
4.4 急性丙型肝炎
确诊的急性HCV感染者(HCV RNA阳性)应与慢性HCV感染者接受相同的治疗,而不必等待可能的自发清除。对于急性HCV感染,不建议采用缩短疗程的DAA治疗。
全文下载 PDF & HTML
http://www.lcgdbzz.org/cn/article/doi/10.3969/j.issn.1001-5256.2023.12.008
引证本文 Citation
饶慧瑛 .《美国肝病学会/美国感染病学会丙型肝炎指导意见:HCV感染的检测、管理和治疗(2023年更新)》意见要点[J].临床肝胆病杂志, 2023, 39(12): 2798-2803

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#丙型肝炎# #HCV#
28