【Blood Adv】纳基奥仑赛治疗成人R/R B-ALL的中国多中心2期研究结果
昨天 聊聊血液 聊聊血液 发表于陕西省
该研究的2年随访数据表明,纳基奥仑赛注射液在R/R B-ALL中表现出令人鼓舞且持久的反应,且具有可控的安全性,证实了其对这一患者群体的潜在治疗获益。
纳基奥仑赛注射液
2023年11月,我国首款针对白血病领域的CAR-T细胞产品——纳基奥仑赛注射液(Inaticabtagene Autoleucel;CNCT19)获得国家药品监督管理局(NMPA)正式批准,用于治疗成人复发难治性B细胞急性淋巴细胞白血病(R/R B-ALL)。其关键性注册临床研究HY001201研究(NCT04684147)为一项在中国10家临床中心开展的前瞻性、多中心、单臂2期研究,2022年第64届ASH曾以口头报告的公布39例患者的结果,显示总缓解率(ORR)达82.1%,中位随访9.3个月时中位缓解持续时间(DOR)未达到;≥3级上细胞因子释放综合征(CRS)发生率为10.3%,≥3级免疫效应细胞相关神经毒性综合征(ICANS)发生率为7.7%,无非预期靶向CD19 CAR-T治疗导致的不良事件。
近日《Blood Advances》发表了48例患者随访2年的结果,通讯作者为中国医学科学院血液病医院(中国医学科学院血液学研究所)王建祥教授,王迎教授和合源生物科技(天津)有限公司吕璐璐博士为共同第一作者。

研究结果
该研究纳入48例接受纳基奥仑赛注射液输注(中位剂量0.53×108CAR阳性T细胞)的成人R/R B-ALL患者并进行疗效和安全性评估。其中34例患者达到并维持缓解超过3个月,3个月ORR(定义为完全缓解率或完全缓解伴不完全血液学恢复率[CR/CRi])为70.8%,高于历史对照的25%(P<0.0001),达到主要终点;最佳ORR为85.4%,所有应答者均达到微小残留病(MRD)阴性。41例应答者中12例(29.3%)在缓解期接受了移植巩固。此外基于不同的基线和临床协变量,所有亚组均显示获得缓解。
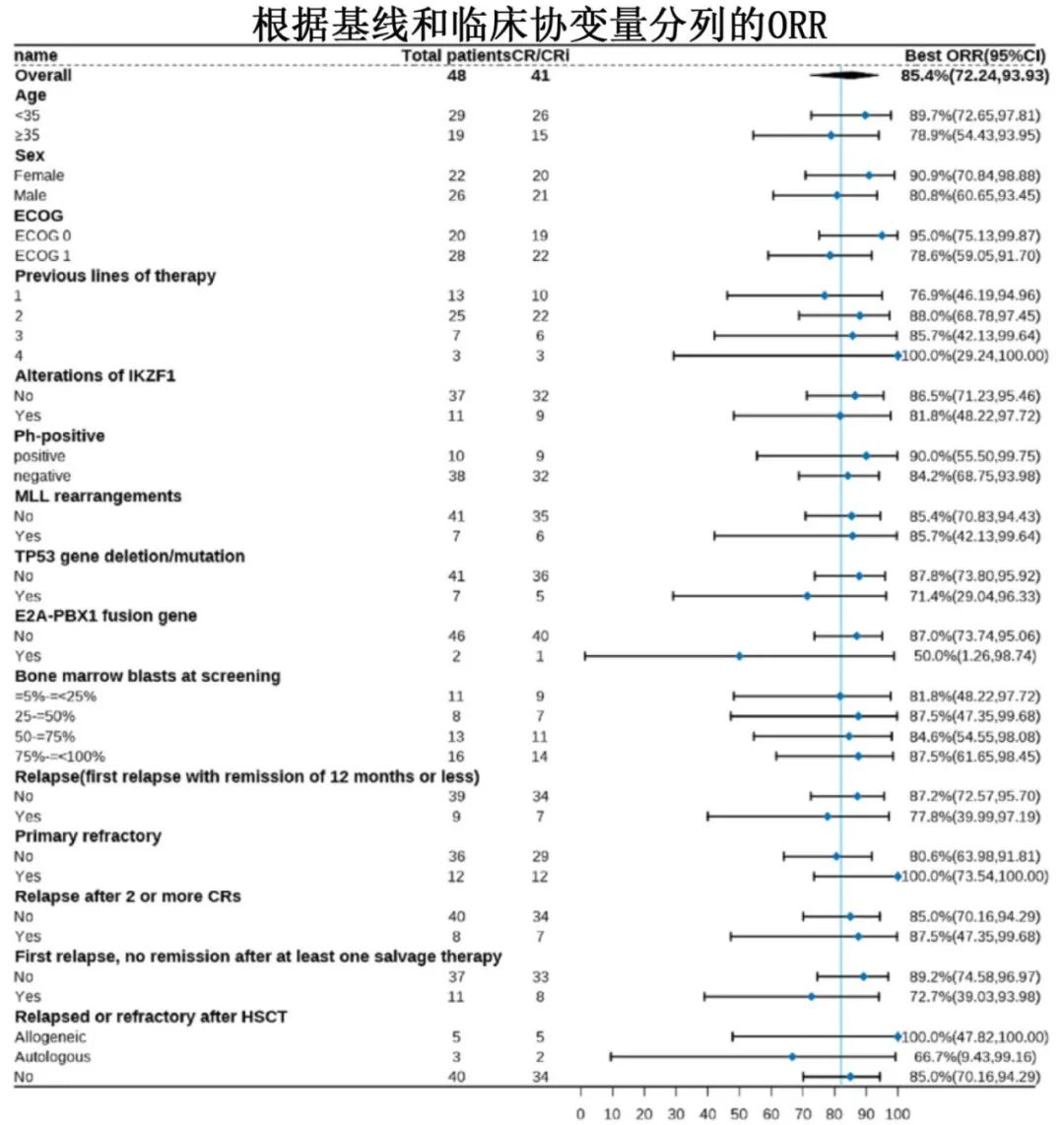
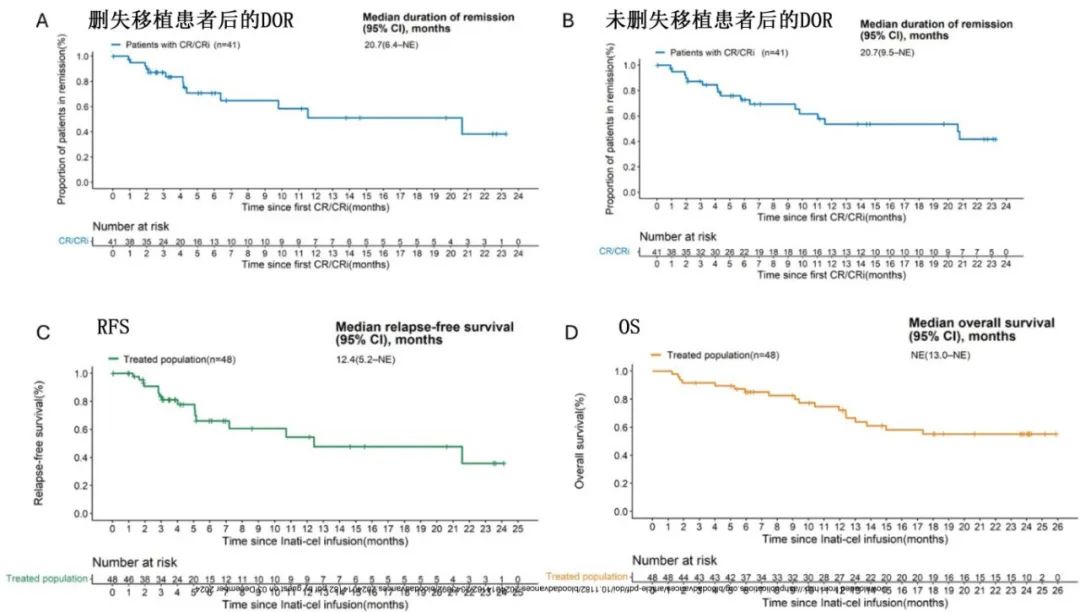
中位随访23.7个月,中位DOR为20.7个月,中位总生存期(OS)未达到,2年OS为55.2%,中位无复发生存期(RFS)为12.4,2年RFS为35.8%。≥3级CRS和ICANS分别为12.5%和6.2%。
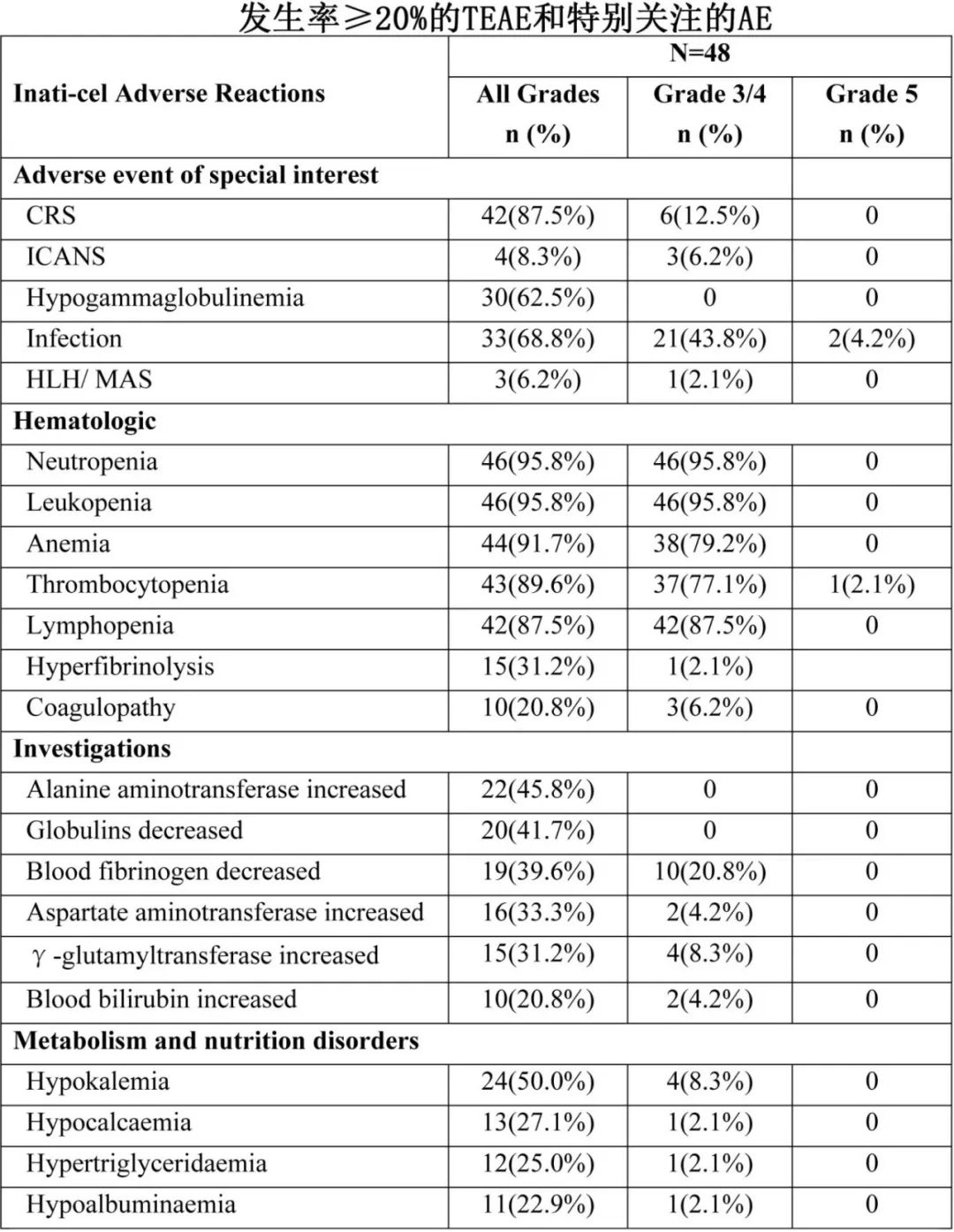
治疗期间发生的不良事件(TEAE)发生率为97.9%,最常见的是血液学不良事件。87.5%的患者发生CRS,≥3级仅有12.5%;8.3%的患者发生ICANS,≥3级为6.2%。噬血细胞性淋巴组织细胞增生症/巨噬细胞活化综合征(HLH/MAS)发生率为6.2%。低丙球蛋白血症发生率为62.5%,均为1-2级。感染发生率为68.8%,≥3级发生率为47.9%。
总结
该研究的2年随访数据表明,纳基奥仑赛注射液在R/R B-ALL中表现出令人鼓舞且持久的反应,且具有可控的安全性,证实了其对这一患者群体的潜在治疗获益。
参考文献
Ying Wang, Lulu Lv, Yongping Song, Xudong Wei, Hongsheng Zhou, Qifa Liu, Kailin Xu, Dongmei Yan, Cheng Zhang, Shuangyou Liu, Jie Jin, Heng Mei, Ting Niu, Aibin Liang, Runxia Gu, Jienan Ren, Yi Feng, Wei Jin, Yan Zhou, Yiping Deng, Jianxiang Wang; Inaticabtagene Autoleucel (CNCT19) in adult relapsed or refractory B-cell acute lymphoblastic leukemia. Blood Adv 2024; bloodadvances.2024014182. doi: https://doi.org/10.1182/bloodadvances.2024014182
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#B-ALL# #纳基奥仑赛#
4