JAMA Oncol:大规模队列研究揭示新辅助ICI治疗对早期乳腺癌特定表型患者有益
2024-09-22 测序中国 测序中国 发表于上海
鉴于新辅助ICI疗法的高效性和经济成本,研究团队建议未来研究可着重确定可从新辅助ICI治疗中获益的乳腺癌患者,以便临床决策。
近期的研究分析了免疫检查点抑制剂(ICI)联合(新)辅助化疗治疗早期乳腺癌。但关于这一联合治疗策略的最佳方法仍存在争论。
近日,西班牙巴塞罗那医院研究团队在JAMA Oncology发表了题为“Neoadjuvant Immune Checkpoint Inhibitors Plus Chemotherapy in Early Breast Cancer”的研究文章,通过荟萃分析系统地阐述了新辅助ICI疗法联合化疗与早期三阴性乳腺癌(TNBC)、早期PD-L1阳性/ERBB2阴性乳腺癌预后改善相关。鉴于新辅助ICI疗法的高效性和经济成本,研究团队建议未来研究可着重确定可从新辅助ICI治疗中获益的乳腺癌患者,以便临床决策。

免疫细胞表达的免疫检查点能够调节免疫激活的程度,适当的活性可以调控免疫活动,维持生物稳态。如果免疫检查点功能失常或过度激活,就会引起疾病产生。肿瘤细胞正是利用了免疫检查点作为“刹车系统”的特点,表达PD-L1等因子负向调节T细胞活化与增殖,从而实现免疫逃逸。应运而生的ICI疗法是通过阻断免疫检查点与其配体的结合来解除免疫抑制,从而激活免疫细胞发挥抗肿瘤作用。
ICI疗法最初在黑色素瘤[1]等癌症中进行了评估,后来证实其在转移性TNBC中具有改善疗效的作用,并将新辅助ICI联合化疗扩展到了TNBC之外的乳腺癌亚型中,例如ERBB2+ HR+/ERBB2-表型。在该最新分析中,研究团队评估了跨分子表型早期乳腺癌(EBC)患者的新辅助ICI治疗与病理完全缓解(pCR)的关系,量化了pCR状态之外ICI治疗的生存益处,并估计了特定不良事件的发生率。
对不同乳腺癌表型的治疗效果
研究团队纳入了9项临床随机试验(PCTs)研究,共5114例早期乳腺癌(EBC)患者(2097例TNBC,1924例HR+/ERBB2-,1115例ERBB2+),其中2802例接受了新辅助ICI治疗,2312例未接受ICI治疗。
研究评估了全部患者的pCR指标,发现新辅助ICI治疗可提高TNBC的总pCR率(46.6%增至59.9%),其中PDL1+与PDL1-肿瘤的获益程度相近(图1)。HR+/ERBB2-肿瘤经新辅助ICI治疗后,总pCR率从14.8%提高到24.6%,并主要由PDL1+队列获益。ERBB2+肿瘤并未观察到新辅助ICI治疗的益处。
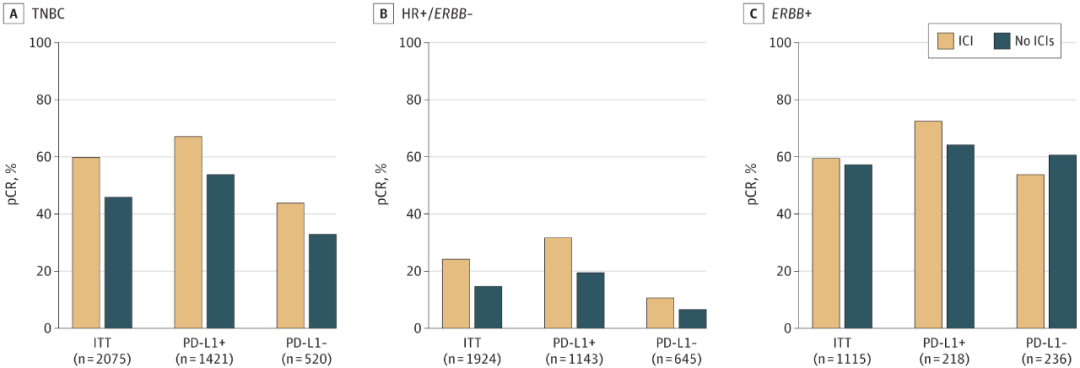
图1.不同乳腺癌表型接受新辅助ICI治疗的获益程度
对TNBC患者生存结局的影响
新辅助ICI治疗可改善TNBC患者的无病生存期(EFS),无论其是否达到pCR。
在达到pCR的TNBC患者中,研究团队将KEYNOTE-522[2]和IMpassion031[3]实验组的pCR患者与GeparNuevo和I-SPY2实验组的pCR患者进行了比较,发现新辅助ICI治疗改善了pCR患者的EFS,接受ICI治疗的患者5年EFS为92.0%,未接收ICI治疗的患者5年EFS为88.0%。
在具有残余病灶的患者队列中,接受和未接受新辅助ICI治疗的患者之间的EFS风险比为1.64。新辅助ICI辅助治疗表现出更好的EFS,接受ICI治疗的患者5年EFS为63.3%,未接受ICI治疗的患者EFS为56.1%。无论是pCR还是残留病灶患者,新辅助ICI治疗均未显示出数值上的改善(所有风险比均>1)。
ICI治疗提高了用药不良反应发生率
ICI治疗效果可能受到免疫治疗相关不良反应(irAEs)的影响,但是发生频率和严重程度各异,其中最常见的irAEs为疲劳、瘙痒、皮疹和腹泻[4,5]。因此,研究团队探究了ICI治疗与不良反应(AE)发生率的相关性。
在新辅助治疗阶段,ICI治疗导致患者出现3级或更高级别AE的发生率增加9.5%;在接受和未接受ICI治疗的患者中,因AE停药的患者分别为20.4%和12.2%。最常见的AE包括恶心、疲劳和中性粒细胞减少症。
在接受ICI治疗的患者中,任何级别甲状腺功能减退症和甲状腺功能亢进症的发生率分别为13.3%和6.1%,有10.3%的患者出现3级或更高级别的irAEs。
综上所述,该系统研究整合9项RCT数据评估了ICI联合新辅助化疗治疗早期乳腺癌的疗效与安全性,阐明了ICI治疗对患者pCR及其他指标的影响,并揭示ICI疗法对TNBC、HR+ PDL1+/ERBB2-患者有益,并具有可接受的安全性;而于ERBB2+患者而言无明显益处。考虑到与ICI相关的经济和毒性成本,未来的研究应优先确定最有可能从ICI联合新辅助化疗治疗中获益的患者。该研究为临床乳腺癌治疗决策提供了新的见解与依据。
原文链接:
https://jamanetwork.com/journals/jamaoncology/article-abstract/2822926
参考文献:
[1] Amaria RN, Reddy SM, Tawbi HA, et al. Neoadjuvant immune checkpoint blockade in high-risk resectable melanoma. Nat Med. 2018;24(11):1649-1654.
[2] Schmid P, Cortes J, Dent R, et al. Pembrolizumab or placebo plus chemotherapy followed by pembrolizumab or placebo for early-stage TNBC: updated event-free survival results from the phase III KEYNOTE-522 Study. Ann Oncol. 2023;34(suppl 2):S1257.
[3] Mittendorf EA, Zhang H, Barrios CH, et al. Neoadjuvant atezolizumab in combination with sequential nab-paclitaxel and anthracycline-based chemotherapy versus placebo and chemotherapy in patients with early-stage triple-negative breast cancer (IMpassion031): a randomised, double-blind, phase 3 trial. Lancet. 2020;396(10257):1090-1100.
[5] Khan Z,Hammer C,Guardino E,et al. Mechanisms of immune-related adverse events associated with immune checkpoint blockade: using germline genetics to develop a personalized approach[J]. Genome Med,2019,11(1):39.
[6] Wang Y,Zhou S,Yang F,et al. Treatment-related adverse events of PD-1 and PD-L1 inhibitors in clinical trials:a systematic review and meta-analysis[J]. JAMA Oncol,2019,5(7):1008-1019.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#乳腺癌# #新辅助ICI治疗#
60