真实世界中,乳腺癌和妇科肿瘤患者获益于NGS指导的靶向治疗,有的甚至改变临床诊断
2024-06-23 苏州绘真医学 苏州绘真医学 发表于上海
这项回顾性研究可能提供进一步的真实世界证据,证明精准肿瘤学可以改善一小部分接受过大量治疗的晚期妇科癌症和乳腺癌患者的临床结果。
通过分子肿瘤委员会(MTB)的实施,精准肿瘤治疗在乳腺和妇科肿瘤中得到越来越广泛的应用,但现实世界的临床结果数据仍然有限。对2018年至2023年转诊至本中心MTB的乳腺癌(BC)和妇科恶性肿瘤患者进行了回顾性分析。分析涵盖患者特征、下一代测序(NGS)结果、MTB建议、接受的治疗和临床结果。
63 名患者(77.8%)患有转移性疾病,44名患者(54.3%)之前接受过三线或更多线全身治疗。50名患者(63.3%)获得了个体化治疗建议,29名患者(36.7%)没有可干预的靶点。最终,23名患者(29.1%)接受了分子匹配治疗(MMT)。泛妇科肿瘤(BC和妇科恶性肿瘤)患者常见的变异基因包括TP53(n=42/81,51.9%)、PIK3CA(n=18/81,22.2%)、BRCA1/2(n=10/81,12.3%)和ARID1A(n=9/81,11.1%)。接受MMT治疗的患者的无进展生存期显著延长(中位PFS 5.5个月 vs. 3.5个月,p=0.0014)。在所有接受分子分析的患者中,13.6%通过精准肿瘤学获得了主要临床获益(PFSr ≥ 1.3 和 PR/SD ≥ 6个月)。总体而言,在真实世界中,使用panel诊断的NGS指导精准肿瘤学在乳腺癌和妇科癌症患者亚组中显示出了改善的临床结果。
研究背景
NGS能够在临床环境中快速、经济高效地表征肿瘤复杂的突变谱。迄今为止,临床诊断的首选NGS方法包括靶向基因panels,可以检测多种已明确表征的基因变异,包括短结构变异(SSV)、拷贝数变异(CNA)、易位和多个基因的融合。然而,由于近年来可治疗的基因变异和预测性生物标志物的迅速扩展,精准肿瘤学也已变得可行,尤其是在肺癌和妇科肿瘤学领域。值得注意的是,英国十万基因组计划于2024年1月发布的最新数据提供了13,880个实体瘤的全基因组测序(WGS)信息。研究结果显示,20-49%的妇科癌症存在临床相关突变,包括乳腺浸润性癌、卵巢高级别浆液性癌和子宫内膜癌。相比之下,胰腺癌、前列腺癌、食道癌和胃腺癌等其他癌症在不到20%的病例中表现出临床相关突变。
近年来,乳腺癌和妇科肿瘤领域新的精准肿瘤疗法迅速增多,靶向生物标志物的治疗带来了更显著的生存获益。尤其是聚(ADP-核糖)聚合酶(PARP)抑制剂已获批用于靶向治疗BRCA突变或同源重组缺陷(HRD)上皮性卵巢癌以及胚系BRCA突变乳腺癌(BC)。此外,FDA已批准使用帕博利珠单抗作为肿瘤不可知疗法,用于治疗微卫星不稳定性高(MSI-H)、错配修复缺陷(MMRd)或肿瘤突变负荷高(TMB-H)的转移性肿瘤。TMB-H和MSI-H是免疫检查点阻断疗法取得阳性反应的预测因素,尤其是在子宫癌、宫颈癌和外阴癌等实体癌中。例如,仅在2023年,FDA就批准了艾拉司群用于治疗ESR1突变的BC,戈沙妥珠单抗用于治疗HR阳性和Her2阴性BC,并批准了泛AKT抑制剂卡帕塞替尼用于治疗HR阳性、Her2阴性晚期或转移性BC,且存在一个或多个PIK3CA/AKT1/PTEN变异。
与这些发展相反,SHIVA试验(首个分析精准肿瘤学结果的随机试验)表明,对于接受过大量治疗的癌症患者,与医生选择的治疗相比,使用多基因测序和超出推荐适应症分子靶向药物并不能提高PFS。鉴于其他研究也同样报告了精准肿瘤学并无益处,这些结果被认为令人非常失望。然而,必须注意的是,自2012年至2014年SHIVA试验招募期以来,可用的癌症治疗方法大幅增加,同时获得负担得起的基于NGS的先进分子肿瘤分析的机会也得到了改善。与这些进展一致,最近发表的论文证明精准医疗可以改善乳腺癌和妇科癌症患者的预后。
重要的是,Charo等人发现,接受更高程度匹配治疗的乳腺癌和妇科癌症患者的总体反应率和无进展生存期都有所增加,并且总体生存率有改善的趋势。然而,SAFIR02-BREAST试验是一项前瞻性随机研究,比较了转移性BC患者的靶向疗法与标准治疗(SoC)治疗,其结果显示,只有欧洲肿瘤内科学会(ESMO)分子靶点临床可操作性量表(ESCAT)分类为 I/II 级的基因变异才可改善 PFS,不能超过II级。因此,精确肿瘤学的益处仅限于有高水平证据表明所确定的变异具有治疗可干预性的病例。
在这项回顾性研究中,旨在评估NGS指导的精准肿瘤学在乳腺癌和妇科癌症临床实践中的应用,分析患者特征、肿瘤特异性基因变异、治疗建议和结果,以提供额外的真实世界数据并评估NGS指导精准肿瘤学的临床益处。本研究中PFS的计算方法是从开始使用推荐的匹配疗法(或不匹配的疗法/医生的选择)的第一天开始,直到疾病进展或死亡。PFS比值(PFSr)的计算方法是从匹配或不匹配疗法开始的进展时间(PFS2)除以与最后一次先前全身治疗相关的进展时间(PFS1)。PFSr>1.3被认为提示匹配疗法的PFS有所改善。研究者认为PFSr≥1.3和SD≥6个月为主要临床获益。
研究结果
研究人群和 MTB 工作流程:
2018年8月至2023年8月,84例乳腺癌或其他妇科恶性肿瘤患者转诊到本中心的MTB进行扩展分子诊断。扩展分子诊断包括 67 或 185 个基因的 NGS panel,用于检测短结构变异(SSV)和拷贝数变异(CNA),以及 53 或 137 个基因的融合panel。在选定病例中进行的MMRD/MSI(涉及错配修复蛋白 MLH1、PMS2、MSH2 和 MSH6,其中一种或多种蛋白质的核染色丧失表明肿瘤中存在错配修复缺陷)、Her2和PD-L1表达(抗体克隆号E1L3N)的免疫组织化学补充了 NGS 分析。由于组织不足以进行诊断,三名患者被排除在本分析之外,两名患者在分子分析结束前死亡。总共有79名患者在MTB中进行了讨论,其中50名患者(63.3%)获得了个体化治疗建议,而其余29名患者(36.7%)未确定可干预的靶点。最终有23例(29.1%)患者接受了分子匹配治疗(MMT),但有 27 例(34.2%)患者未接受 MMT,原因包括医生偏向其他治疗方案(14/27)、决定采用最佳支持治疗(BSC)(4/27)、医疗保险公司拒绝承担费用(2/27)、分子匹配治疗后不久死亡(4/27)或失访(3/27)(图 1)。
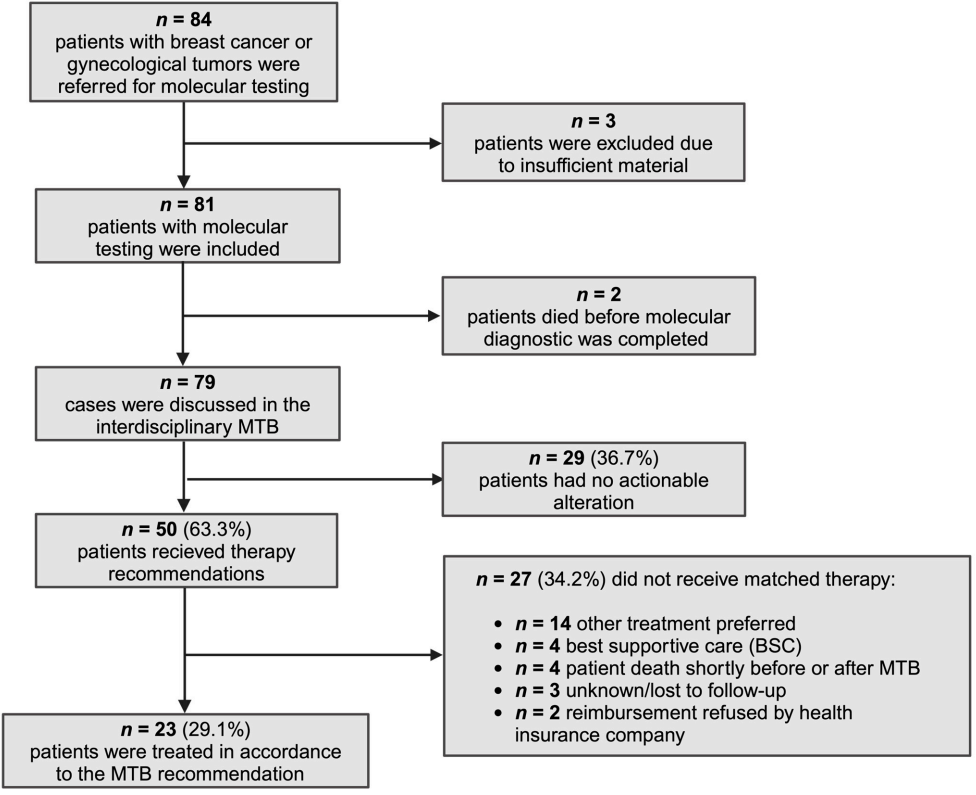

图1
接受NGS分析的患者特征:
本回顾性分析包括81名乳腺癌或妇科恶性肿瘤患者,建议进行扩展分子诊断。转诊时的中位年龄为 59 岁。大多数患者(77.8%)患有转移性疾病,59 名患者(72.8%)最初接受了治愈性治疗,随后复发或进展到转移期。共有 22 名患者(27.2%)在诊断时已经患有转移性疾病。患者中的主要癌症类型是乳腺癌(44.4%),其次是卵巢癌(25.9%)和子宫肉瘤(7.4%)。超过50%的患者在讨论 MTB 之前已经接受过三线或更多线全身治疗(表1)。
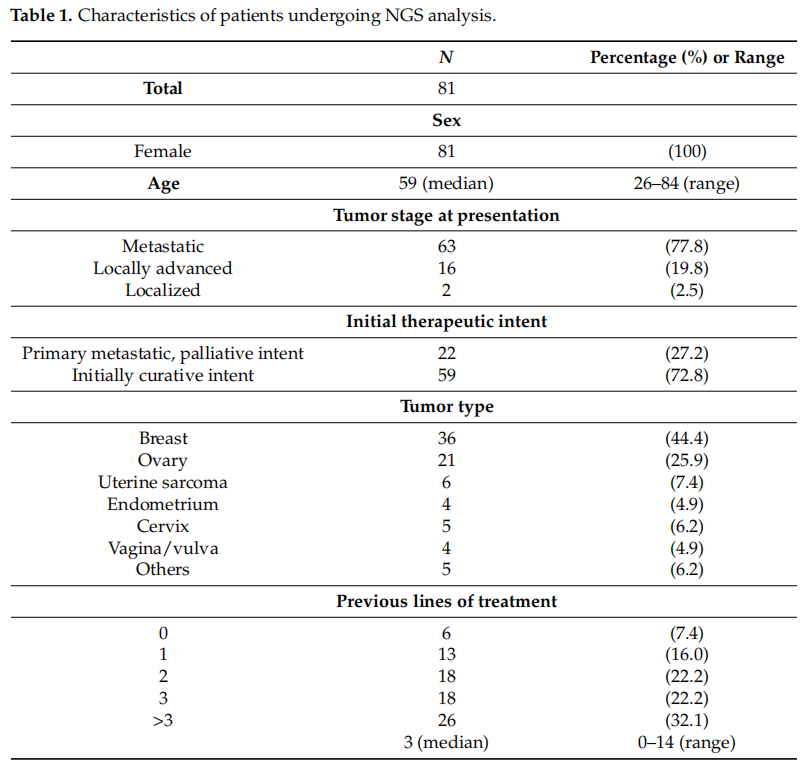
表1
分子检测和治疗建议:
对 81 名患者进行了完整的 NGS 诊断(FP + VP)。36名乳腺癌患者中最常见的变异基因是 TP53(n = 20/36,55.6%)、PIK3CA(n = 14/36,38.9%)、ATM(n = 6/36,16.7%)和 BRCA1/2(n = 4/36,11.1%)。45 名妇科癌症患者中最常见的变异基因是 TP53(n = 22/45,48.9%)、ARID1A(n = 6/45,13.3%)、BRCA1/2(n = 6/45,13.3%)和 KRAS(n = 5/45,11.1%)(图2a)。在所有 81 名接受分子检测的泛妇科肿瘤(BC和妇科恶性肿瘤)患者中,常见的变异基因包括 TP53 ( n = 42/81,51.9%)、PIK3CA ( n = 18/81,22.2%)、BRCA1/2 ( n = 10/81,12.3%) 和 ARID1A ( n = 9/81,11.1%)。最常见的 PIK3CA 突变包括可靶向的 H1047R、E542K 和 E545K 热点突变以及 PIK3CA 基因扩增。根据 ESCAT 和 NCT/DKTK 量表,检出的 PIK3CA 和 BRCA 突变(主要为 Tier I 或 m1)的治疗可行性证据水平最高。对于其余发现的变异,证据级别主要为 III 级或 m2(图 2b、c)。
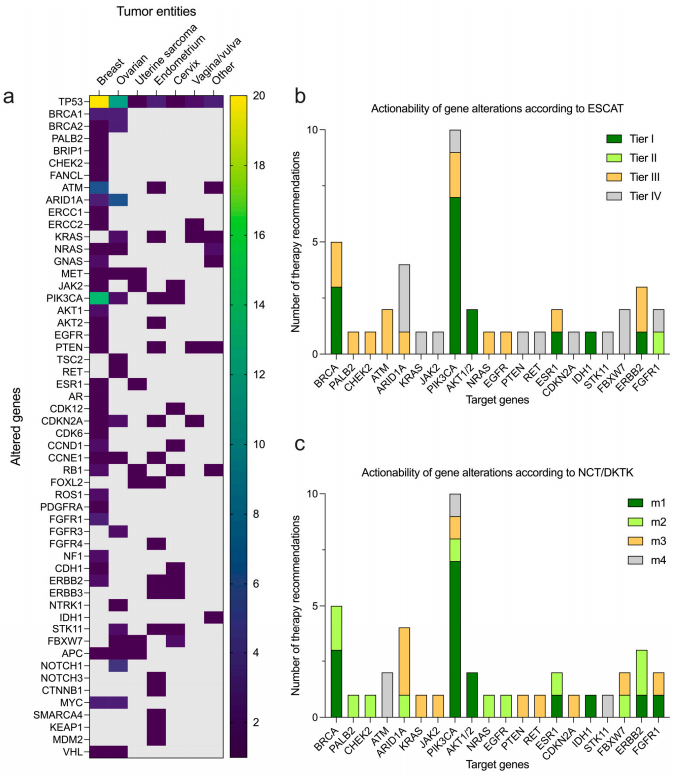

图2
共有 14 名患者出现基因融合,表 2总结了具有精确定义断点的特定融合及其相关性。在本队列中发现了一些特别具有表征性的基因融合,例如乳腺幼年分泌性癌(JSCV)患者的NTRK-ETV6(使用 NTRK 抑制剂 (恩曲替尼) 进行肿瘤不可知治疗的分子原理)、VMM(外阴/阴道粘膜黑色素瘤)中的TRIM24-BRAF(MEK 抑制剂 (曲美替尼) 的分子原理)以及 FGFR2-TACC2(FGFR 抑制剂 (佩米替尼) 的分子原理)(表 2)。非常罕见的 KIF5B-RET 基因融合,以前仅在少数乳腺癌患者中发现,可以用 FDA 批准的靶向 RET 抑制剂塞普替尼治疗。总体而言,KIF5B-RET 融合是非小细胞肺癌最常见的致癌驱动因素(约占所有病例的 1-2%),可以用塞普替尼成功治疗。然而,该种 MTB 的分子分层建议无法应用,因为患者在 MTB 后几天死亡。此外,研究者在文献中首次描述了VPDC(低分化阴道癌)中的 SYN2-PPARG 基因融合和UUC(子宫未分化癌)中的 YAP1-MAML2 融合。BCOR2-ZC3H7B 融合的检测导致了非常罕见的诊断,即具有 BCOR2-ZC3H7B 融合的高级别ESS(子宫内膜间质肉瘤)的高度侵袭性亚型(表 2)。
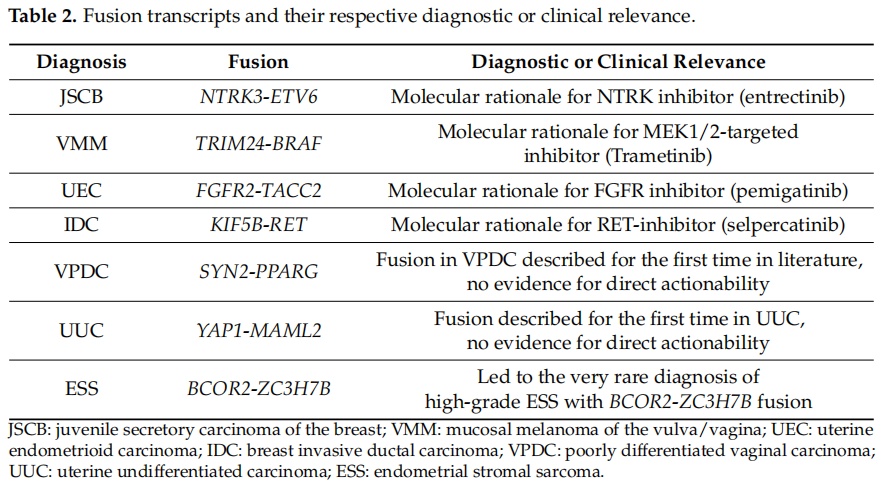
表2
MTB 推荐治疗的结果:
81名完成分子诊断的患者中,23名接受了分子匹配治疗,并接受了随访以进行临床结果分析。在其余 58 名未接受分子匹配治疗的患者中,6 名患者在 MTB 会诊之前或之后不久死亡,7 名患者接受了 BSC,7 名患者仍采用之前的治疗方案,9 名患者由于随访时间短(<3 个月)而无法评估。总体而言,81 名患者中有 52 名在 MTB 讨论后接受了全身治疗,并可评估临床结果。使用 Kaplan–Meier 分析比较了接受 MTB 推荐治疗的患者的 PFS 以及根据医生的选择和乳腺和妇科肿瘤委员会的其他建议接受其他全身治疗的患者的 PFS。接受匹配治疗(MTB 推荐)的患者的 PFS(n = 23)显著延长(中位 PFS 5.5 vs. 3.5 个月,p = 0.0014,图3)。根据研究者对主要临床益处的初步定义,23 名可评估患者中有 11 名在接受 MTB 推荐治疗后获得了主要临床获益(PFSr ≥ 1.3 和 PR/SD ≥ 6 个月)(表3)。因此,在接受分子分析的 81 名乳腺癌或妇科恶性肿瘤患者中13.6%(11/81)的患者通过精准肿瘤学获得了非常显著的临床改善(主要临床获益)。特别是,一名阑尾粘液腺癌(MAAP)患者也受益于扩展的分子诊断,该患者之前曾被作为卵巢癌治疗。通过识别 MAAP 患者中常见的分子变异(表3),在新的组织病理学评估后相应地改变了诊断,并根据 MTB 的建议对该患者接受了 HIPEC 和化疗(FOLFOX)作为 SoC 治疗,并获得了 6 个月的 PR。此外,在一名被诊断为原发性转移性乳腺癌(mBC)且之前已接受过五线全身疗法的患者中,研究者通过扩展分子诊断检测到了PALB2 c.3202-1G>A 突变。随后确认该突变为胚系变异,不同于任何胚系或体细胞BRCA1/2序列变异(表3)。根据 MTB 的建议,患者接受了奥拉帕利治疗,并在 22 个月内病情稳定。这凸显了检测PALB2、CHEK2和RAD51C胚系序列变异的重要性,尤其是考虑到 PARP 抑制剂在 mBC 中的临床潜力,这超出了目前批准的适应症。
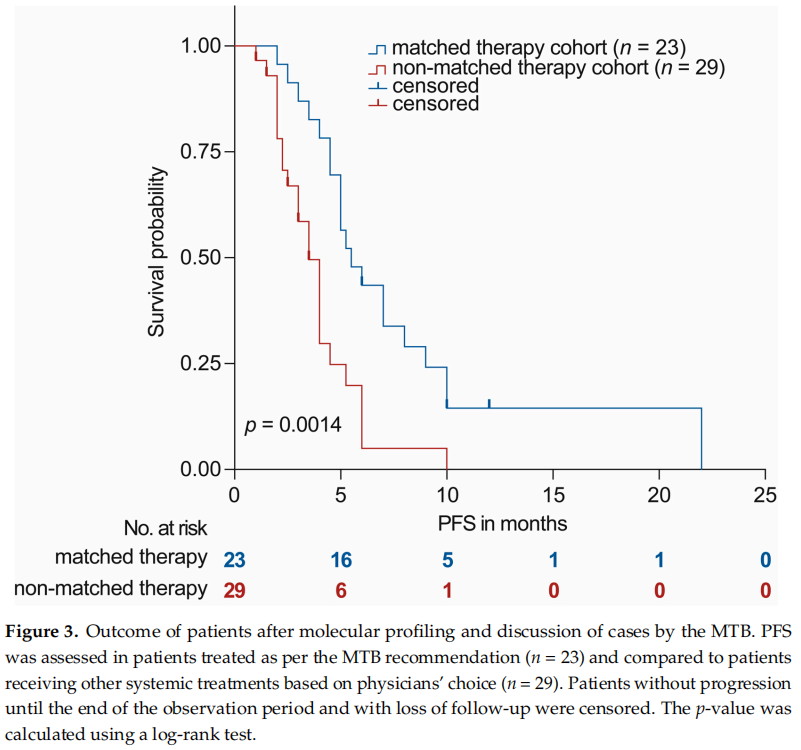
图3
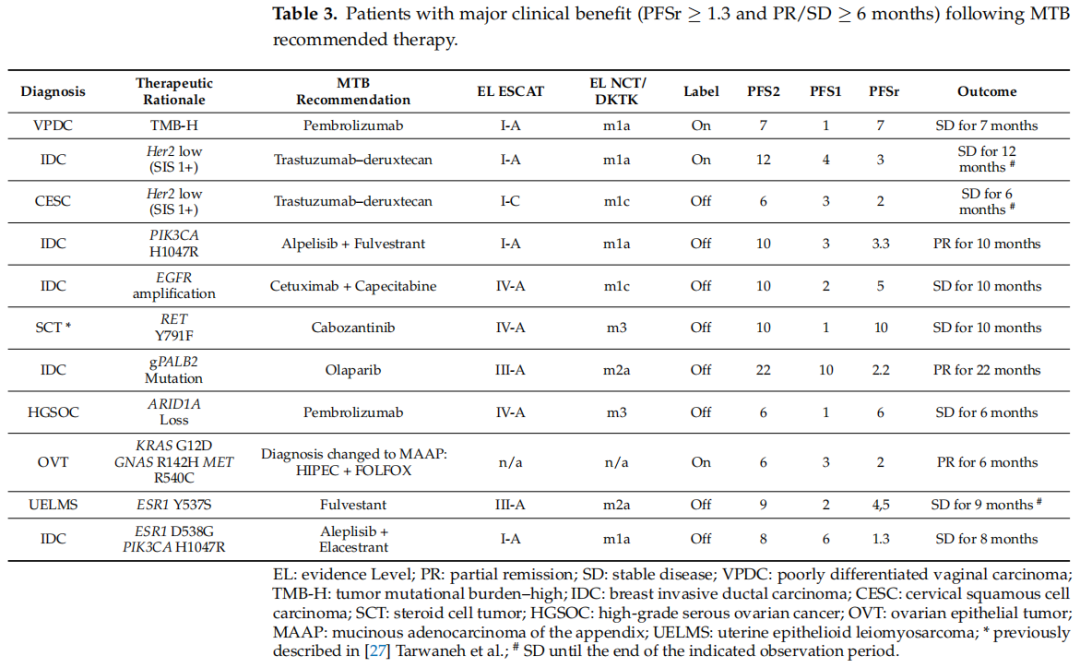
表3
为了分析匹配和非匹配治疗队列之间是否存在可能影响患者结果的异质性,研究者根据各种因素(就诊时的肿瘤分期、初始治疗意图、肿瘤类型和既往治疗线数)进行了队列分析。该比较显示,匹配和非匹配治疗队列中转移性(78.3% vs. 75.9%)、局部晚期(17.4% vs. 20.7%)和局部肿瘤分期(4.3% vs. 3.4%)的患者比例相似。匹配和非匹配治疗队列中的大多数患者最初接受的是治愈性治疗(69.6% vs. 75.9%),并且患有原发性转移性疾病(30.4 vs. 24.1%)。两个队列中的主要癌症类型是乳腺癌(43.5% vs. 48.3%),其次是卵巢癌(34.8% vs. 17.2%)和子宫内膜癌(8.7 vs. 13.8%)。在两个队列中,超过 60% 的患者在讨论 MTB 之前已经接受过三线或三线以上的全身治疗(表 4)。总体而言,匹配和非匹配治疗队列中的患者在肿瘤分期、初始治疗意图、肿瘤分期和既往治疗线数方面相当。
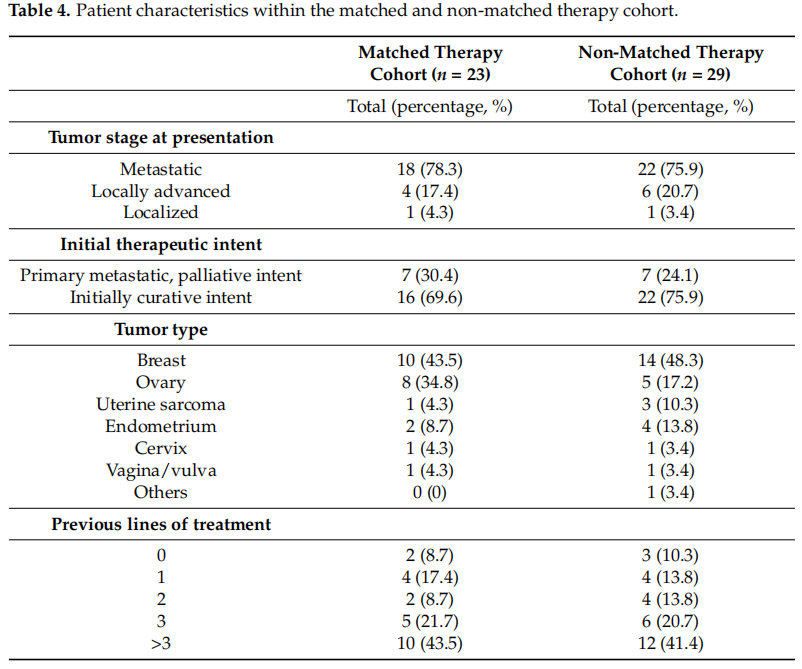
表4
讨 论
NGS指导的精准肿瘤学越来越多地用于确定晚期肿瘤患者的治疗方案,这些患者已用尽批准的SoC治疗方法。随着对癌症驱动基因分子功能、临床试验前景和潜在超说明书用药的可用性的了解迅速变化,MTB 对于识别和排序个案中标准治疗以外的治疗方法至关重要。在本研究中,MTB 讨论的所有患者中有63.3%得到了个体化治疗建议,这与最近其他针对乳腺癌和妇科肿瘤的研究结果一致。例如,Sultova等人报告称,95名BC和妇科恶性肿瘤患者中有41名(43.2%)有可干预的变异,而Bruzas等人报告称,他们的mBC队列中有63名患者(66.3%)适合MMT。在包含更多不同肿瘤实体的队列中,具有可干预变异的患者比例从Le Tourneau等人的39.5%到Walter等人的最高87%不等,受到研究人群在不同肿瘤实体和多样化突变状况方面的异质性的影响。
本研究分析了乳腺癌和妇科恶性肿瘤(泛妇科肿瘤)中的靶向分子图谱,最常见的突变是TP53、PIK3CA 、 BRCA1/2和ARID1A。这种模式与TCGA中2579个泛妇科肿瘤的分子数据以及164个泛妇科肿瘤患者MTB的真实世界靶向NGS数据非常相似。尤其是,两项研究都显示出TP53(TCGA 中为 44% vs. 泛妇科 MTB 分析中为 54%)、PIKC3CA(32% vs. 27%)、PTEN(20% vs. 15%)和ARID1A(14% vs. 15%)的变异率很高,与本研究的观察结果相似,而PTEN变异并不在本研究排名前四的变异基因之列。最后,本研究队列中仅 23 例患者(29.1%)接受了分子匹配治疗 (MMT),这与既往研究结果一致,但由于各种原因,接受 MTT 治疗的患者比例波动很大。例如,Pernas 等人在 SOLTI-1301 AGATA 研究中和 Aftimos 等人在 AURORA 研究中报道,分别只有 5% 和 7% 的患者接受了 MMT。相比之下,Parker 和 Walter 等人(各为42 %)和 Bruzas 和 Fukada 等人(分别为 36% 和26 %)报告的最终接受 MMT 治疗的患者比例与本研究相当。在文献中,拒绝推荐的 MTT 的原因包括医生或患者倾向于其他疗法、缺乏报销、无法获得药物以及疾病进展、导致某一患者在实际使用MMT时体能状态不佳或死亡。尤其是,其他研究强调,在进行panel测序时东部肿瘤协作组 (ECOG) 状态迅速恶化是限制个性化治疗潜在益处的一个重大缺点,这强调了在患者处于适合耐受 MTT 的状态时启动 NGS panel测序的重要性。
最后,在本研究中,接受匹配疗法(MTB推荐)治疗的泛妇科肿瘤患者的PFS显著延长(中位PFS 5.5个月 vs. 3.5个月,p=0.0014)。然而,在接受分子分析的81名患者中,只有一小部分(13.6%)通过精准肿瘤学获得了主要临床获益。在接受过大量治疗的晚期泛妇科肿瘤人群中,这一较低的临床获益率与MOSCATO-01研究的结果一致,MOSCATO-01研究是法国的一项单中心癌症筛查项目,针对包括乳腺癌在内的各种转移性恶性肿瘤患者转移部位的活检样本进行研究。研究的主要终点已经达到,948名患者中有63名(占所有入组患者的7%)的PFSr>1.3,受益于靶向药物治疗。在本机构的一项泛癌症队列回顾性分析中,9.6%的所有入组患者通过精准肿瘤学获得了重大临床益处,而在 Bruzas 等人发表的一项研究中,13.6%的mBC患者从NGS指导治疗中获得了临床益处。即使分析的基因数量增加,这一低百分比似乎在各种测序技术中保持不变。值得注意的是,尽管精确肿瘤学领域正在迅速向整合大型基因panels甚至全系统的测序方法和蛋白质组学或功能分析进入临床常规的方向发展,但本机构的MTB目前使用靶向测序分析来制定个性化治疗建议。重要的是,PERMED-01 试验的结果表明,全外显子组测序 (WES) 的使用并没有比仅分析几百个基因的基因panels产生更多的临床相关信息。然而,研究表明,患者的临床结果与ESCAT建议的水平及其依从性有关。具体而言,Andre等人的一项研究表明,MTT可改善具有ESCAT分类I/II级基因变异的PFS(调整后的HR:0.41,90%CI:0.27-0.61,p < 0.001),但并非在包括所有ESCAT级别建议的整个队列中都有效(调整后的HR:0.77,95%CI:0.56-1.06,p=0.109)。
尽管这项研究有很多优点,但它也存在一些局限性,这一点应该注意。解读本研究结果时的潜在偏倚源于其非随机设计(考虑到MTT决策的差异、分子分析的标准化、启动NGS诊断的时间点、NGS panel类型和临床随访)。然而,这些局限性反映了这项研究的真实世界性质。另一点是患者队列有限,在肿瘤实体和既往治疗方面表现出显著的异质性。尽管由于这项研究的回顾性而缺乏随机性,但本队列分析显示,匹配和非匹配治疗队列中的患者在肿瘤分期、初始治疗意向和既往治疗线数方面相当。最后,ESMO指南建议对卵巢癌、非鳞状 NSCLC、前列腺癌和胆管癌患者使用NGS。因此,对于这些适应症之外的妇科患者,NGS诊断的应用应根据个体情况进行评估。
这项回顾性研究可能提供进一步的真实世界证据,证明精准肿瘤学可以改善一小部分接受过大量治疗的晚期妇科癌症和乳腺癌患者的临床结果。
参考文献:
Gremke N, Rodepeter FR, Teply-Szymanski J, Griewing S, Boekhoff J, Stroh A, Tarawneh TS, Riera-Knorrenschild J, Balser C, Hattesohl A, et al. NGS-Guided Precision Oncology in Breast Cancer and Gynecological Tumors—A Retrospective Molecular Tumor Board Analysis. Cancers. 2024; 16(8):1561. https://doi.org/10.3390/cancers16081561

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#乳腺癌# #妇科肿瘤# #NGS#
5