NEJM:两个免疫治疗联合药物成功使恶性黑色素瘤消失
2015-04-22 MedSci MedSci原创
“纽约一分钟”是一个美国标语,意味着非常短暂或极度压缩的时间。它恰好可以描述最近发生在纽约斯隆•凯德琳癌症纪念研究中心的黑色素瘤病人的治疗反应。一位患有转移性黑色素瘤的49岁女病人,左胸下有一个具大有蒂的坏死性肿瘤,在进行一个剂量的试验性结合免疫治疗3周后,肿瘤消失了。肿瘤消失的程度和速度是难以置信的, 4月20日发表于NEJM上的MSK的三名临床医生书信中写道。 “这是我见
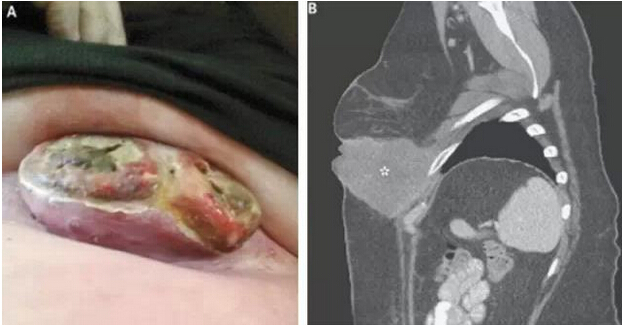
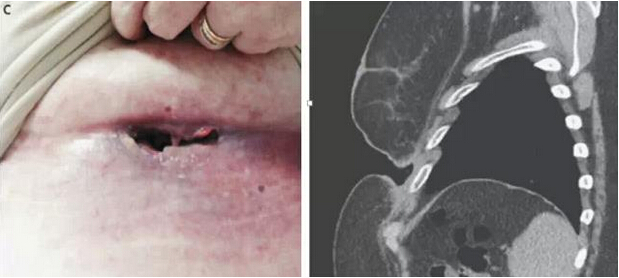
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#色素#
0
#黑色素#
44
#黑色素#
47
期待
118