铜代谢疾病:从Menkes病到Wilson病
2024-07-18 神经科学论坛 神经科学论坛 发表于上海
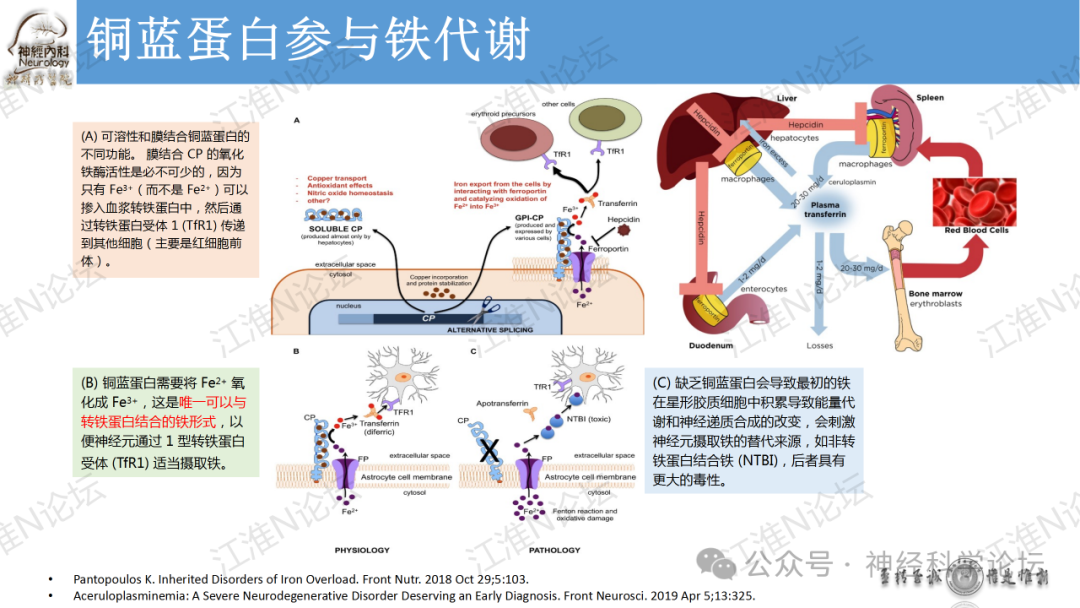
介绍与人类铜代谢疾病有关的基因,包括 Menkes 病、Wilson 病,还提到新发现的铜死亡,阐述相关基因作用及铜代谢异常导致的疾病。
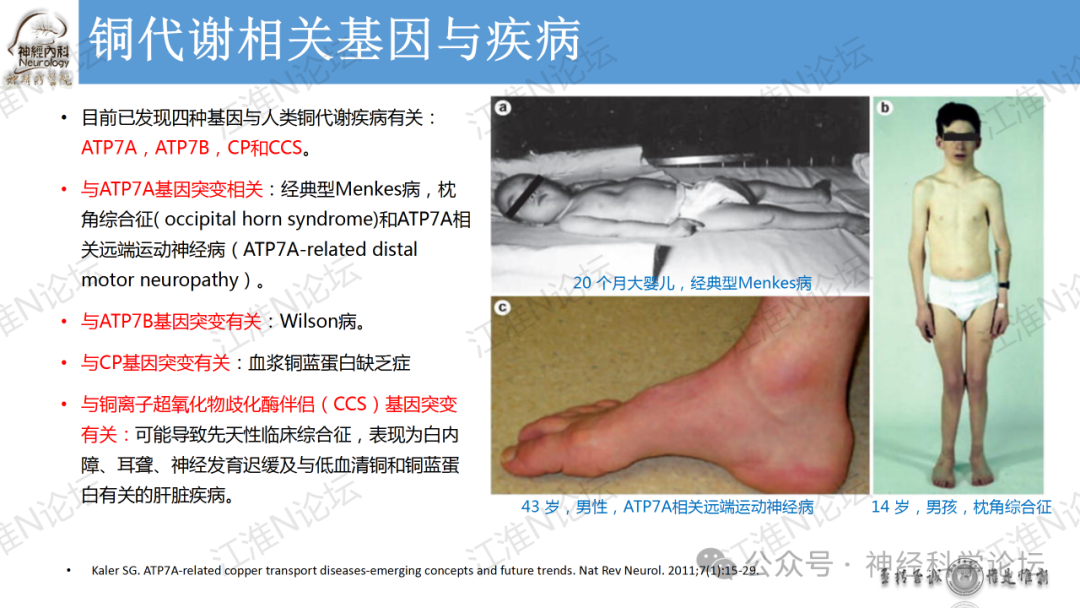
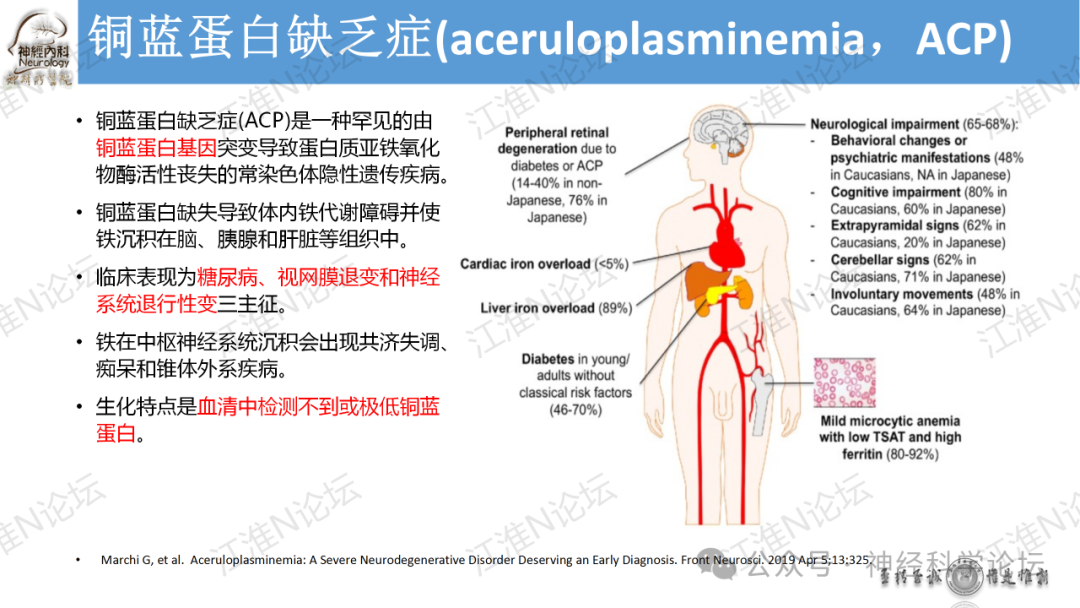
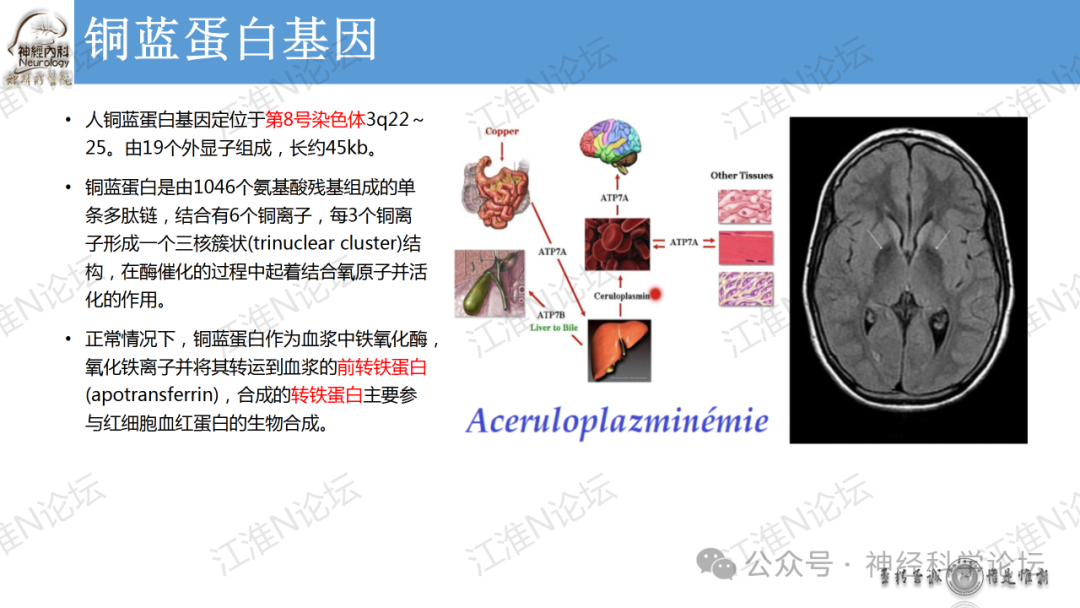
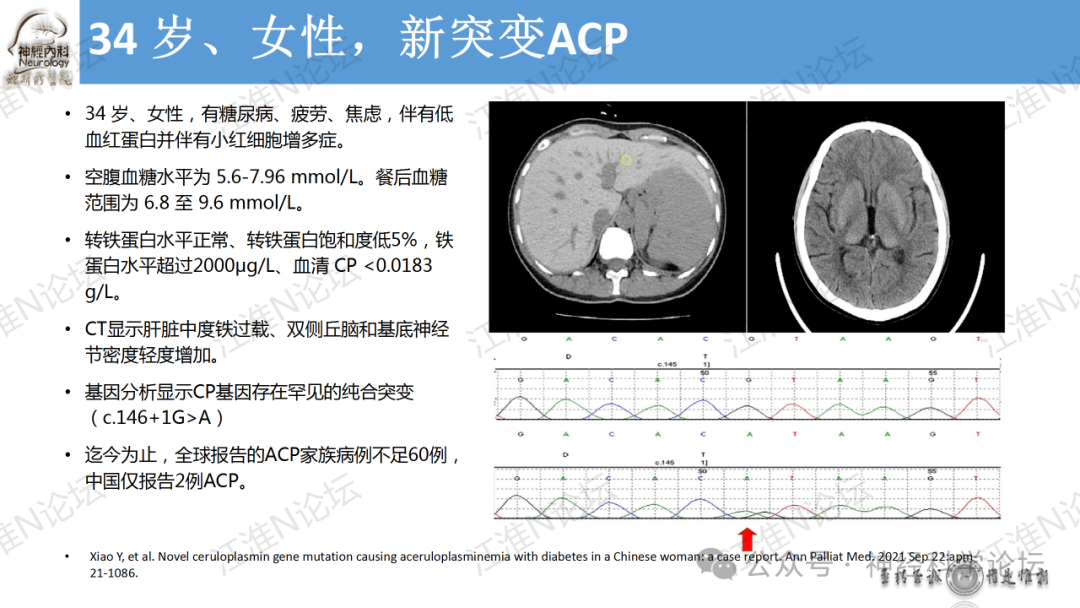
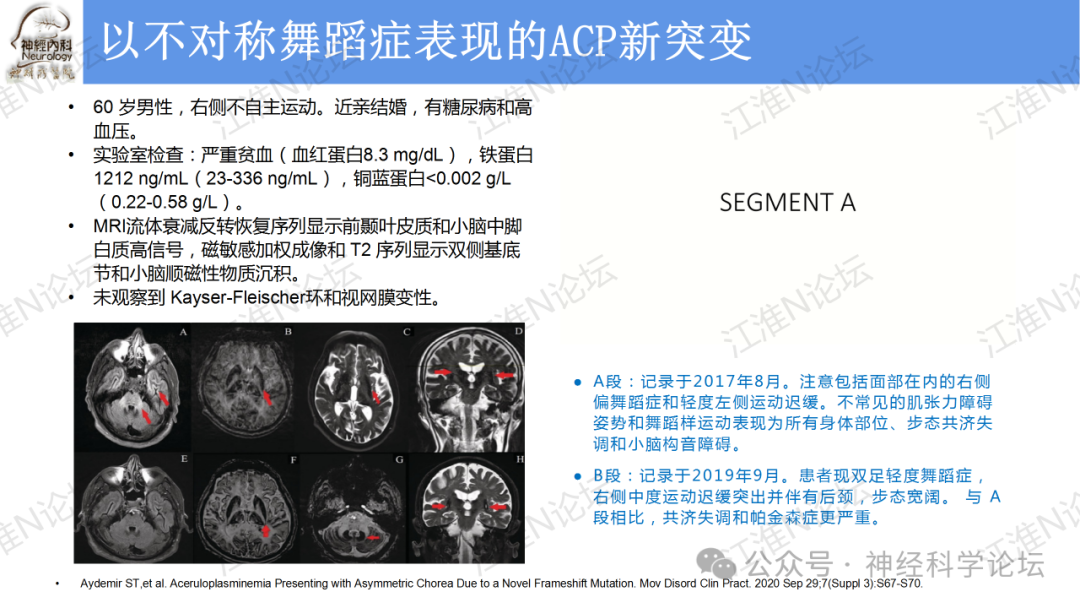
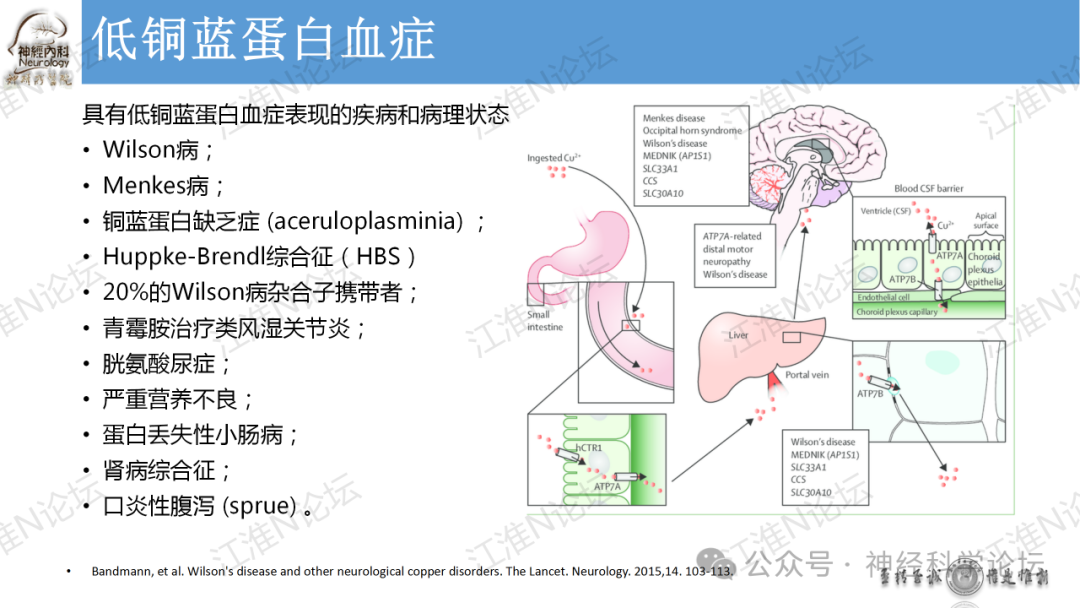
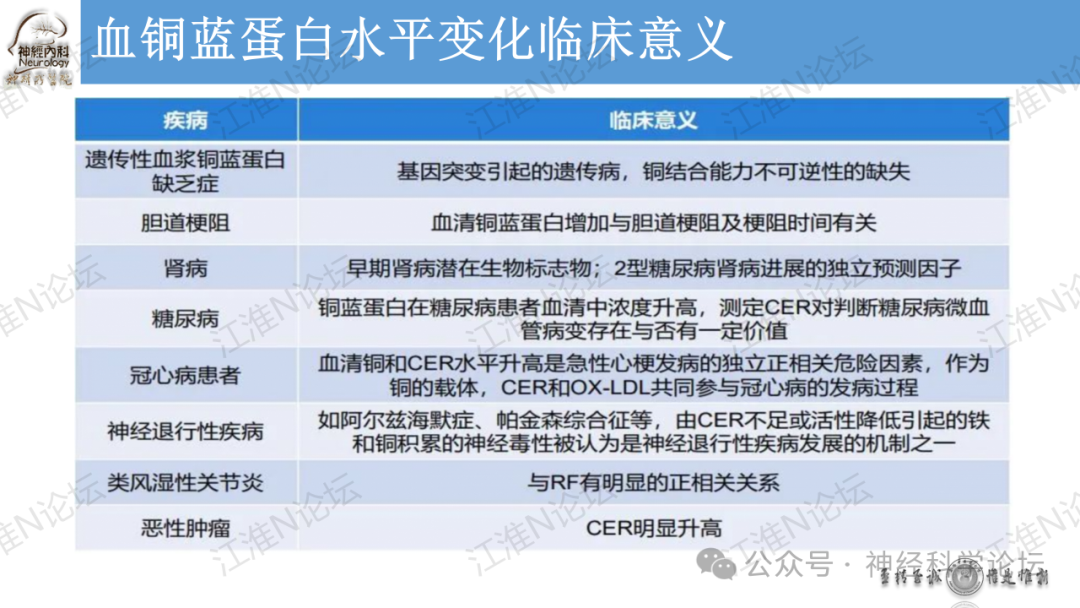
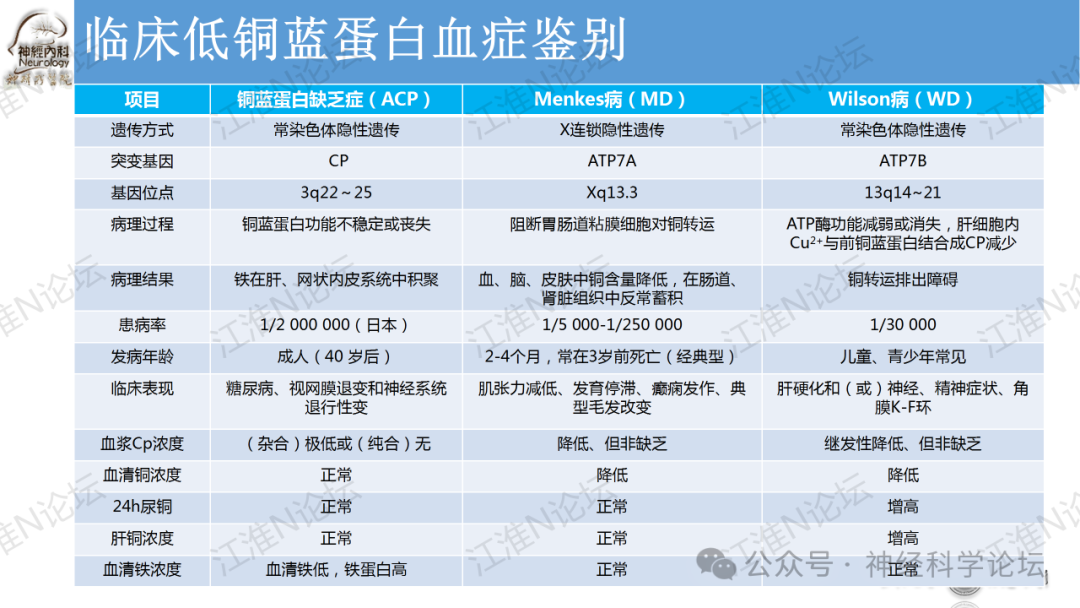
论坛导读:目前已发现四种基因与人类铜代谢疾病有关:ATP7A,ATP7B,CP和CCS。与ATP7A基因突变相关:经典型Menkes病,枕角综合征( occipital horn syndrome)和ATP7A相关远端运动神经病(ATP7A-related distal motor neuropathy)。与ATP7B基因突变有关:Wilson病。与CP基因突变有关:血浆铜蓝蛋白缺乏症与铜离子超氧化物歧化酶伴侣(CCS)基因突变有关:可能导致先天性临床综合征,表现为白内障、耳聋、神经发育迟缓及与低血清铜和铜蓝蛋白有关的肝脏疾病。
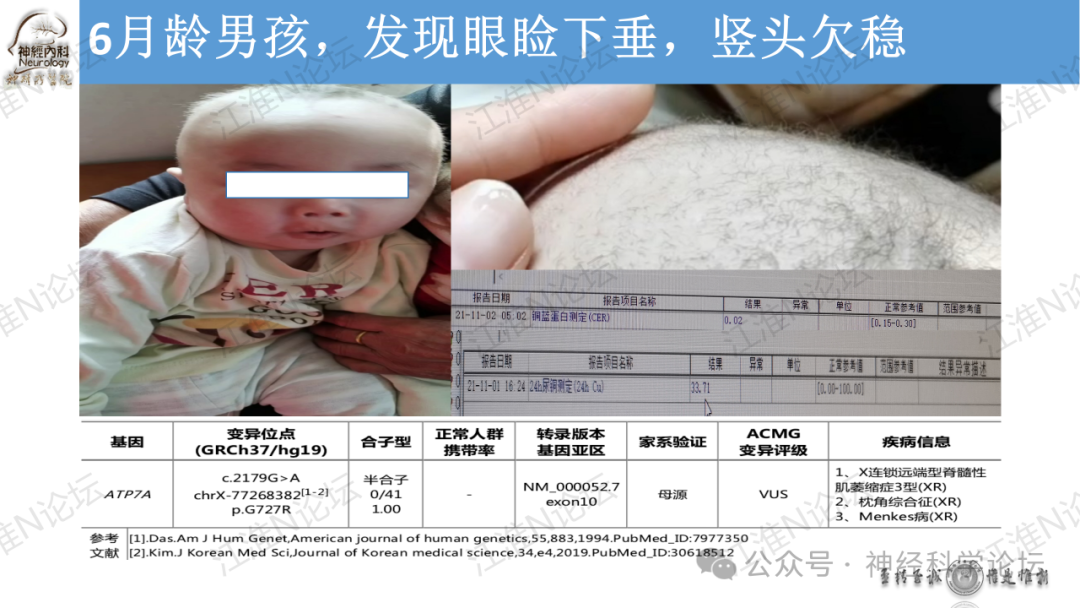
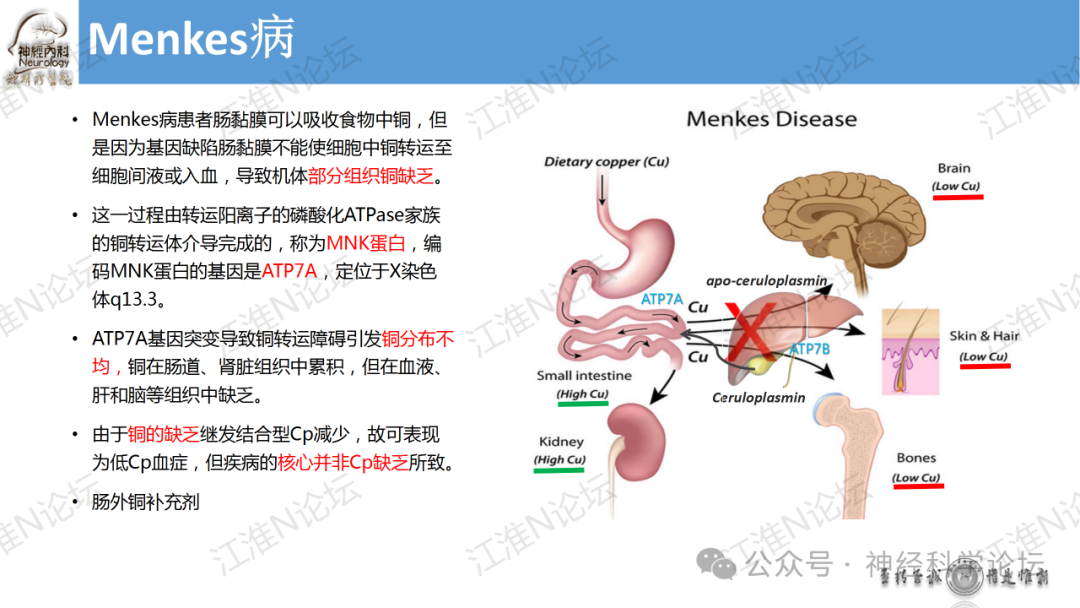
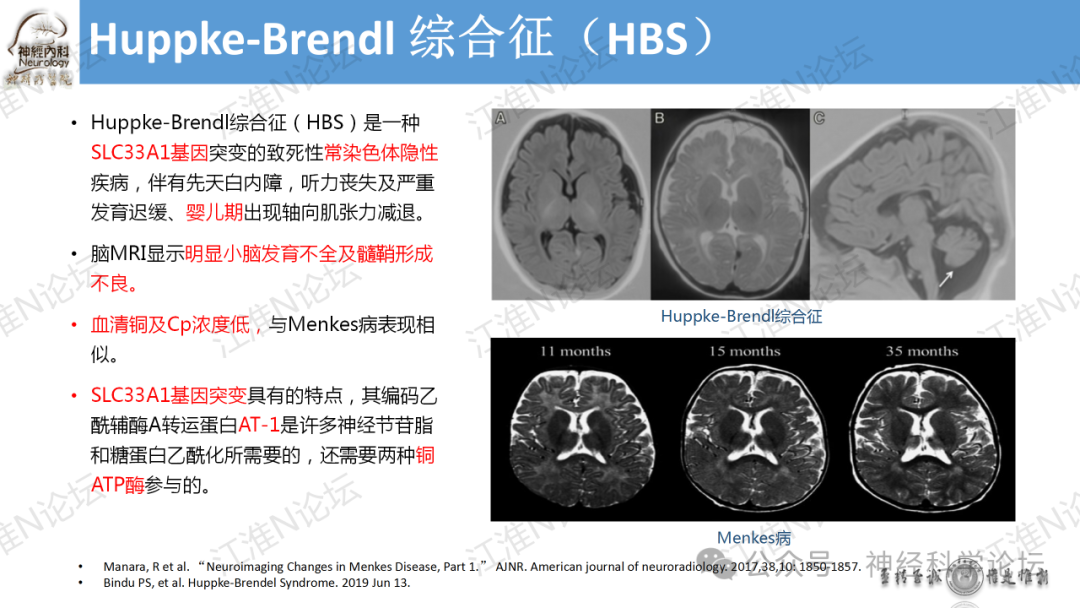
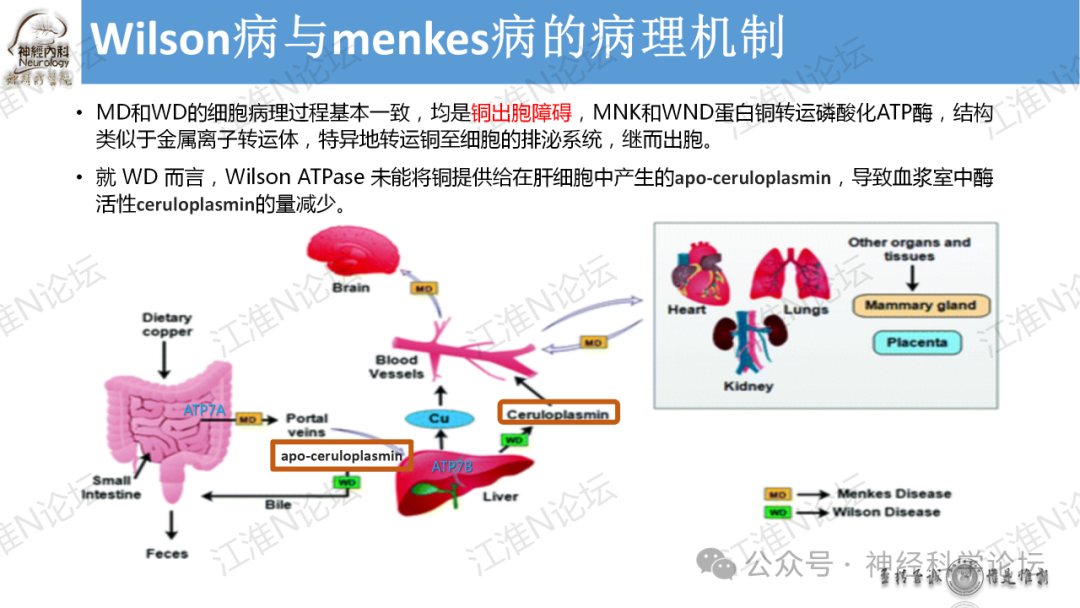
Menkes病(Menkes disease,MD)是一种罕见的先天性铜代谢异常疾病,遗传方式为X连锁隐性遗传。Menkes病患者肠黏膜可以吸收食物中铜,但是因为基因缺陷肠黏膜不能使细胞中铜转运至细胞间液或入血,导致机体部分组织铜缺乏。这一过程由转运阳离子的磷酸化ATPase家族的铜转运体介导完成的,称为MNK蛋白,编码MNK蛋白的基因是ATP7A,定位于X染色体q13.3。
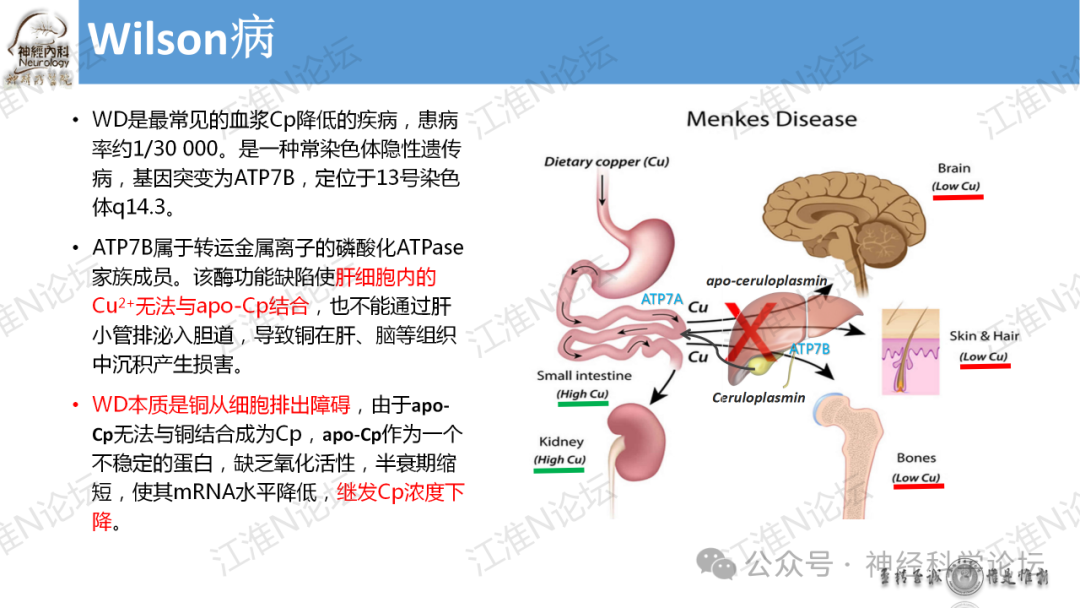
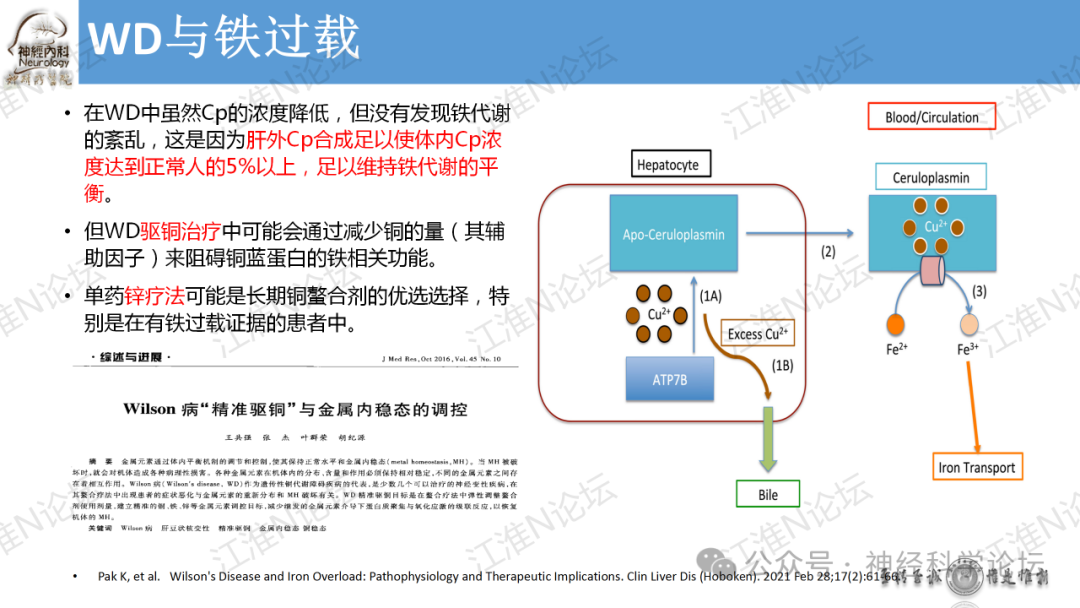
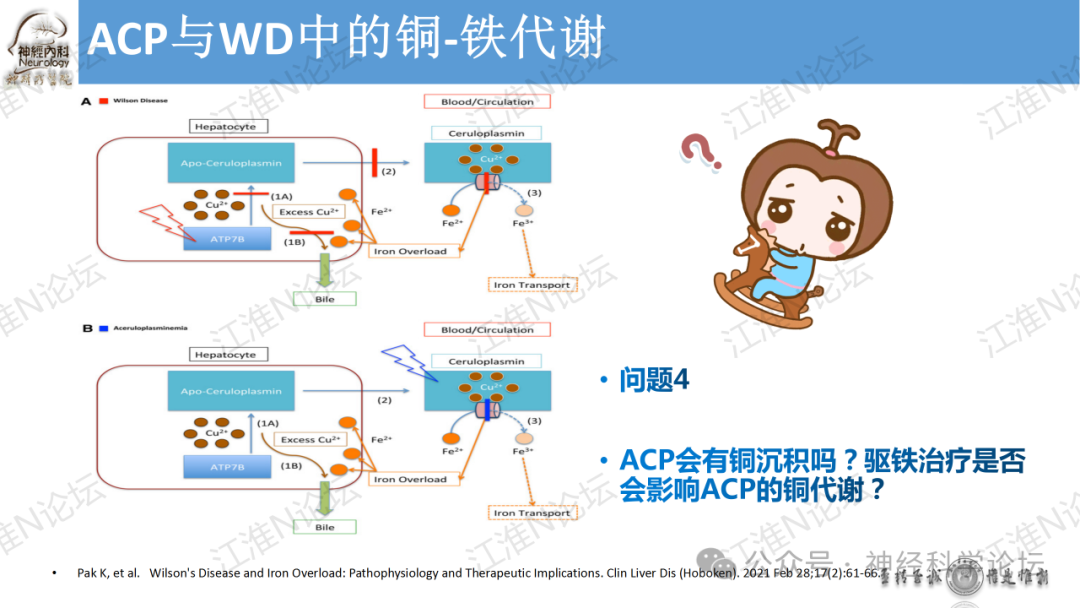
WD是最常见的血浆Cp降低的疾病,患病率约1/30 000。是一种常染色体隐性遗传病,基因突变为ATP7B,定位于13号染色体q14.3。ATP7B属于转运金属离子的磷酸化ATPase家族成员。该酶功能缺陷使肝细胞内的Cu2+无法与apo-Cp结合,也不能通过肝小管排泌入胆道,导致铜在肝、脑等组织中沉积产生损害。
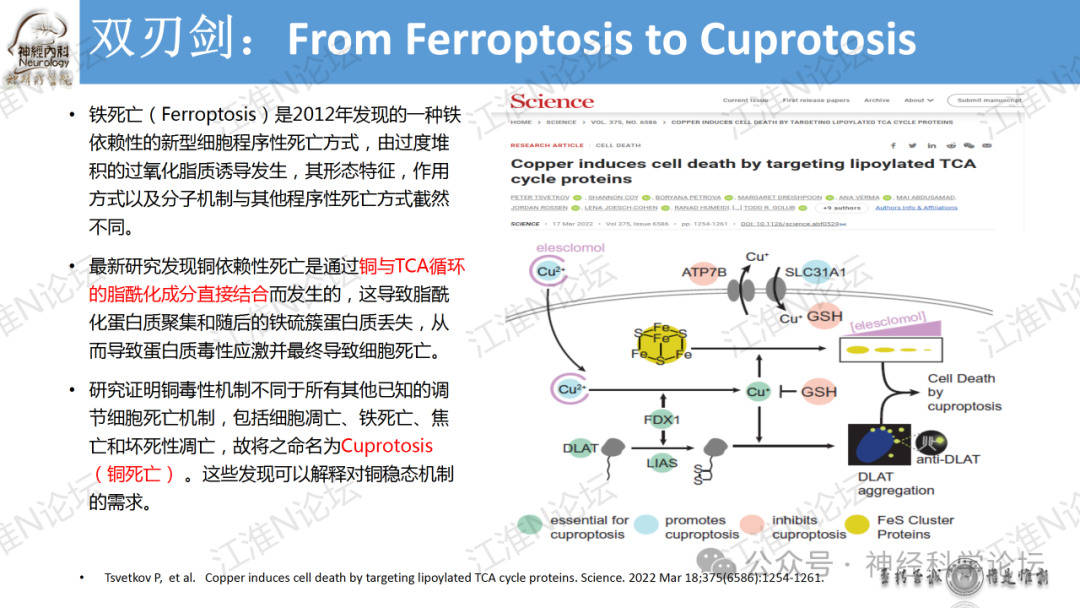
铁死亡(Ferroptosis)是2012年发现的一种铁依赖性的新型细胞程序性死亡方式,由过度堆积的过氧化脂质诱导发生,其形态特征,作用方式以及分子机制与其他程序性死亡方式截然不同。
最新研究发现铜依赖性死亡是通过铜与TCA循环的脂酰化成分直接结合而发生的,这导致脂酰化蛋白质聚集和随后的铁硫簇蛋白质丢失,从而导致蛋白质毒性应激并最终导致细胞死亡。 研究证明铜毒性机制不同于所有其他已知的调节细胞死亡机制,包括细胞凋亡、铁死亡、焦亡和坏死性凋亡,故将之命名为Cuprotosis(铜死亡) 。这些发现可以解释对铜稳态机制的需求。





本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#Wilson病# #Menkes病# #铜代谢#
61