Hepatology:对乙酰胺基酚的肝毒性机制被揭示
2022-03-26 网络 网络
对乙酰氨基酚(Paracetamol),别称泰诺林(Tylenol)、必理通(Panadol)、百服宁(Bufferin),本品是非那西丁的体内代谢产物,通过抑制下丘脑体温调节中枢前列腺素合成酶,减少
对乙酰氨基酚(Paracetamol),别称泰诺林(Tylenol)、必理通(Panadol)、百服宁(Bufferin),本品是非那西丁的体内代谢产物,通过抑制下丘脑体温调节中枢前列腺素合成酶,减少前列腺素PGE1、缓激肽和组胺等的合成和释放。PGE1主要作用于神经中枢,它的减少将导致中枢体温调定点下降,体表温度感受器感觉相对较热,进而通过神经调节引起外周血管扩张、出汗而达到解热的作用,其抑制中枢神经系统前列腺素合成的作用与阿司匹林相似,但抗炎作用较弱。对血小板及凝血机制无影响。
2017年10月27日,世界卫生组织国际癌症研究机构公布的致癌物清单初步整理参考,对乙酰氨基酚在3类致癌物(致癌性不明确,可能性比较低)清单中。
有人把对乙酰氨基酚比喻成一个火药桶,就是因为它的肝毒性。临床观察发现,长期、大剂量以及联合用药,常可诱发对乙酰氨基酚的严重不良反应,尤以肝坏死最为严重。
以前认为,对乙酰氨基酚的肝毒性源于药物代谢过程中出现的问题,在生物转化过程中,它会产生一种代谢物质,即N-乙酰对苯醌亚胺(NAPQI),其毒性较 大,需要与体内的还原性谷胱甘肽等保护因子结合才能降低毒性。如果服用对乙酰氨基酚剂量过大,或谷胱甘肽等保护因子减少时,致使这一毒性较大的中间代谢产 物与其他重要的大分子结合,就会出现肝损害。但是,最新一项研究给出全新的机制。

2022年3月21日,武汉大学宋质银及孟庆涛共同通讯在Hepatology(IF=17)在线发表题为“Loss of Sam50 in hepatocytes induces cardiolipin-dependent mitochondrial membrane remodeling to trigger mtDNA release and liver injury”的研究论文,该研究展示了 Sam50 与 MICOS 和 ATAD3 相互作用形成 Sam50-MICOS-ATAD3-mtDNA 轴,从而维持 mtDNA 的稳定性。Sam50 的丢失导致 mtDNA 聚集。此外,Sam50 与 Mic60 合作结合心磷脂,维持线粒体膜的完整性。Sam50 耗竭导致心磷脂外化,从而导致线粒体外膜和内膜(包括嵴膜)重塑,触发 Bax 线粒体募集、mtDNA 聚集和释放。
对乙酰氨基酚(APAP,一种有效的解热镇痛药)引起的 Sam50 减少,会诱导 mtDNA 释放,从而导致 cGAS-STING 通路的激活和小鼠的肝脏炎症。此外,Sam50 的外源性表达显著减弱了 APAP 诱导的肝毒性。如果Sam50 肝脏特异性敲除也会有类似的效应。
线粒体是高度动态的双膜细胞器,含有线粒体 DNA (mtDNA),它编码线粒体呼吸链复合物的关键亚基,对 ATP 的产生至关重要。Sam50(或 Samm50)是线粒体外膜中 β 桶蛋白组装所必需的分选和组装机器 (SAM) 的关键组成部分,可调节线粒体形态和嵴结构。此外,Sam50 与 MICOS 复合物结合形成超复合物 BIM,它连接线粒体外膜和内膜。有趣的是,Sam50 消耗会诱导 PINK1-Parkin 依赖性线粒体自噬,但会导致 mtDNA 聚集,从而保护 mtDNA 不被线粒体自噬移除。此外,Sam50 基因的多态性与非酒精性脂肪肝的发生和进展显著相关。然而,Sam50在调节mtDNA中的作用以及Sam50与人类疾病之间的关系仍不清楚。
与核 DNA 不同,mtDNA 缺乏保护性组蛋白,并且特别容易受到线粒体损伤因子(如 ROS)的攻击。受损或受压的 mtDNA 可以从线粒体释放到细胞质中。最近,许多研究报告了 mtDNA 释放的机制。在细胞凋亡过程中,Bax 与 Bak 寡聚化,在线粒体外膜中形成极大的大孔,从而介导 mtDNA 的释放 。此外,受氧化应激的线粒体通过线粒体外膜中的 VDAC 寡聚体形成的孔释放短 mtDNA 片段。此外,位于线粒体内膜的线粒体通透性转换孔可能参与 mtDNA 的释放。然而,mtDNA 释放的信号传导和潜在机制仍然知之甚少。
为了应对各种感染,环状 GMP-AMP (cGAMP) 合酶 (cGAS) 充当细胞溶质 DNA 感应器,通过产生第二信使 cGAMP 来激活先天免疫反应,从而激活接头 STING。激活的 STING 然后募集并激活 TBK1,它使 STING 和 IRF3 磷酸化以诱导 I 型 IFN 和许多其他促炎细胞因子的产生。此外,TBK1 的活性受激酶激活环内 Ser-172 磷酸化的调节。除了来自微生物感染的病原体衍生 DNA 之外,cGAS-STING 途径也可以被细胞溶质 mtDNA 激活。此外,胞质 mtDNA 激活 TLR9 或炎症小体介导的信号通路。
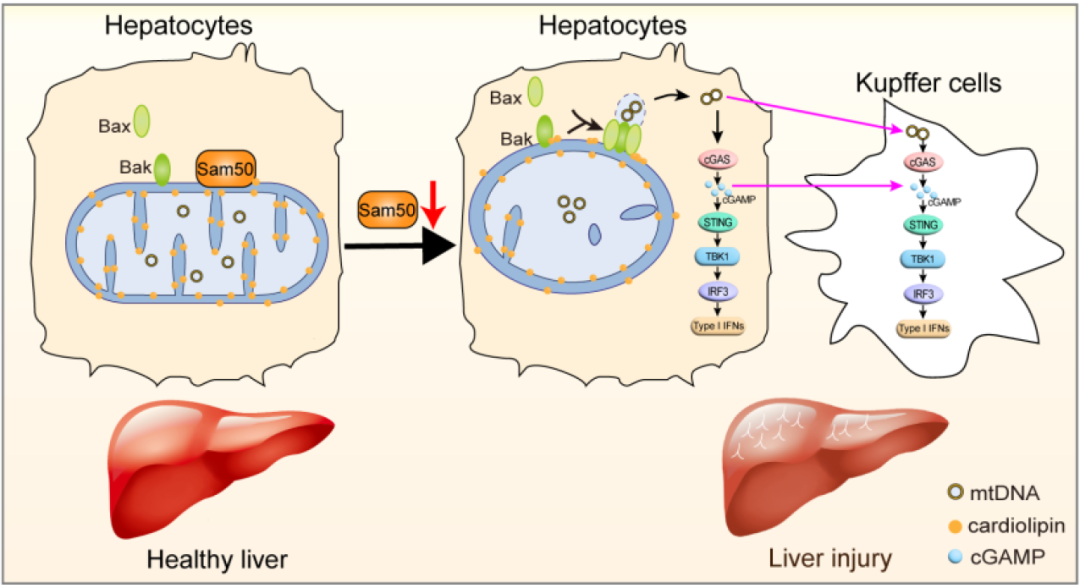
文章模式图(图源自Hepatology )
心磷脂是一种独特的二聚体磷脂,主要存在于线粒体内膜内以维持线粒体膜的完整性。心磷脂是几个关键的线粒体过程所必需的,包括线粒体呼吸、线粒体动力学、细胞凋亡和线粒体自噬。心磷脂直接与线粒体呼吸链复合物相互作用并稳定它以调节 ATP 的产生。心磷脂作为启动细胞凋亡和线粒体自噬的关键信号平台,它暴露于线粒体外膜(心磷脂外化)以响应许多线粒体应激,外化心磷脂促进 Bax 或 Bak 寡聚化以诱导大膜孔并与 LC3 结合触发线粒体自噬 。
对乙酰氨基酚 (APAP) 是一种有效的解热镇痛药,但过量服用 APAP 是最常见的药物中毒,也是全球急性肝功能衰竭的主要原因。APAP 过量导致过量的中间代谢物 N-乙酰基-对苯醌亚胺 (NAPQI) 排出谷胱甘肽 (GSH),导致细胞蛋白中的巯基共价结合,尤其是线粒体蛋白,导致线粒体氧化应激、功能障碍,最终导致肝细胞坏死和肝损伤。虽然越来越多的证据表明线粒体在 APAP 诱导的肝损伤中的作用,但 APAP 导致 DAMP(损伤相关分子模式)释放和随后的肝损伤的机制仍不清楚。
在这里,该研究表明 Sam50 消耗或 APAP 处理导致 mtDNA 通过 Bax/Bak 线粒体孔释放,然后激活 cGAS-STING 信号通路和小鼠肝脏炎症。重要的是,该研究发现 Sam50 耗竭诱导心磷脂外化,导致 Bax 线粒体募集,并最终触发 mtDNA 释放。因此,该研究结果表明,Sam50 耗竭诱导的心磷脂外化是 mtDNA 释放的新信号。
参考消息:
Chen L, Dong J, Liao S, Wang S, Wu Z, Zuo M, Liu B, Yan C, Chen Y, He H, Meng Q, Song Z. Loss of Sam50 in hepatocytes induces cardiolipin-dependent mitochondrial membrane remodeling to trigger mtDNA release and liver injury. Hepatology . 2022 Mar 21. doi: 10.1002/hep.32471 https://aasldpubs.onlinelibrary.wiley.com/doi/10.1002/hep.32471
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#EPA#
41
#肝毒性#
39