Metabolism 朱毅教授/付成来研究员合作发现调控胆固醇逆转运关键蛋白apoA-I的内源性分子
2025-01-03 论道心血管 论道心血管 发表于陕西省
研究发现IP6K1的产物5PP-InsP5是调控apoA-I表达的内源性分子,5PP-InsP5通过促进UBE4A介导的apoA-I泛素化导致apoA-I降解。
动脉粥样硬化心血管疾病是导致人类死亡的主要原因,其典型表现是血管壁脂质沉积。载脂蛋白A-I (apoA-I)是高密度脂蛋白(HDL)的结构蛋白和功能蛋白,通过介导胆固醇逆向转运减少胆固醇在血管壁的沉积,从而抑制动脉粥样硬化的发生发展。因此,上调血液循环中apoA-I的表达水平是防治动脉粥样硬化的有效手段。
六磷酸肌醇激酶1 (Inositol hexakisphosphate kinase 1, IP6K1)广泛表达于哺乳动物细胞,其产物七磷酸肌醇(5PP-InsP5)参与多种细胞生物学过程。IP6K1/5PP-InsP5的表达异常会引起糖尿病、神经发育障碍和癌症等疾病。然而,IP6K1和5PP-InsP5在代谢性心血管疾病中的作用尚不清楚。
2024年12月9日,天津医科大学朱毅教授与上海交通大学医学院附属新华医院付成来研究员合作在Metabolism-clinical and Experimental 杂志上在线发表了题为“Inhibiting IP6K1 confers atheroprotection by elevating circulating apolipoprotein A-I”的研究论文,发现IP6K1的产物5PP-InsP5是调控apoA-I表达的内源性分子,5PP-InsP5通过促进UBE4A介导的apoA-I泛素化导致apoA-I降解。干预IP6K1通过上调apoA-I来促进胆固醇逆转运从而减轻动脉粥样硬化,为动脉粥样硬化心血管疾病的防治提供了新的思路和潜在靶点。

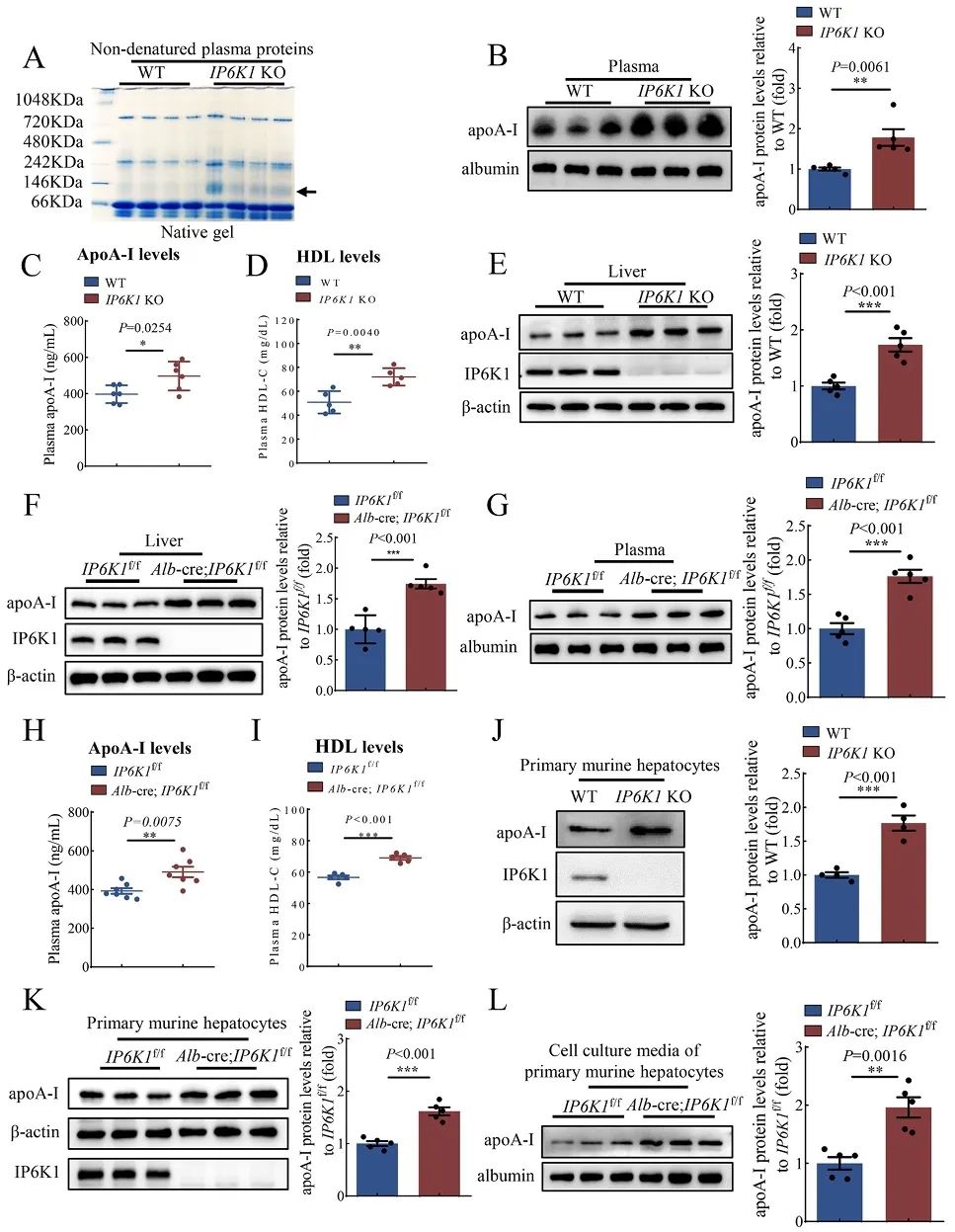
研究者通过比较IP6K1 KO和WT的小鼠血浆蛋白,意外发现敲除IP6K1会上调血浆中apoA-I的表达水平。ApoA-I主要来源于肝细胞,研究者通过构建肝细胞特异性IP6K1敲除小鼠验证了敲除IP6K1通过增加肝细胞表达apoA-I来上调血浆中apoA-I和HDL。
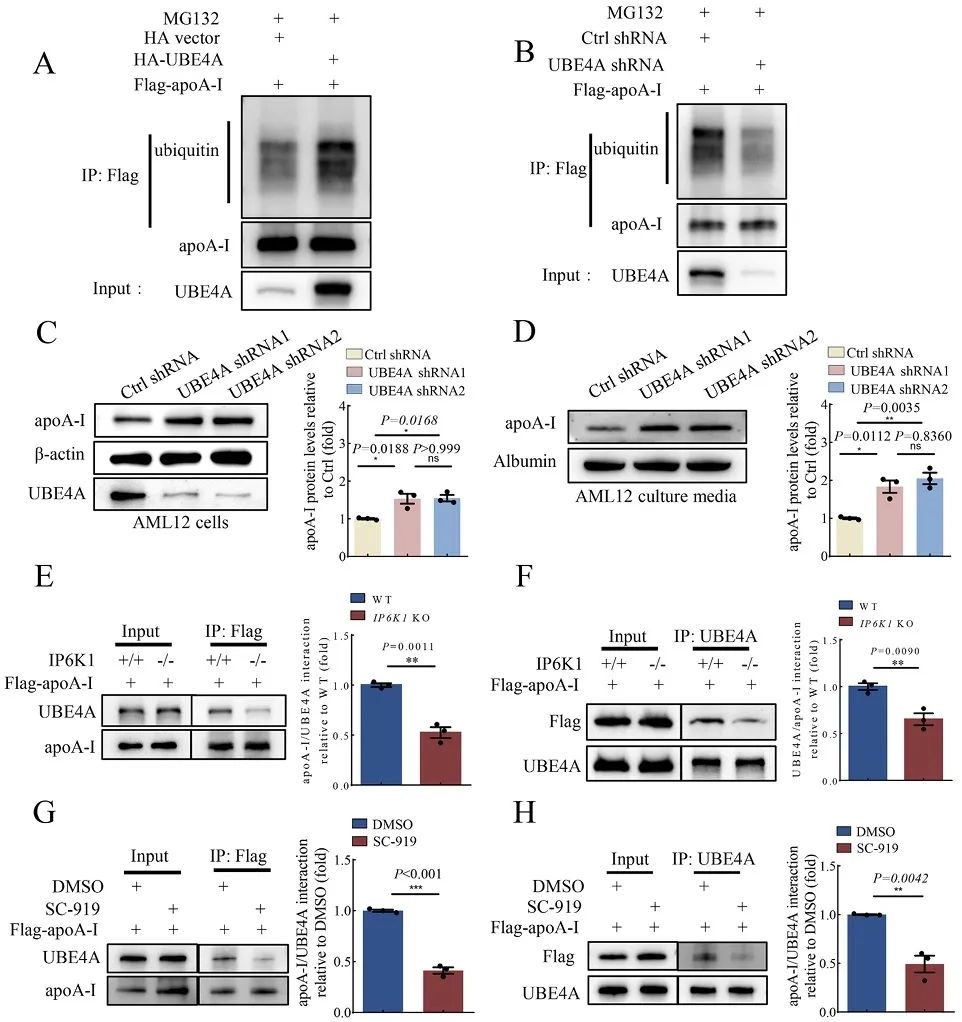
在分子机制方面,作者通过免疫沉淀和蛋白质谱等方法寻找与IP6K1和apoA-I结合蛋白,发现两者同时结合E3泛素连接酶UBE4A。研究者通过一系列分子生物学和化学生物学实验阐明IP6K1通过其产物5PP-InsP5促进UBE4A与apoA-I的相互作用,导致apoA-I泛素化修饰最终被降解。
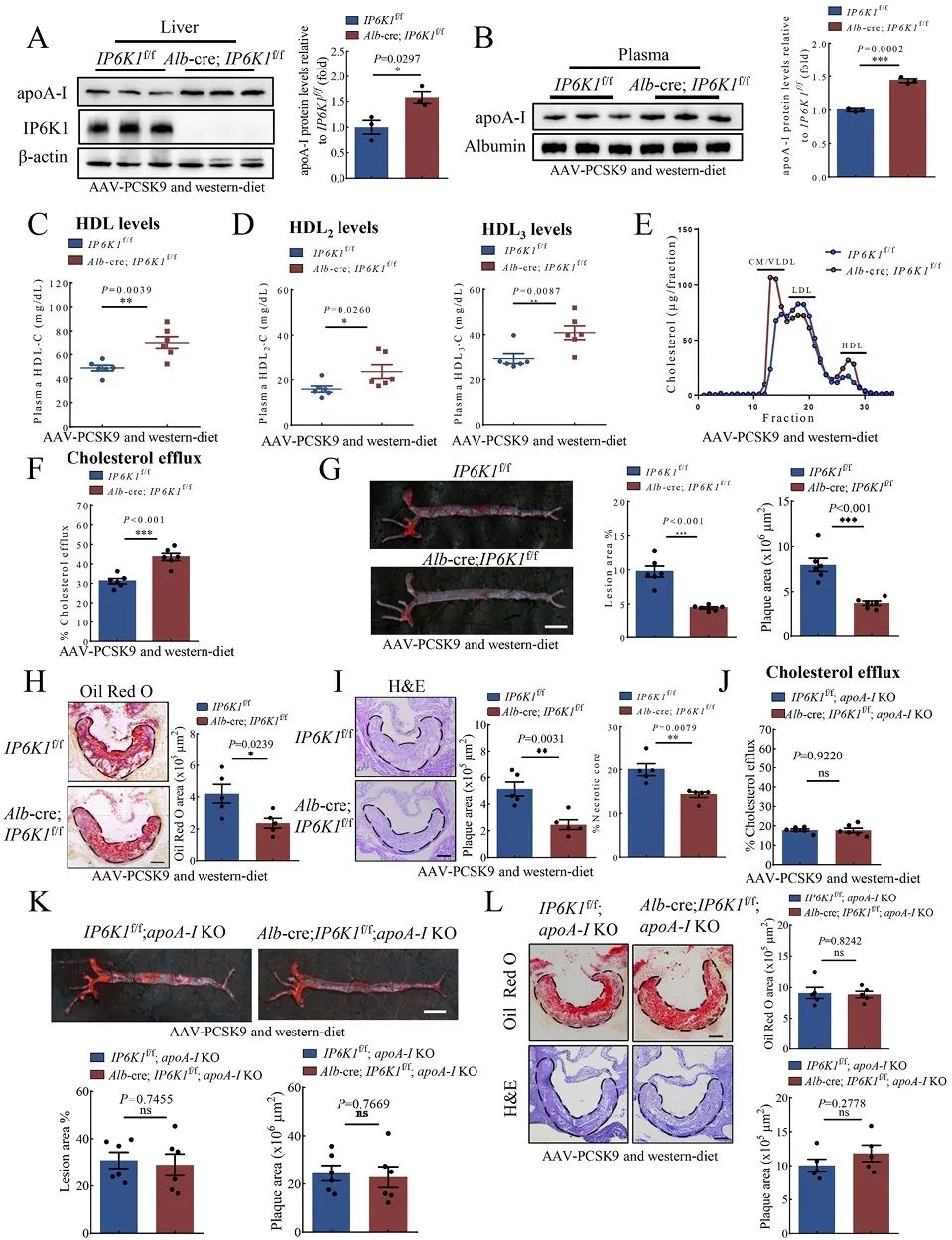
在病理生理意义方面,研究者发现特异性敲除肝细胞表达的IP6K1促进apoA-I介导的胆固醇外流,抑制实验动物动脉粥样硬化的进展。
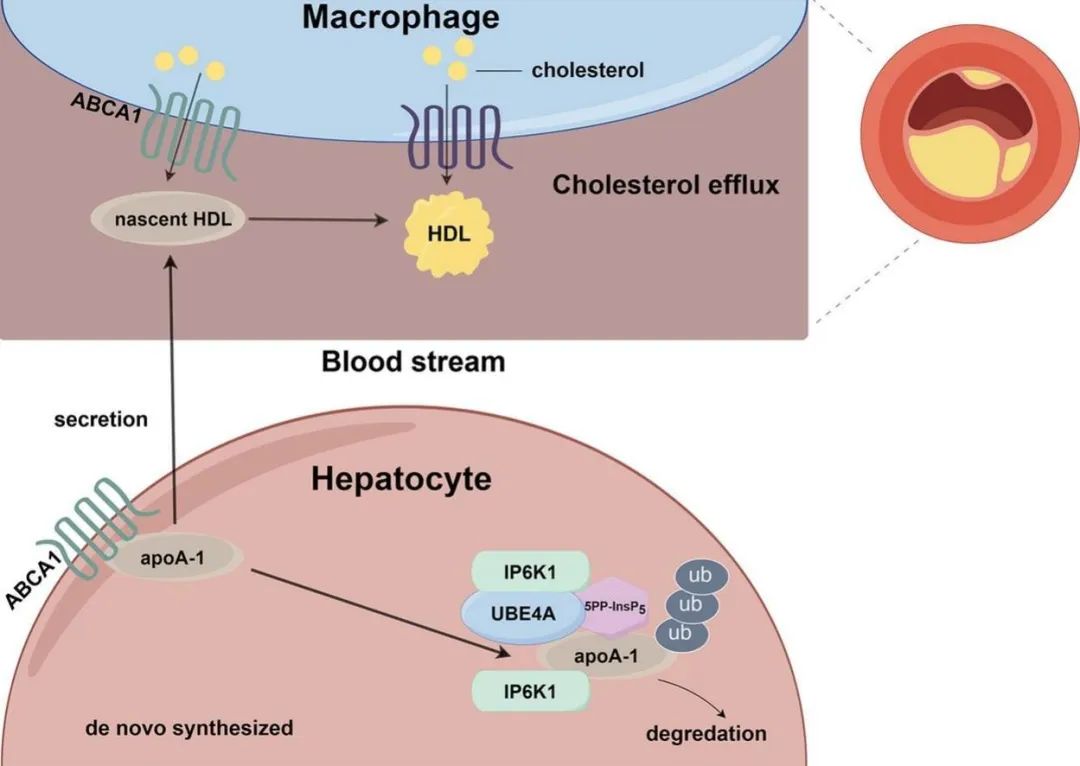
综上所述,该课题研究发现IP6K1的产物5PP-InsP5是调控apoA-Ⅰ表达的内源性分子,干预IP6K1通过上调血浆apoA-Ⅰ促进胆固醇逆转运来发挥抗动脉粥样硬化的保护作用。
天津医科大学医学生理学专业刘小琪博士为本文第一作者,天津医科大学朱毅教授和上海交通大学医学院附属新华医院付成来研究员为本文通讯作者。课题得到了牛津大学Barry Potter教授、德国莱布尼茨研究所的Dorothea Fiedler教授、天津医科大学张栩研究员和天津医科大学第二医院刘彤教授的大力支持。本研究得到国家自然科学基金项目的资助。
原文链接:
https://www.metabolismjournal.com/article/S0026-0495(24)00326-3/fulltext
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#动脉粥样硬化心血管疾病# #胆固醇逆转运#
7