唐本忠院士团队最新AM:基于聚集诱导NIR-II发射发光剂的间质光纤介导的原位乳腺癌多模态光疗
2024-07-30 BioMed科技 BioMed科技 发表于上海
首次提出了一种将具有聚集诱导发射特性的多功能分子tBuTTBD与改性光纤相结合的综合策略,以实现原位乳腺肿瘤的全面肿瘤诊断和“由内而外”发光。
基于单分子的一体化光疗法被认为是癌症治疗的一种方便方法,其疗效依赖于通过多模式成像的精确病灶定位,再加上光疗的有效应用。为了充分发挥光疗法的潜力,光疗法药物和光传递方法的进步至关重要。
在此,深圳大学唐本忠教授、Zhourui Xu、王东教授、许改霞教授和张志军助理教授等人首次提出了一种将具有聚集诱导发射特性的多功能分子tBuTTBD与改性光纤相结合的综合策略,以实现原位乳腺肿瘤的全面肿瘤诊断和“由内而外”发光。由于强烈的供体-受体相互作用、高度扭曲的构象、丰富的分子转子和聚集时松散的分子间堆积,tBuTTBD可以在激光照射下同步进行第二近红外(NIR-II)荧光发射、光热和光动力产生,有助于实现三模式NIR-II荧光光声(PA)-光热成像引导的光疗。这项工作不仅丰富了NIR-II光疗法制剂的种类,而且为探索用于实际癌症治疗的综合光疗法方案提供了有价值的见解。相关工作以“Interstitial Optical Fiber-Mediated Multimodal Phototheranostics Based on an Aggregation-Induced NIR-II Emission Luminogen for Orthotopic Breast Cancer Treatment”为题发表在Advanced Materials。

【文章要点】
在这篇文章中,作者首次利用NIR-II发射光致抗肿瘤剂和光传递方法,实现了更加先进的光驱动肿瘤治疗。通过增强高度扭曲的共轭骨架上的电子供体-受体(D-A)相互作用,作者成功合成了一种多模式光致变色AIEgen试剂,即tBuTTBD,其特征是NIR吸收、NIR-II发射、显著的PA信号、显著的光热效应,以及在808 nm激光照射下高效的活性氧(ROS)产生能力。具体而言,作者使用叔丁基取代的二苯胺作为强电子供体,空间位阻的己基噻吩作为π桥和额外的电子供体,高度吸电子的苯并噻二唑作为强受体,从而构建化合物tBuTTBD(图1)。其中,叔丁基取代二苯胺的螺旋桨状构象、叔丁基的空间位阻以及己基噻吩的长烷基链共同扭曲了整个分子骨架,这不仅通过显著减少分子间π-π堆积和与水的相互作用来抑制聚集过程中的荧光淬灭,而且为分子内运动提供了足够的空间,有利于非辐射热能衰减。此外,凭借较强的D-A效应tBuTTBD有望减少电子带隙并改善ISC工艺,从而产生红移吸收和发射波长以及良好的光动力势能。
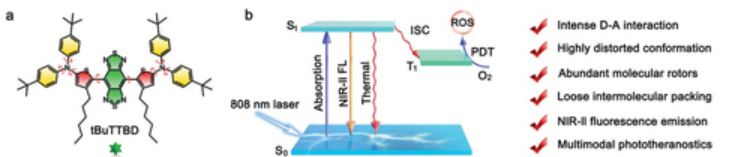
图1 tBuTTBD
在两亲性聚合物和iRGD表面改性的促进下,tBuTTBD纳米粒子iRGD(NPs-iRGD)在静脉注射后可以有效地靶向肿瘤部位,并实现光触发的NIR-II FLI-PAI-PTI三模态成像。不仅如此,作者还使用改良的光纤(图2)启动原位乳腺肿瘤的原位光疗。该光纤是通过将平端光纤与空芯光纤端拼接而制成的,可以最大限度地提高激光在肿瘤内的扩散。这种方法显示出比通过准直器进行激光照射的传统光疗方法更优越的治疗效果。这项工作提出了光疗剂和光传递方法的奇妙组合,不仅可以绕过身体上的生物光屏障,还可以释放光疗法的全部潜力,为临床应用的进步铺平道路。
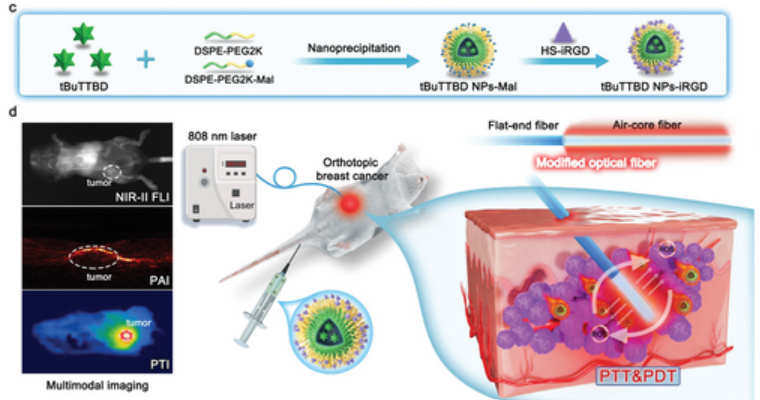
图2 NPs-iRGD的制备以及光纤介导的光疗
原文链接:
https://onlinelibrary.wiley.com/doi/10.1002/adma.202406474
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#乳腺肿瘤# #NIR-II#
73