Adv Sci:中国科学院乐颖影团队研究揭示甘油激酶驱动非酒精性脂肪肝肝脏从头脂肪生成和甘油三酯合成
2024-10-21 iNature iNature 发表于上海
该研究在饮食诱导和遗传小鼠的NAFL模型中发现肝脏Gk表达增加,并且与肝脏SREBP-1c表达和TG水平呈正相关。胆固醇和脂肪酸刺激肝细胞中的GK表达。
甘油激酶(GK)通过催化甘油代谢参与甘油三酯(TG)合成。GK是否会导致非酒精性脂肪肝(NAFL)尚不清楚。
2024年10月17日,中国科学院上海营养与健康研究所乐颖影通讯在Advanced Science 在线发表题为“Glycerol Kinase Drives Hepatic de novo Lipogenesis and Triglyceride Synthesis in Nonalcoholic Fatty Liver by Activating SREBP-1c Transcription, Upregulating DGAT1/2 Expression, and Promoting Glycerol Metabolism”的研究论文。该研究在饮食诱导和遗传小鼠的NAFL模型中发现肝脏Gk表达增加,并且与肝脏SREBP-1c表达和TG水平呈正相关。胆固醇和脂肪酸刺激肝细胞中的GK表达。
在HFD诱导的NAFL小鼠中,肝脏Gk的敲低会降低SREBP-1c及其靶脂肪生成基因以及DGAT1/2的表达,增加血清甘油水平,降低血清TG水平,并减弱肝脏TG积累。在小鼠或培养的肝细胞中过度表达GK会产生相反的结果。机制研究表明,GK通过与SREBP-1c基因启动子结合直接刺激SREBP-1c转录,并通过与SREBP-1c蛋白结合间接刺激SREBP-1c转录,从而增加脂肪生成基因表达和从头脂肪生成。对截短GK和突变GK的研究表明,GK诱导SREBP-1c转录独立于其酶活性。GK通过催化甘油代谢而不是调节SREBP-1c转录来促进生理条件下的脂质稳态。总之,这些结果表明,增加肝脏GK通过刺激SREBP-1c转录和DGAT1/2表达并催化甘油代谢来促进NAFL中的从头脂肪生成和TG合成。

非酒精性脂肪性肝病(NAFLD)目前是全球慢性肝病的主要原因。它包括一系列疾病,包括非酒精性脂肪肝(NAFL)和非酒精性脂肪性肝炎(NASH)。NAFL会增加代谢紊乱的风险,例如2型糖尿病和高脂血症,并可能发展为NASH、肝硬化或肝细胞癌。肝细胞中脂质(主要是甘油三酯(TG))的过量积累是NAFL的标志。使用稳定同位素示踪策略的研究表明,NAFL患者肝脏中积累的TG主要来自从头脂肪生成。
固醇调节元件结合蛋白1c(SREBP-1c)是一种主要转录因子,可调节肝细胞中从头脂肪生成和TG合成中涉及的酶的表达,包括用于脂肪酸合成和去饱和的ATP柠檬酸裂解酶(ACLY)、乙酰辅酶A羧化酶(ACC)、脂肪酸合酶(FASN)、长链延长酶(ELOVL6)和硬脂酰辅酶A去饱和酶1(SCD1);以及用于TG合成的甘油-3-磷酸酰基转移酶(GPAT)。SREBP-1c蛋白作为位于内质网膜上的无活性前体合成。蛋白水解切割后,前体的N端结构域转移到细胞核中,通过结合启动子中的固醇调节元件(SRE)来激活其自身基因和其他靶基因。在人类NAFLD患者和NAFL动物模型的肝脏中,SREBP-1c及其靶脂肪生成基因的表达增加。敲减或抑制SREBP-1c或其靶脂肪生成酶,如ACC、SCD1、ELOVL6和GPAT,可减少NAFLD动物和患者的肝脏脂质沉积,表明SREBP-1c对肝脏脂肪变性的关键作用。在生理条件下,SREBP-1c的基因转录调控、前体蛋白加工和蛋白质翻译后修饰已被广泛研究。然而,SREBP-1c在NAFL中的转录调控尚不完全清楚。
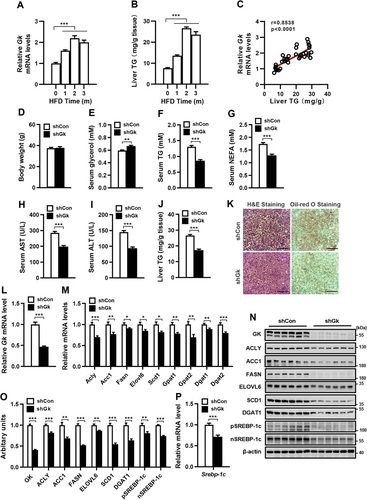
肝脏中Gk的敲低会减弱HFD诱导的肝脏Srebp-1c和脂肪生成基因表达、肝脏脂肪变性和高脂血症。(图源自Advanced Science )
甘油激酶(GK)属于FGGY激酶家族,它催化ATP将甘油磷酸化为甘油-3-磷酸(G3P)。G3P是TG合成的底物,参与糖异生。作者之前的研究表明,GK不仅通过将甘油转化为G3P来调节肝脏糖异生,而且还通过AKT-FOXO1通路上调磷酸烯醇丙酮酸羧激酶和葡萄糖-6-磷酸酶的表达。GK在生理条件下的葡萄糖稳态中起重要作用,并导致糖尿病小鼠的高血糖。作者发现,在HFD诱导的高血糖和高脂血症的肥胖小鼠中,肝脏GK上调。然而,尚不清楚GK是否有助于生理条件下的脂质稳态和NAFL的发展。
在本研究中,作者发现GK在饮食诱导和遗传性NAFL小鼠模型的肝脏中上调,并在肝脂肪变性的发展中起着至关重要的作用。作者确定胆固醇和脂肪酸是肝细胞中GK表达的调节剂。通过腺病毒介导的功能获得和丧失研究,作者证明GK不仅通过催化甘油代谢参与肝脏TG合成,而且还通过上调SREBP-1c转录促进肝脏从头脂肪生成和TG合成。作者进一步探索了GK调节SREBP-1c转录的分子机制。此外,作者研究了肝脏GK对生理条件下脂质稳态的贡献。
参考消息:
https://onlinelibrary.wiley.com/doi/10.1002/advs.202401311
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#非酒精性脂肪肝# #甘油激酶#
14