TRANSPLANTATION:美国DCD肝脏下降后的移植候选结果
2023-10-07 Bob Wang MedSci原创 发表于陕西省
DCD报价的接受与肝脏移植候选人的大量长期生存益处有关,即使是老年DCD捐赠者或有合并症的捐赠者。应鼓励增加DCD肝脏的恢复和利用。
拯救生命的肝移植的需求远远超过了可用性,美国候补名单上有超过12 767名患者,但在2019年只进行了8896名肝移植(LT)。188%的肝脏候补名单注册者在等待报价时每年因死亡或健康状况恶化而被移除。为了缓解器官供需之间的差距,已经大力利用现有肝脏,包括边缘移植。临床实践中常见的边缘移植来自心脏死亡(DCD)后的捐赠:一个遭受毁灭性和不可逆转的脑损伤的捐赠者,可能接近死亡,但不符合正式的脑死亡标准。
DCD肝脏是一个严重利用不足的资源,仅从2009年所有已故捐赠者LT的5%略微增加到2019年的8.5%。尽管对器官有严重需求,但近29.9%的DCD肝脏被丢弃,是脑死亡(DBD)肝脏(7.1%)后捐赠的4倍。
DCD肝脏的高丢弃率可能是由于这些边缘器官的生存益处的不确定性。与DBD不同,从DCD中恢复的肝脏在采购过程中有一定程度的缺氧:具体来说,从停止心肺支持到启动器官冷却之间的时间。由于这种长时间的温暖缺血时间,DCD肝脏的接受者与DBD肝脏接受者相比,移植失败率更高;与DBD肝脏接受者相比,LT相关成本增加。
然而,这些比较假设候选人可以在同时提供DCD和DBD肝脏之间进行选择,这不能准确反映现实世界的情况。相反,患者及其提供者今天面临着接受“高风险”DCD移植的决定,或者拒绝该提议并等待可能永远不会到来的“更好的”DBD提议。更好地理解与接受或拒绝DCD肝脏相关的权衡,将更好地为LT候选人和提供者经常面临的实时决策提供信息。这些权衡可能取决于DCD捐赠者的特征;额外的捐赠者风险因素,如高龄、肥胖或合并症,可能会影响接受与拒绝DCD提议的相对益处。
2023年9月20日发表在TRANSPLANTATION的文章,研究人员使用美国国家注册数据:(1)描述拒绝DCD报价的候选人的自然历史,(2)将DCD报价接受者的生存率与DCD报价拒绝者的生存率进行比较,(3)将具有其他风险因素的DCD肝脏接受者与类似报价的拒绝者之间的生存率进行比较,以及(4)如果DCD肝脏的使用率与DBD肝脏相同,则确定每年执行的额外LT数量。

使用2009年-2020年的美国注册数据,我们确定了代表DCD肝脏报价被接受的1564名候选人(“接受者”)和代表DCD肝脏报价被拒绝的16 981名候选人(“接受者”)。我们使用竞争风险框架来描述下降者的结果,并使用Cox回归来估计接受DCD肝脏的生存益处(调整后危险比[95%置信区间])。
研究结果显示,在DCD报价下降的10年内,50.9%的候选人在移植任何类型的同种异体移植之前死亡或被从候补名单中删除。与10年后的下降者相比,DCD接受者的死亡率较低(35.4%对48.9%,P < 0.001)。在对候选协变量进行调整后,DCD报价的接受与死亡率降低46%有关(0.54 [0.49-0.61])。与DCD下降者相比,老年人(年龄≥50岁)、肥胖(体重指数≥30)、高血压、非局部、糖尿病和风险增加的DCD肝脏的受体分别分别有44%(0.56 [0.42–0.73])、40%(0.60 [0.49–0.74])、48%(0.52 [0.41–0.66])、46%(0.54 [0.45–0.65])、32%(0.68 [0.43–1.05])和45%(0.55 [0.42–0.72])的死亡率风险。
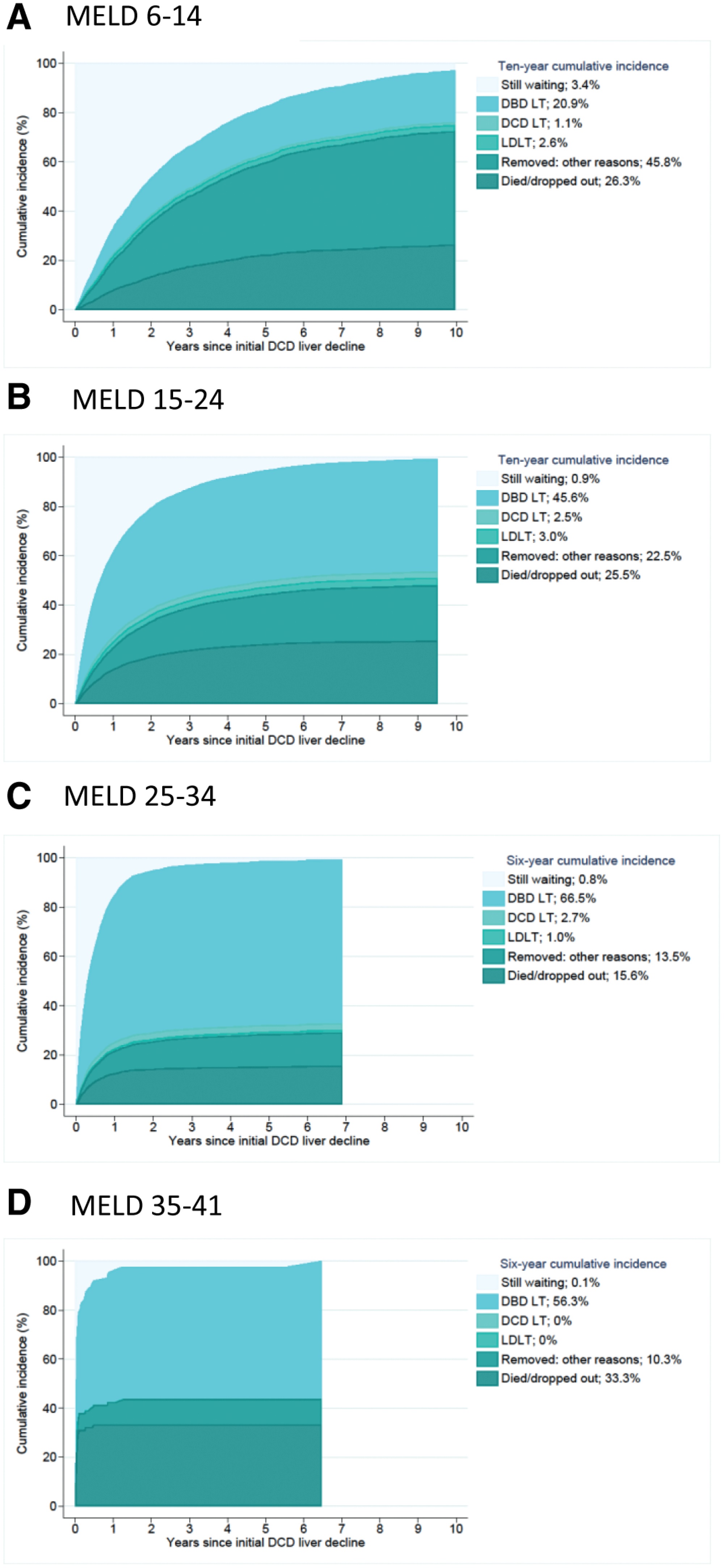
图1:每个MELD层中DCD肝脏衰退的结果
综上所述,我们已经表明,与下降和等待下一个最佳报价相比,接受DCD肝脏与大量和长期的生存益处有关。患者和提供者应仔细权衡拒绝DCD移植的后果,因为一半的候补候选人在下降后死亡或被除名10年。对DCD肝脏的评估是复杂的,特别是在存在额外的供体和受体合并症的情况下,这可能会增加这些边缘器官生存益处的不确定性。
然而,我们的发现提供了可以指导未来临床决策的证据:与拒绝相同DCD的候选人相比,老年、肥胖、高血压、共享或IRD肝脏的接受者死亡率仍然明显降低。鉴于持续的器官短缺、DCD肝脏的高丢弃率以及机器灌注的商业增长,我们的结果支持更多地使用DCD移植物来扩大捐赠者库并降低候补名单死亡率。
原文出处
Ishaque, Tanveen ScM, MBBS1; Eagleson, Mackenzie A. MD2; Bowring, Mary G. MPH2; Motter, Jennifer D. MHS1; Yu, Sile MD, MPH2; Luo, Xun MD, MPH3; Kernodle, Amber B. MD, PhD, MPH2; Gentry, Sommer PhD1,4,5; Garonzik-Wang, Jacqueline M. MD, PhD6; King, Elizabeth A. MD, PhD2; Segev, Dorry L. MD, PhD1,4,5; Massie, Allan B. PhD, MHS1,4. Transplant Candidate Outcomes After Declining a DCD Liver in the United States. Transplantation ():10.1097/TP.0000000000004777, September 20, 2023. | DOI: 10.1097/TP.0000000000004777
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言