恒定自然杀伤T(iNKT)细胞疗法增加胰腺癌肝转移小鼠的浸润性免疫细胞含量,促进T细胞毒性,缓解病程发展
2024-07-22 《基因启明》公众号 《基因启明》公众号 发表于上海
胰腺癌是一种致死率极高的恶性肿瘤,已成为危害公共健康的突出问题,5年生存率不足10%。胰腺癌诊治困难主要在于其起病隐匿、转移迅速。
亮点
1. 注射α-GalCer能够激活体内iNKT细胞,进而阻止胰腺癌肝转移(PCLM)进程,减少肿瘤细胞数量,增加浸润性免疫细胞含量。
2. 活化的iNKT细胞能够促进T细胞细胞毒性,诱导靶肿瘤细胞裂解,促进干扰素(IFN-γ)生成大幅增加,肿瘤小鼠的免疫力得到了极大提升。
3. α-GalCer激活iNKT细胞可使CD4 T细胞偏向细胞毒性Th1型、CD8 T细胞偏向细胞毒性型发展,这有助于缓解PCLM。
胰腺癌是一种致死率极高的恶性肿瘤,已成为危害公共健康的突出问题,5年生存率不足10%。胰腺癌诊治困难主要在于其起病隐匿、转移迅速。肝脏是胰腺癌最易发的转移器官,50%以上的胰腺癌患者在确诊时已有肝转移。
恒定自然杀伤T(iNKT)细胞是CD1d靶向性T淋巴细胞,可利用恒定的T细胞受体 (TCR)识别特定的脂质抗原,其细胞因子的产生有助于确定免疫反应的进程。由于强大的抗肿瘤功效,iNKT细胞目前已成为免疫治疗的热点。
近期,一项题为scRNA-Seq and imaging mass cytometry analyses unveil iNKT cells-mediated anti-tumor immunity in pancreatic cancer liver metastasis的研究表明,用α-半乳糖基神经酰胺(α-GalCer)激活iNKT细胞,可显著增加免疫细胞浸润并抑制胰腺癌肝转移的发展。具体表现为治疗后小鼠体内iNKT/NK细胞的细胞毒性活性增强、CD4 T细胞偏向细胞毒性Th1型、CD8 T细胞偏向细胞毒性型,研究结果揭示了iNKT细胞在胰腺癌肝转移中的保护功能,为临床药物研发提供了理论依据。

首先,研究人员构建了胰腺癌肝转移(PCLM)小鼠模型,以确定iNKT细胞在疾病中的作用。
在体内情况下,iNKT细胞能够识别和响应糖脂抗原α-半乳糖基神经酰胺的刺激,发挥细胞毒性。果不其然,注射α-GalCer阻止了小鼠PCLM进程,并且显著减少了肿瘤细胞数量,增加了浸润性免疫细胞含量,这表明,激活的iNKT细胞可将免疫细胞募集到肝脏,并对胰腺肿瘤向肝脏转移产生抑制作用。
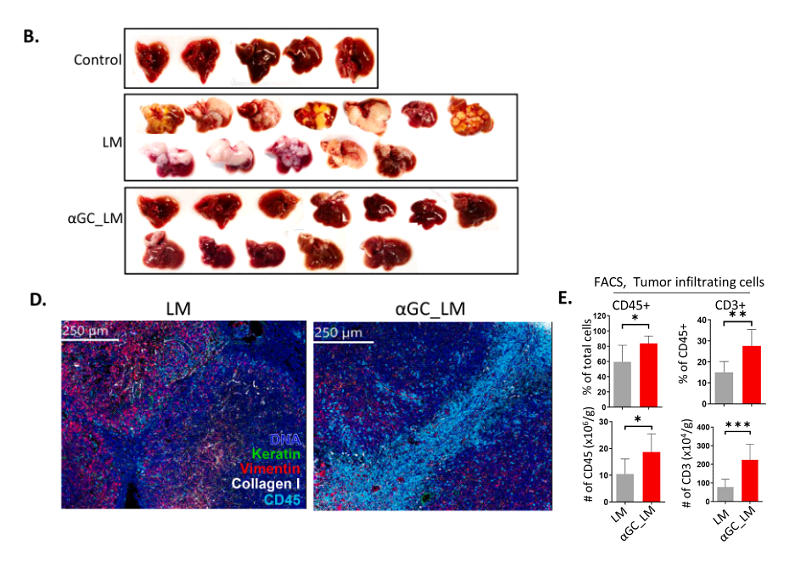
α-GalCer治疗抑制胰腺肿瘤肝转移
随后,为了评估α-GalCer激活的iNKT细胞对PCLM的免疫学效应,研究人员对小鼠单细胞悬液中的免疫细胞进行了RNA测序。令人鼓舞的是,他们发现α-GalCer治疗下,肝转移小鼠中T淋巴细胞含量明显高于未治疗组小鼠,巨噬细胞、中性粒细胞等含量也有所增加,说明了活化的iNKT细胞会增强T淋巴细胞的肝脏浸润,并明显改善PCLM的免疫特征。
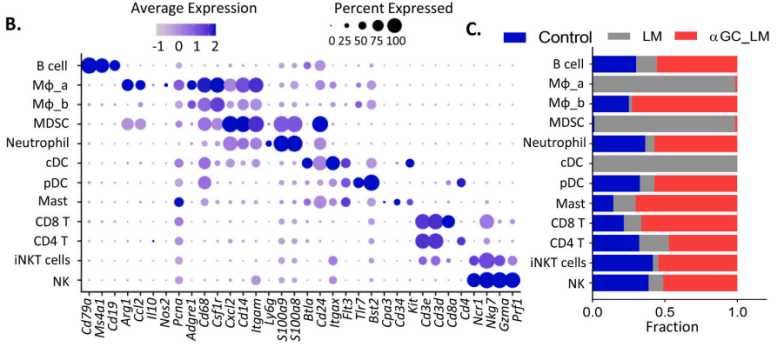
基于单细胞基因表达的CD45细胞亚型分析
那么,α-GalCer防止肝转移的潜在机制是什么呢?
为回答这一疑问,研究人员对活化的iNKT细胞进行了深入分析。他们发现,α-GalCer激活iNKT细胞可导致Gzma、Gzmb和Prf1的转录上调,从而促进T细胞细胞毒性,诱导靶肿瘤细胞裂解;小鼠肝脏中浸润的NK细胞的频率和数量也明显升高;此外,α-GalCer处理下肝转移小鼠的干扰素(IFN-γ)生成大幅增加,肿瘤小鼠的免疫力得到了极大提升。
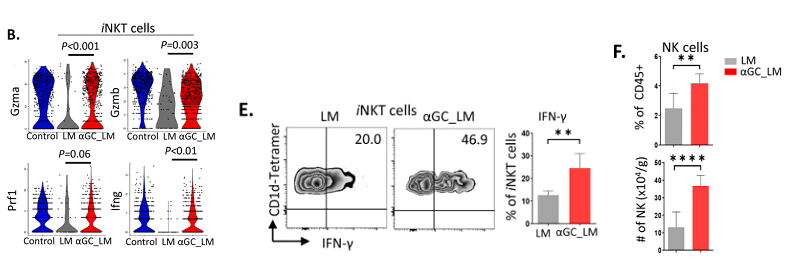
iNKT细胞中基因表达谱、NK细胞含量和IFN-γ含量
此外,已有研究表明,iNKT细胞产生的IFN-γ可以激活其他淋巴细胞(如CD4 T和 CD8 T细胞),于是,研究人员进一步测试了PCLM小鼠中适应性T淋巴细胞的活性是否会随着α-GalCer的治疗而改善。
令人惊喜的是,接受α-GalCer治疗的小鼠CD4 T细胞大量扩增。用流式细胞术具体分析,发现α-GalCer处理的肝转移小鼠肿瘤浸润的CD4 T细胞表现出Th1表型, IFN-γ和TNF-α的产生得以增多;且具有细胞毒性特性的CD4细胞在PCLM微环境中得以富集。总而言之,用α-GalCer激活iNKT细胞可使CD4 T 细胞偏向细胞毒性Th1特征发展,这有助于缓解并治愈PCLM。
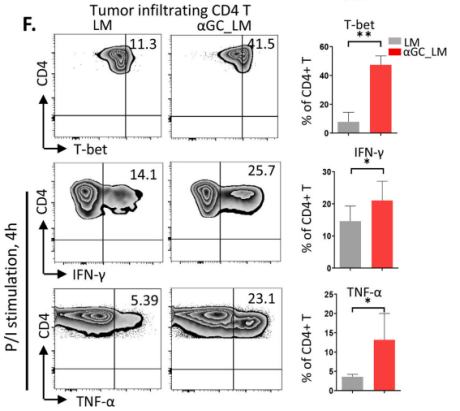
小鼠肿瘤浸润CD4 T细胞中IFN-γ和TNF-α含量
众所周知,细胞毒性CD8 T细胞在肿瘤的分布与癌症预后密切相关。巧合的是,研究人员观察到α-GalCer处理的肝转移小鼠中CD8 T细胞浸润较高,在肝脏中富集明显;对其基因进行富集分析,发现多集中于NK细胞信号传导、Th1通路和细胞毒性T淋巴细胞信号传导通路中。同时,肝脏中浸润的CD8 T细胞也显示出了极大的细胞毒性活性,其TNF-α生成显著增加。
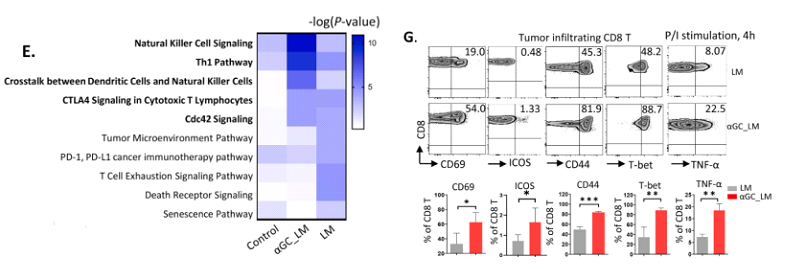
α-GalCer激活iNKT细胞促进CD8 T细胞细胞毒性
讲到这里,这项研究基本进入了尾声。研究者最后检测了巨噬细胞在PCLM中的含量,发现α-GalCer处理显著降低了肿瘤相关巨噬细胞(TAM)的标记物水平。据了解,TAMs是一种免疫抑制性免疫细胞,有助于肿瘤的进展并抑制NK和iNKT细胞的免疫活性。因此,α-GalCer激活iNKT细胞活性后,能够有效缓解TAMs的潜在免疫抑制作用,改善胰腺癌肝转移的发展进程。
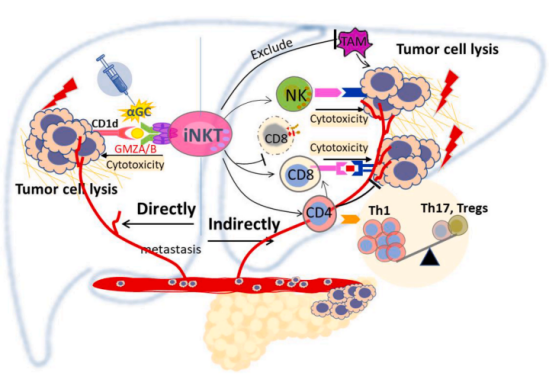
iNKT细胞介导的PCLM保护模型
总而言之,这项研究为胰腺癌的治疗提供了新思路,随着iNKT细胞疗法的日渐发展与完善,相信在不久的将来,癌症必不再无药可治。
来源:
微信公众号: 基因启明
参考文献
Yi Q, Wang J, Liu T, Yao Y, Loveless I, Subedi K, Toor J, Adrianto I, Xiao H, Chen B, Crawford HC, Fang D, Zhou L, Mi QS. scRNA-Seq and imaging mass cytometry analyses unveil iNKT cells-mediated anti-tumor immunity in pancreatic cancer liver metastasis. Cancer Lett. 2023 May 1;561:216149. doi: 10.1016/j.canlet.2023.216149. Epub 2023 Mar 27. PMID: 36990268.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#胰腺癌#
65