【BJH】大样本研究证实放疗桥接在CAR-T治疗LBCL中可行
2024-05-07 聊聊血液 聊聊血液 发表于上海
英国学者提出一个大型、多中心全国性复发/难治性(r/r LBCL)患者队列,患者在CD19 CAR-T之前用RT进行桥接,该研究旨在评估RT作为单一模式和联合模式桥接治疗在不同患者亚组中的适用性。
CAR-T的放疗桥接
CD19 CAR-T细胞疗法的桥接治疗(BT)包括皮质类固醇、免疫化疗、放疗(RT)或联合治疗(CMT;即全身治疗联合放疗),其目标是在制备期间控制疾病,可影响长期结局,但最佳BT方案仍未知,也没有相关指南或建议。其中放射治疗(RT)与CAR-T具有协同作用,但由于后勤挑战和缺乏标准化方案,尚未广泛用作桥接治疗,也未确定 RT 的最佳剂量、分割、时间和体积。
英国学者提出一个大型、多中心全国性复发/难治性(r/r LBCL)患者队列,患者在CD19 CAR-T之前用RT进行桥接,该研究旨在评估RT作为单一模式和联合模式桥接治疗在不同患者亚组中的适用性。该研究也是首个评估ITT人群中RT桥接的多中心研究,结果近日发表于《British Journal of Haematology》。

研究结果
作者分析了2018年12月至2022年10月期间12家英国中心,≥2线治疗失败并计划接受axicabtagene ciloleucel(axi-cel)或tisagenlecleucel(tisa-cel)治疗的连续r/r LBCL患者763例,其中717例单采且有BT数据,因此纳入分析,具体BT方案由医生决定。
在717例可获得数据的患者中,169例(23.6%)接受RT桥接,其中129例(18.0%)接受单一模式,40例(5.6%)接受CMT。随着时间的推移,RT的使用率从18.3%(2018-2019)增加到27.1% (2021-2022;P=0.024)。
接受RT桥接(单一模式或CMT)的患者中位年龄为60岁。其中69.2%为原发LBCL, 4.7%为原发性纵隔B细胞淋巴瘤,20.7%为转化性滤泡性淋巴瘤,3.6%为其他低级别淋巴瘤,1.8%为Richter转化。RT桥接患者的疾病特征见表1。65.7%为晚期,36.9%为大包块,86.5%的LDH升高,41.7%的国际预后指数(IPI)≥3,15.2%为双/三打击。与接受全身治疗/CMT的患者相比,接受单一模式RT的患者中晚期(p<0.001和p=0.024)或≥2个结外部位(p=0.038和p=0.016)的比例更小(表1)。
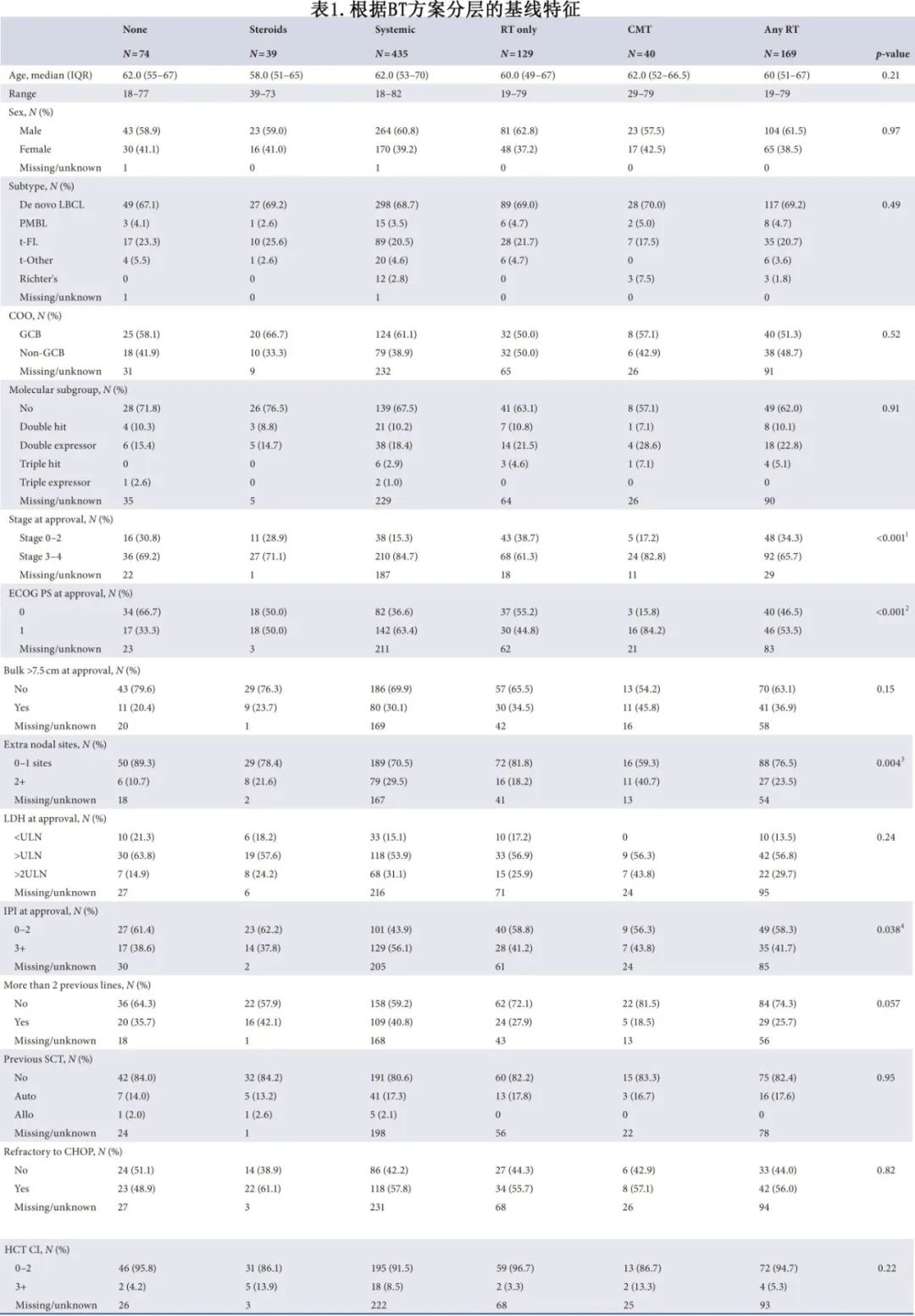
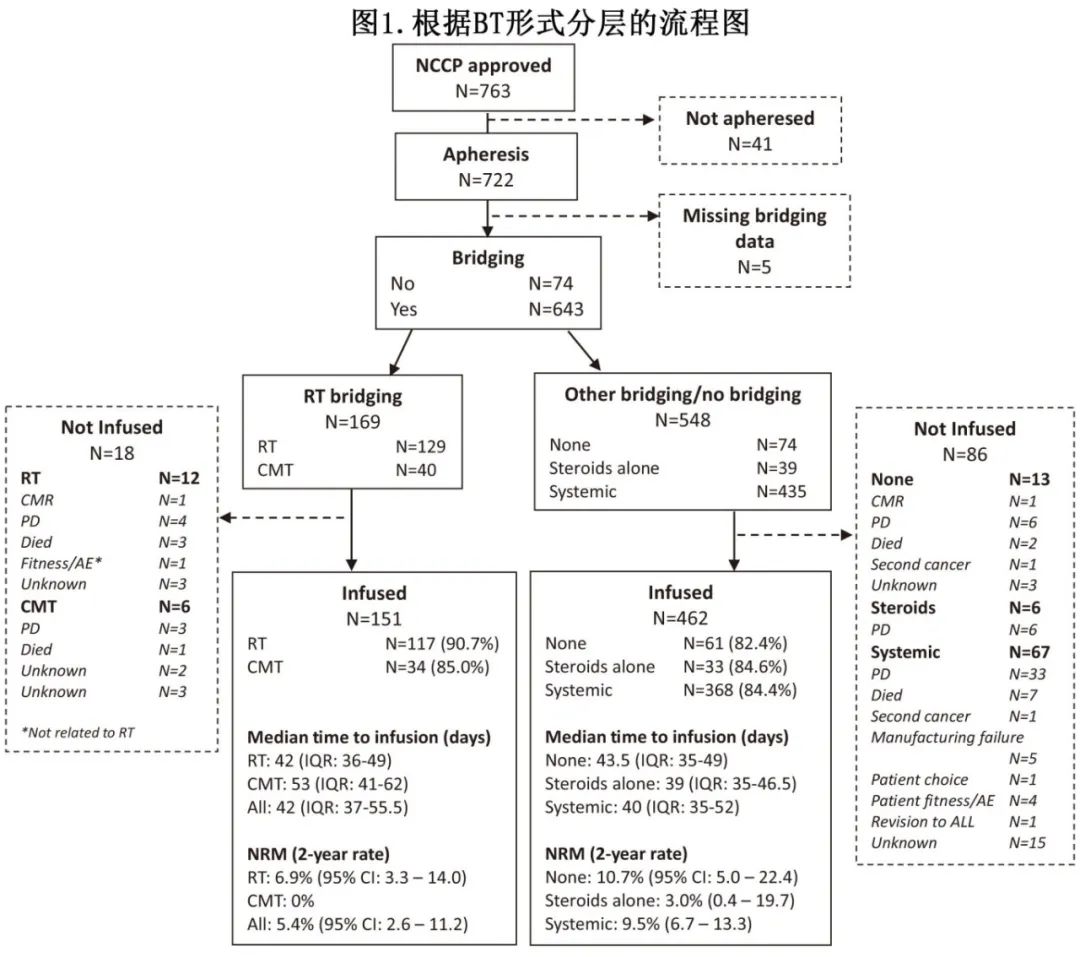
从白细胞单采到输注的中位时间为41天, 且各BT方案之间无显著差异(图1)。接受单一模式RT的患者中90.7%和CMT患者中85.0%接受输注(而其他BT组为82.4%-84.6%) (p=0.40;图1)。
部分患者可获得放疗技术、解剖位置和毒性的详细信息(表2)。使用的剂量为2-39 Gy(每部分2Gy的等效剂量(EQD2) =1.8-42.3 Gy)(中位剂量30 Gy),包括多剂量组合;67.8%的患者接受调强放疗(IMRT)。只有1例患者出现≥3级放射治疗毒性(腹部放射治疗后出现3级呕吐)。从最后一次放疗到开始清淋的中位时间为21天。
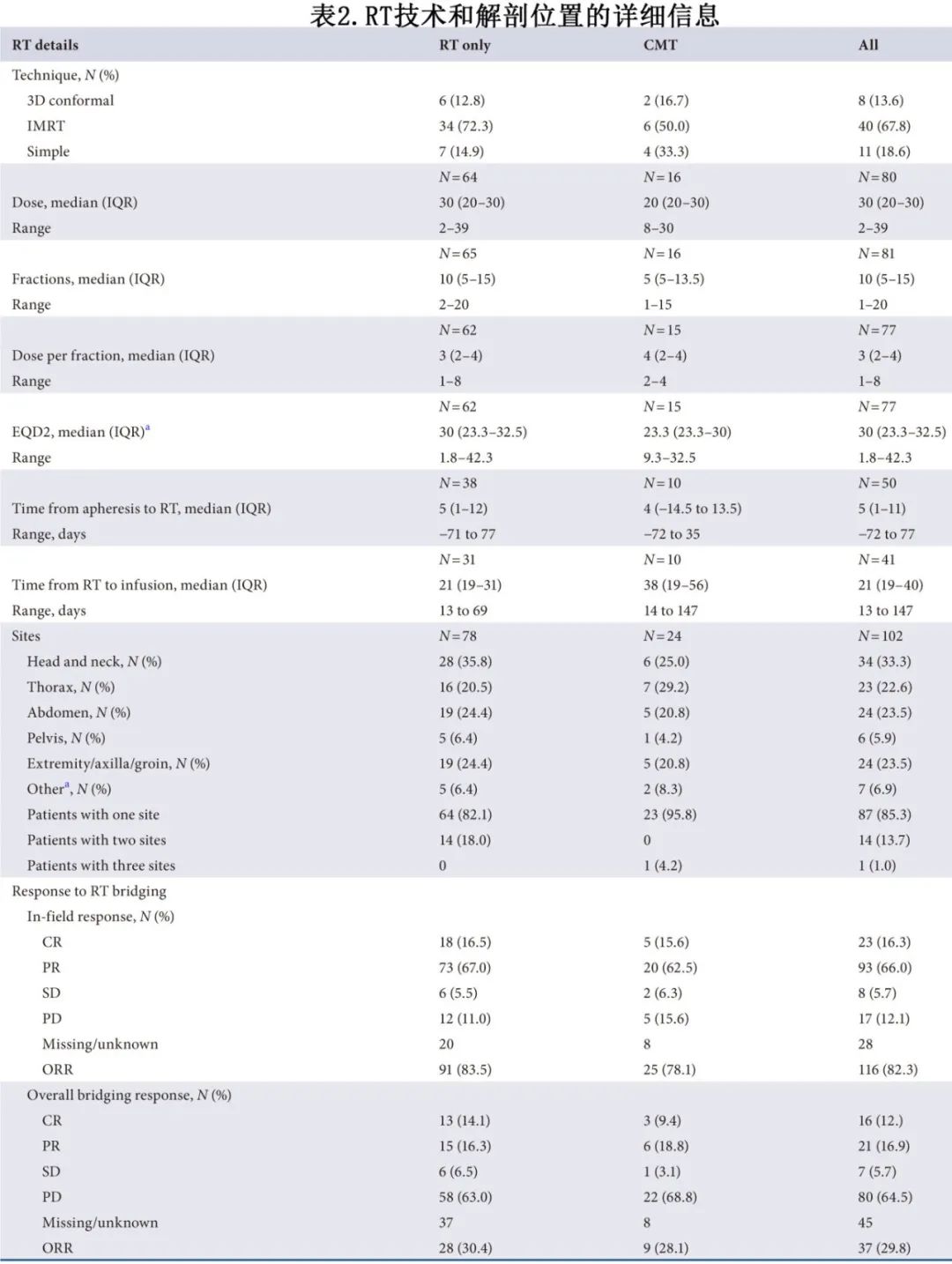
141例RT患者可通过输注前PET扫描评估桥接治疗(野内)的反应。值得注意的是,为了不延迟CAR-T输注,这些扫描通常在RT完成后早期进行,因此没有足够的时间来评估RT反应的全部程度。116例(82.3%)患者出现野内缓解(完全缓解[CR] 23例,部分缓解[PR] 93例),8例病情稳定(SD),17例疾病进展(PD)。野内缓解的116例患者中96例可获得总体疾病缓解的数据,其中58例(60.4%)分类为总体PD。
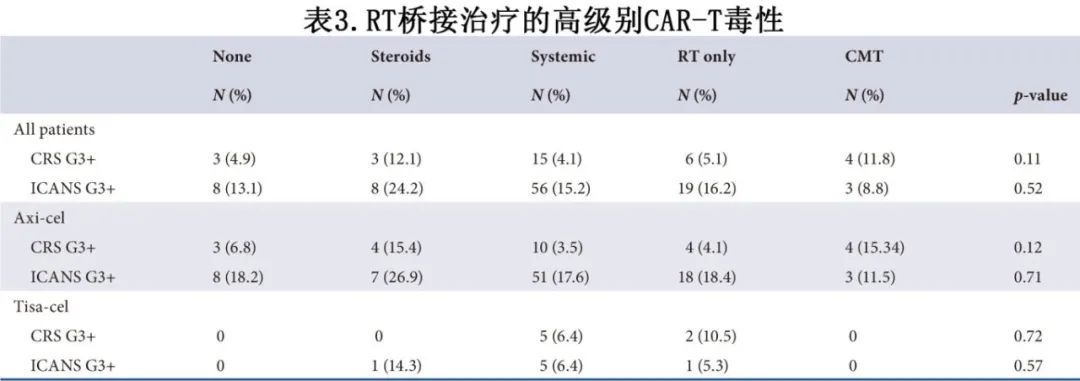
CAR相关免疫毒性,即≥3级细胞因子释放综合征(CRS)的发生率为5.2%,≥3级免疫效应细胞相关神经毒性综合征(ICANS)的发生率为15.3%,且各BT组无显著差异(表3)。
第1个月时,全身桥接患者的血小板减少发生率(56%)明显高于单纯RT桥接患者(32%;p=0.006)或CMT (10%;p=0.007),第3个月时仍较高但不显著(分别为22%、6%和20%)。第1和3个月时中性粒细胞减少的发生率无显著差异,NRM发生率也无显著差异(p=0.33;图1)。
CAR-T治疗后的最佳总体缓解率(ORR)/CR率:单一模式为82.1%/62.5%,CMT为81.8%/63.6%,高于单纯使用类固醇(63.6%/39.4%)和全身桥接(74.0%/55.9%),但仅单一模式RT与类固醇相比差异显著(p=0.032)。在RT桥接的患者中,无论总体或野内缓解率如何,CAR-T后缓解率和长期生存率均相似。
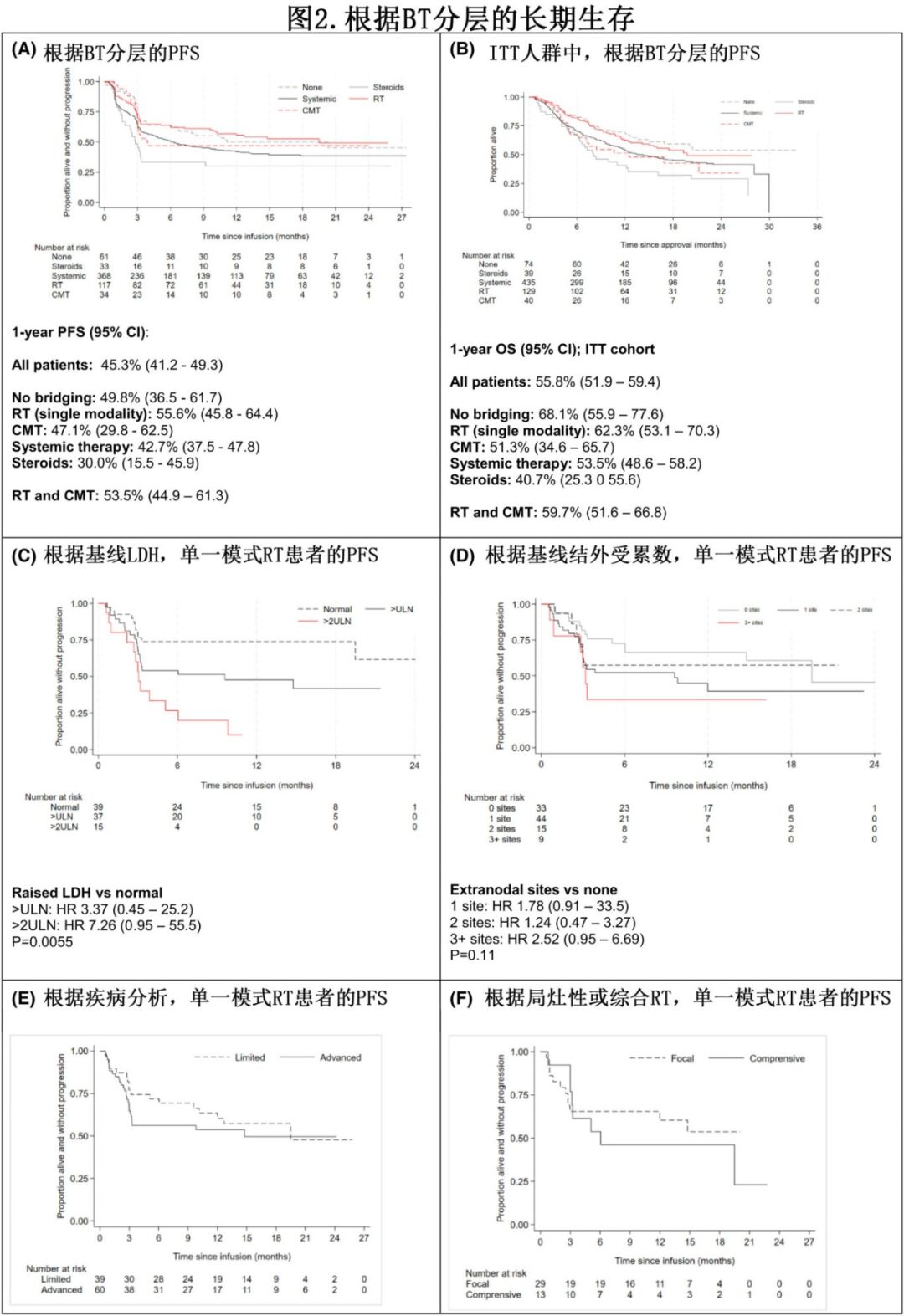
中位随访18.2个月,RT桥接患者的结局较好,包括单一模式1年PFS为56%,CMT为47%(图2A)。所有批准CAR - T治疗的患者的ITT 1年OS率分别为62%(单一模式)和51%(CMT)(图2B)。基线时高LDH和/或存在3+各结外部位与接受RT单一模式桥接治疗的患者预后较差相关 (图2C/D);由于数量太少,无法在RT桥接患者队列中单独进行多因素分析。单一模式RT桥接与局限期和晚期疾病的良好预后均相关(图2E)。对于局灶性放疗与包括所有活动性疾病的综合放疗,未观察到结局差异,但患者数量过少(图2F)。
总结
作者分析了在英国12个中心获批使用3 线axicabtagene ciloleucel或tisagenlecuucel的LBCL患者的RT桥接情况。在763例批准的患者中,722例进行单采,717例有桥接治疗数据。169/717例(24%)接受RT桥接治疗,其中129例为单一模式,40例为联合模式 (CMT)。在169例患者中,65.7%为晚期,36.9%为大包块,86.5%为LDH升高,41.7%为国际预后指数(IPI)≥3,15.2%为双/三打击。RT桥接随着时间的推移而增加。静脉-静脉时间和输注速率在各桥接方式之间没有差异。RT桥接的患者结局良好,单一模式的1年PFS为56%,CMT为47%(而全身桥接的1年PFS为43%)。
该研究是在CD19 CAR-T之前接受RT桥接治疗的最大LBCL患者队列,也是首个评估ITT人群中RT桥接的多中心研究。表明即使在晚期和高危疾病中,RT桥接也可以安全有效地使用,实现CAR-T输注,脱落率低(11%),效果良好。此外,脱落率在考虑选择CAR-T还是新型现成药物时尤为重要。该研究可为在淋巴瘤CAR-T桥接治疗中开发高精度、个性化的RT方案提供基础。
参考文献
Kuhnl A, Roddie C, Kirkwood AA, Chaganti S, Norman J, Lugthart S, et al. Outcome and feasibility of radiotherapy bridging in large B-cell lymphoma patients receiving CD19 CAR T in the UK. Br J Haematol. 2024;00:1–12.https://doi.org/10.1111/bjh.19453
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#CAR-T# #LBCL#
7