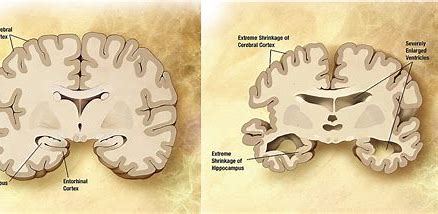
Eisai和Biogen正在向FDA申请aducanumab治疗阿尔茨海默症的优先审查
制药公司百健(Biogen)和卫材(Eisai)近日表示,FDA接受了aducanumab治疗阿尔茨海默症优先审查的申请,并将目标行动日期定为明年3月7日。
MedSci原创 - 阿尔茨海默症,早老性痴呆,aducanumab - 2020-08-09
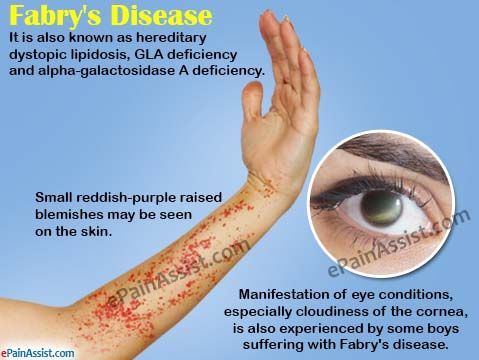
FDA延长法布雷病治疗药物长效α-半乳糖苷酶A产品pegunigalsidase alfa审查周期
Protalix BioTherapeutics是一家致力于开发、生产和商业化由其专有的ProCellEx®植物细胞蛋白表达系统生产的重组治疗蛋白的生物制药公司。近日,该公司与合作伙Chies
网络 - 法布雷病 - 2020-12-02
优化标签外药物使用的治疗决策:范围界定审查和改进实践和研究的共识建议
目的我们提供全面的共识建议,以优化标签外药物使用的治疗决策,并同时推动临床相关研究。成功实施需要适当的资金和基础设施支持,以吸引必要的利益相关者参与并促进相关伙伴关系,这是决策者必须紧急应对的重大挑战
Pharmacoepidemiology and Drug Safety - 标签外药物 - 2023-05-30
欧洲食品药品监督管理局启动默沙东的Keytruda/chemo联合用药的审查
欧洲监管机构启动了对MSD的keytruda/培美曲塞联合用于转移性非鳞癌非小细胞肺癌(NSCLC)一线治疗的审查。
MedSci原创 - 默沙东,联合用药,Keytruda/chemo - 2018-04-25
FDA开始优先审查来那度胺与美罗华联合治疗淋巴瘤的潜力
美国食品和药物管理局FDA已开始优先审查Celgene的Revlimid来那度胺与罗氏的Rituxan美罗华联合治疗淋巴瘤的潜在价值。
MedSci原创 - 淋巴瘤,来那度胺,美罗华 - 2019-02-28
总局公开征求仿制药一致性评价受理审查指南及相关单据意见
总局办公厅公开征求《仿制药质量和疗效一致性评价受理审查指南(需一致性评价品种)(征求意见稿)》《仿制药质量和疗效一致性评价受理审查指南(境内共线生产并在欧美日上市品种)(征求意见稿)》及相关单据意见
CFDA - 一致性评价,CFDA - 2017-06-10
LORBRENA(lorlatinib)治疗先前未经治疗的ALK阳性肺癌的sNDA已被美国FDA接受优先审查
辉瑞公司今天宣布,美国食品和药品监督管理局(FDA)已接受对LORBRENA®(lorlatinib)的补充新药申请(sNDA),以作为ALK阳性转移性非小细胞肺癌(NSCLC)的一线治疗药物
MedSci原创 - 非小细胞肺癌,非鳞非小细胞肺癌,非小细胞肺癌患者,ALK阳性肺癌,LORBRENA(lorlatinib) - 2020-12-29
默克针对革兰氏阴性菌感染的抗生素组合Recarbrio,获得FDA的优先审查
美国食品和药物管理局(FDA)已开始对默克的抗生素组合药物Recarbrio进行审查,该药可为难以治疗的革兰氏阴性菌感染提供新的选择。
MedSci原创 - 默克,革兰氏阴性菌,抗生素组合,Recarbrio,FDA,优先审查 - 2020-02-04
FDA批准了优先审查赛诺菲的白细胞介素-4单抗Dupixent治疗鼻窦炎
该药物获得优先审查是基于两项关键性III期试验数据的支持,这些试验评估了Dupixent与标准治疗药物皮质类固醇鼻喷雾剂联合使用时的疗效和安全性。
MedSci原创 - 白细胞介素-4单抗,Dupixent,鼻窦炎 - 2019-03-08
尿液有形成分分析仪、尿液分析仪注册审查指导原则(2024年修订版)
为进一步规范医疗器械的管理,国家药监局器审中心组织制修订了《尿液有形成分分析仪注册审查指导原则(2024年修订版)》、《尿液分析仪注册审查指导原则(2024年修订版)》,现予发布。
国家药品监督管理局医疗器械技术审评中心 - 尿液 - 2024-06-04
眼科超声乳化和玻璃体切除设备及附件注册技术审查指导原则(2023年修订版)
根据国家药品监督管理局2023年度医疗器械注册审查指导原则制修订计划的有关要求,我中心组织修订了《眼科超声乳化和玻璃体切除设备及附件注册技术审查指导原则(2023年修订版)》。
国家药品监督管理局 - 玻璃体切除 - 2024-01-24
美国优先审查Keytruda/chemo联用作为鳞状非小细胞肺癌一线用药
美国监管机构已对MSD的申请进行了优先审查,以推广免疫疗法Keytruda与化疗联合作为鳞状非小细胞肺癌(NSCLC)的一线治疗方案。
MedSci原创 - Keytruda/chemo联用 - 2018-07-03
FDA 和行业对医疗器械De Novo 分类请求的行动:对 FDA 审查时间和目标的影响
2017 年医疗器械用户费用修正案 (MDUFA IV) 修订了《联邦食品、药品和化妆品法案》(FD&C 法案),授权 FDA 就对 2017 年 10 月 1 日或之后收到的某些上市前提交的
FDA - 医疗器械 - 2021-10-24
正电子发射/X射线计算机断层成像系统(数字化技术专用)注册审查指导原则
为加强医疗器械产品注册工作的监督和指导,进一步提高注册审查质量,根据《医疗器械注册与备案管理办法》(国家市场监督管理总局令第47号),国家药品监督管理局组织制定了生物安全柜注册审查指导原则等2项技术指
CDE - 成像系统 - 2022-01-24
为您找到相关结果约500个