药品医疗器械审评审批制度意见:经典名方类中药,按照简化标准审评审批
近日,中共中央办公厅、国务院办公厅印发了《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》,并发出通知,要求各地区各部门结合实际认真贯彻落实。其中第十三条提出支持中药传承和创新。建立完善符合中药特点的注册管理制度和技术评价体系,经典名方类中药,按照简化标准审评审批。
中国中医 - 药品医疗器械审评审批,经典名方类中药,简化 - 2017-10-16
国家药品监督管理局药品审评过程中审评计时中止与恢复管理规范(试行)
为加强药品监督管理,国家药品监督管理局发布了《国家药品监督管理局药品审评过程中审评计时中止与恢复管理规范(试行)》,本文为其具体文件内容。
国家药品监督管理局官网 - 药品审评 - 2023-08-17
药审中心拟优先审评名单更新
4月17日,药审中心公示的拟优先审评的药品品种新增以岭万洲国际制药有限公司的非洛地平缓释片(规格为2.5mg、5mg、10mg),公示期间如有异议,可在药审中心网站“信息公开-->优先审评公示-->拟优先审评品种公示
中国药审 - 优先评审,药品注册 - 2019-04-22
药品注册申请审评期间变更工作程序(试行)
为配合《药品注册管理办法》的贯彻实施,药审中心组织制定了《药品注册申请审评期间变更工作程序(试行)》。
国家药品监督管理局药品审评中心 - 药品注册 - 2023-07-18
抗疟疾新药获FDA优先审评资格
近日,60 Degrees Pharmaceuticals(60P)宣布,美国FDA授予其预防成人疟疾药物Tafenoquine (TQ)优先审评资格。2018年1月,该药物获得FDA的快速通道资格。
药明康德 - Tafenoquine,FDA,优先审评 - 2018-02-12
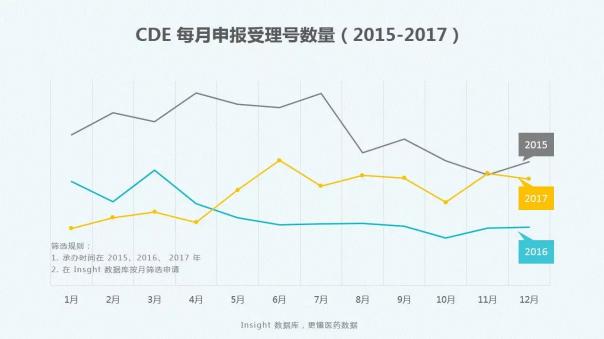
2017全年CDE药品审评报告
Insight数据库2017年终报告梳理了2017年CDE药品申报和审评的数据情况,让大数据来为你指路。
Insight数据库 - 药品审评,CDE,2017 - 2018-01-12
8款药品注册申请拟纳入优先审评
2019年3月29日,药审中心公示的拟优先审评的药品品种新增“盐酸安非他酮缓释片”等,公示期间如有异议,可在药审中心网站“信息公开-->优先审评公示-->拟优先审评品种公示”栏目下提出异议。
中国药审 - 药品,优先审评 - 2019-04-01
药品审评中心补充资料工作程序(试行)
为配合《药品注册管理办法》的贯彻实施,进一步规范药品注册审评补充资料管理工作,结合药品审评以流程为导向的科学管理体系的研究成果和审评工作实际,药审中心研究制定了《药品审评中心补充资料工作程序(试行)》
CDE - 药品审评中心 - 2020-12-07
关于药品注册审评若干问题的讨论
主要问题是审评效率太低,不少企业资料报上去以后,在漫长的排队等待过程中,从充满期望,到失望,到绝望。我们经常批评国内企业不注重研发投入,实际上药品审批的低效率,在很大程度上遏制了企业投入研发的热情。创新药物研发的周期长是客观事实,但“长”在研发过程本身,而不是“长”在漫
蒲公英微信 - 药品,注册 - 2014-11-30
FDA:儿科罕见病优先审评券计划(草案)
本指南提供了有关食品和药物管理局安全与创新法案 (FDASIA) 第 908 节的实施信息,该法案将第 529 节添加到《联邦食品、药品和化妆品法案》(FD&C 法案)中。 根据第 529 条
FDA - 罕见病 - 2021-10-25
为您找到相关结果约500个