Molecular Psychiatry:环境模型中mTOR-FMRP通路的失调与突触可塑性在自闭症谱系障碍中的作用
2024-11-30 xiongjy MedSci原创 发表于上海
Fmr1突变与母体免疫激活(MIA)处理在小鼠模型中均可导致ASD样行为,如社交沟通障碍、社交互动困难及重复行为。
自闭症谱系障碍(ASD)是由基因、表观遗传和环境因素引起的复杂神经发育障碍。人类FMR1基因的突变会导致最常见的单基因型自闭症——脆性X综合症(FXS)。本研究探索了FMR1基因与病毒样感染的交互作用作为环境因素对自闭症样行为和mGluR1/5-mTOR通路的影响。

在该研究中,采用了Fmr1缺失小鼠(Fmr1 KO)和野生型小鼠(WT)进行实验。怀孕期的Fmr1杂合小鼠母鼠和野生型雄鼠配对,并在怀孕12.5天时进行Poly (I:C)注射,以模拟母体免疫激活。实验后代在8至10周龄时进行了多种行为测试,包括超声波发声(USVs)、拾回测试、开放场测试、新物体探索、升高十字迷宫、弹珠埋藏测试、三室社交偏好测试、预刺激抑制(PPI)测试等。通过这些测试评估ASD的核心症状,如社交沟通障碍、互动困难和重复行为等。行为数据的最终结果通过综合分析各项测试的表现得出ASD症状评分。
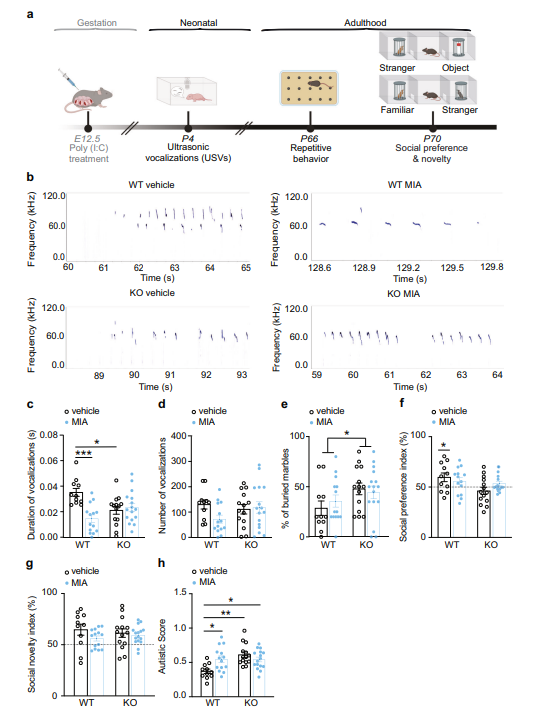
图1:MIA不会加剧Fmr1 KO小鼠的核心自闭症样行为
研究表明,MIA处理的野生型小鼠后代在成年后表现出ASD样行为,包括社会沟通和互动障碍及重复性行为,但不伴随超活动或焦虑等相关共病症。MIA处理导致海马区FMRP水平显著下调,TSC2水平降低,进而导致mTOR通路的过度激活。此外,Fmr1突变小鼠单独表现出较野生型小鼠更高的mTOR信号活性。进一步的分析发现,MIA处理破坏了mGluR1/5的长时程抑制(LTD)通路,转而促进海马突触的长时程增强(LTP)。值得注意的是,Fmr1突变小鼠与MIA暴露的组合未见LTD转变为LTP,表明FMRP的缺失在一定程度上封闭了MIA的影响。
研究还揭示了MIA对FMRP降解的影响,MIA处理导致FMRP的泛素化降解过程受阻。此外,MIA在胚胎期(而非青春期或成年期)暴露时,才会对FMRP水平产生持久影响,这一结果表明胚胎期是免疫激活最为脆弱的时期。免疫激活通过改变蛋白质合成和稳定性,进而影响突触可塑性,可能导致ASD样行为的发生。
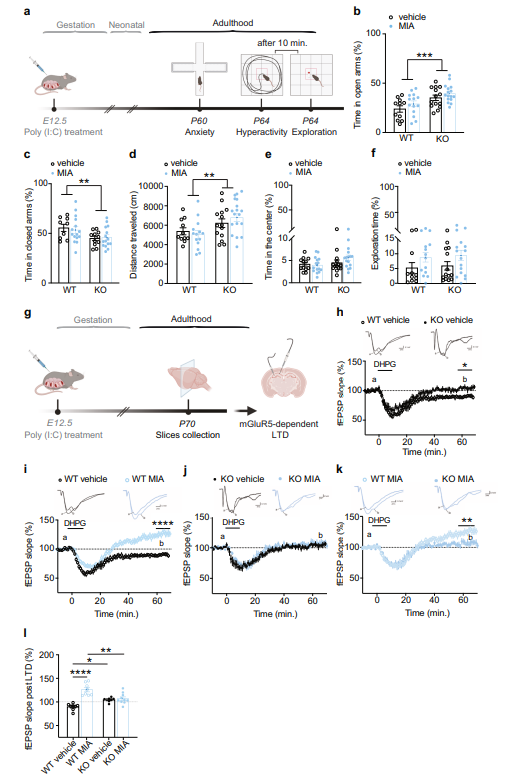
图2:MIA处理不会影响Fmr1 KO小鼠的焦虑和超活动,但在WT和Fmr1 KO小鼠中都破坏了mGluR1/5信号通路
本研究提供了强有力的证据,表明Fmr1突变和母体免疫激活(MIA)通过相似的分子机制影响ASD样行为。具体而言,二者都通过过度激活mTOR通路、下调FMRP水平以及破坏mGluR1/5-LTD通路,导致核心自闭症行为的出现。这些结果为自闭症的遗传和环境因素相互作用提供了新的见解,特别是在突触可塑性和蛋白质合成的调节机制方面。进一步的研究需要深入探讨免疫激活如何在大脑发育过程中改变FMRP的合成和降解,揭示免疫挑战如何在不同发育窗口对神经发育产生长期影响。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#脆性X综合征# #自闭症谱系障碍(ASD)# #突触可塑性# #母体免疫激活#
20