梅奥千例研究,证实NDMM诱导治疗结束至移植的间隔可影响PFS
2022-10-10 聊聊血液 网络
在过去20年中,多发性骨髓瘤 (MM)治疗方案的新进展和自体干细胞移植 (ASCT)的持续使用显著改善了生存结局,但移植的作用最近受到了来自新药及其组合的挑战,它们能够有效控制疾病且在无巩固性移植的情
在过去20年中,多发性骨髓瘤 (MM)治疗方案的新进展和自体干细胞移植 (ASCT)的持续使用显著改善了生存结局,但移植的作用最近受到了来自新药及其组合的挑战,它们能够有效控制疾病且在无巩固性移植的情况下达到相当的结局。这一结果主要是由移植相关手术(如感染)的毒性所驱动,即使它的持续时间已经达到最低,并且通常是可逆的。然而也有许多临床试验表明,与仅药物治疗相比,ASCT仍具有显著的生存获益,近1/3的患者可在未接受任何额外治疗的情况下达到完全缓解 (CR),从诊断开始的中位 PFS 也可达18个月至2年 。
适合一线移植的患者通常接受3-6个周期的诱导方案,然后接受大剂量美法仑和自体干细胞输注。通常情况下,最后一个诱导周期是在干细胞动员和单采前3-4周完成;虽然使用 CXCR 拮抗剂(如普乐沙福)可减少单采延迟,但其他后勤问题仍可增加诱导结束与启动 ASCT之间的间隙。随后患者会接受大剂量化疗并回输干细胞。
尽管许多风险因素(如年龄、肥胖、既往辐射暴露)有助于预测移植结局,但尚不清楚末次化疗日期和干细胞输注日期之间无药物期间的疾病恶化,是否预示着高危疾病和移植后临床结局较差。为评估无化疗期对 ASCT 后无进展生存期 (PFS) 和总生存期 (OS) 的影响,梅奥Shaji Kumar教授等回顾了本中心15年间接受自体移植的1055例NDMM患者数据,发现诱导治疗结束到开始移植的时间以33天为界,>33天患者的PFS显著较差。详细结果近日发表于欧洲血液与骨髓移植学会(EBMT) 的官方期刊《Bone Marrow Transplantation》。

研究方法
该回顾性队列研究纳入了2004年至2018年在梅奥诊所就诊并在诊断后1年内接受一线 ASCT 的所有NDMM患者。排除诱导治疗期间疾病进展的患者,以及在动员前接受环磷酰胺脉冲治疗的患者,因为与标准方案相比,它将人为延长至移植时间。此外为了确保队列同质性,还排除了所有在干细胞采集后接受维持治疗或其他化疗方案的患者。
作者先评估每例患者诱导方案的持续时间,记录患者的末次化疗准确日期,根据从末次化疗日期至干细胞输注日期计算的中位至移植时间 (TTT) 将患者分为2组;然后还收集了预处理方案的给药,并根据IMWG标准确定移植前达到的生化缓解水平。研究中收集了整个队列的基线临床特征,del17p、t(4;14)、t(14;16)、t(14;20)、gain1q异常为高危]。研究终点为PFS(从干细胞输注日期至生化进展或强化治疗日期)和OS(从干细胞输注日期至全因死亡日期)。
研究结果
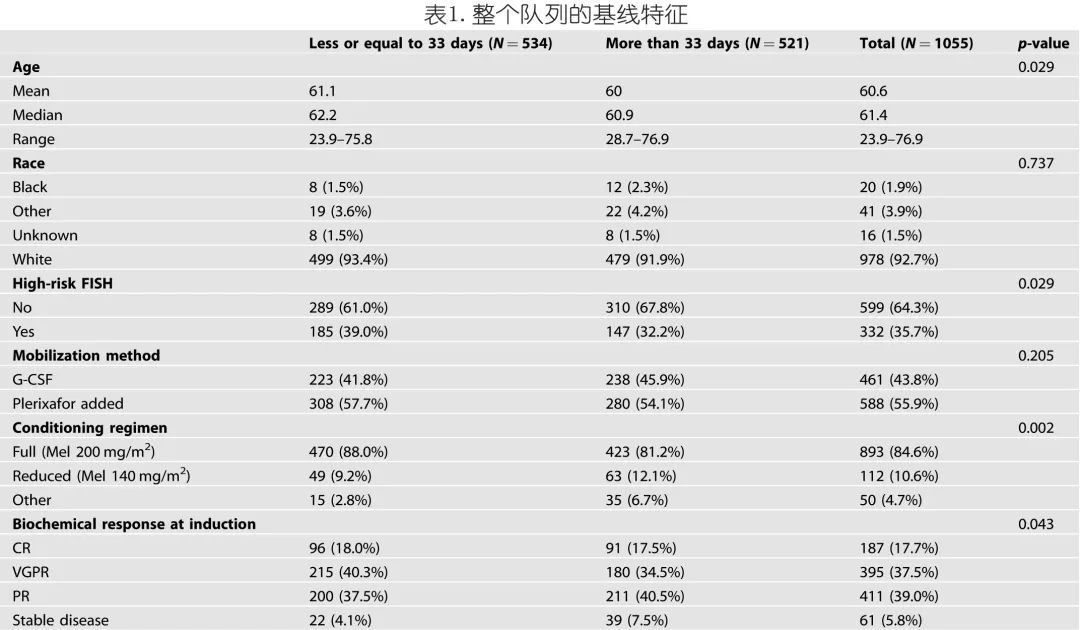
共1055例NDMM患者在诊断后一年内接受自体干细胞移植。诊断时的中位年龄为61.4岁,332例(35.7%)患者有高危 FISH 异常。整个队列中461例 (43.8%) 患者单用 G-CSF 动员,588例 (55.9%) 加用普乐沙福。预处理方面,893例 (84.6%) 患者接受美法仑200 mg/m2,其余患者 [112例 (10.6%)] 接受低剂量方案或其他美法仑方案 [50例 (4.7%)]。干细胞输注日期后的中位PFS和OS分别为33.4和122.3个月。基线临床特征见表1。
自末次化疗日期起的中位 TTT 为33天,因此根据中位TTT(33天)对队列进行了分组。结果发现,TTT ≤33天的患者 PFS 显著长于>33天的患者(35.6 vs. 32.1个月,p< 0.03),但 OS 的差异不显著(128 vs. 122.2个月,p= 0.68)(图1和2)。

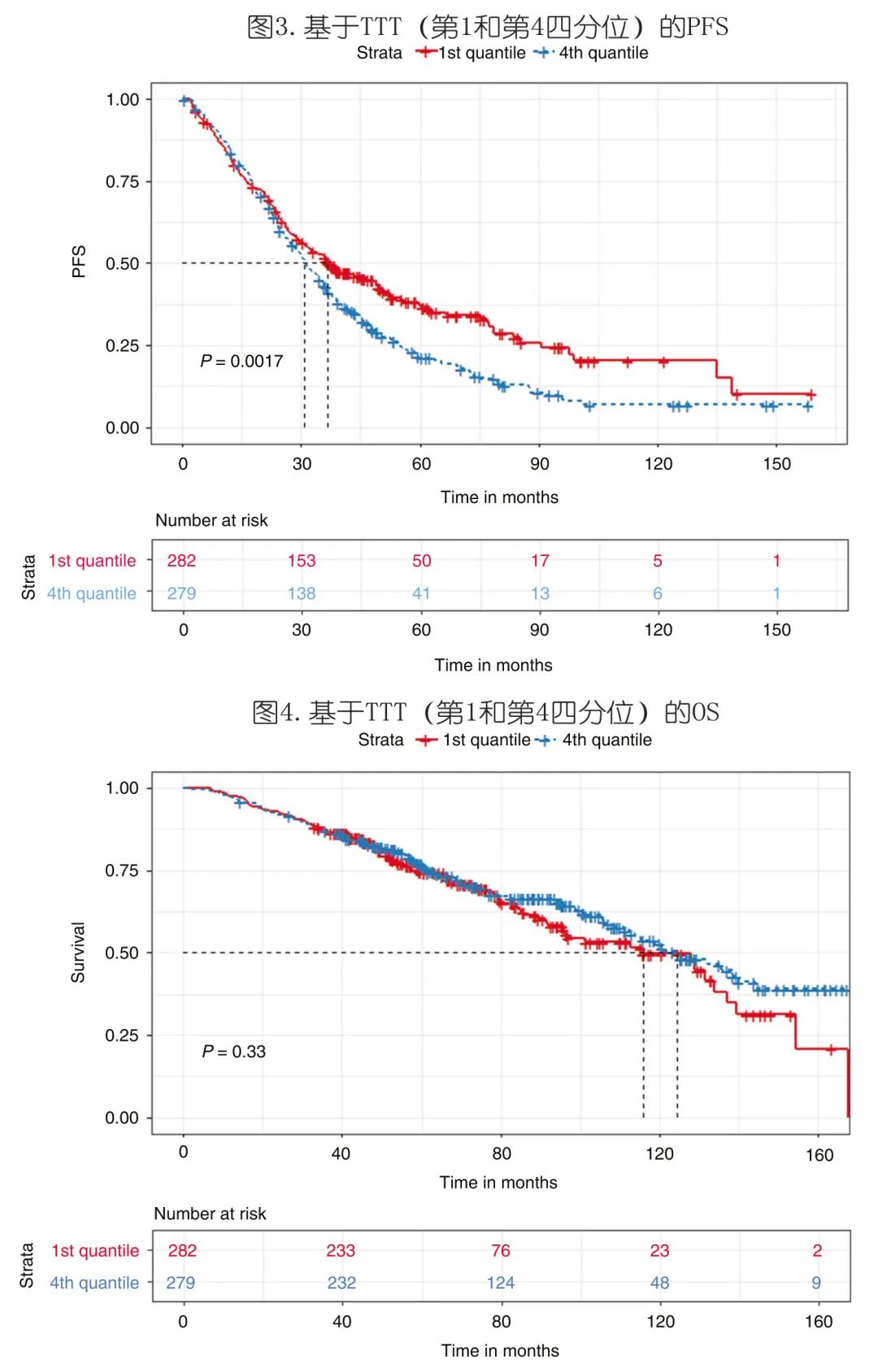
作者随后根据四分位 TTT 对患者进行分组,发现 TTT ≤27天(第1四分位)的患者与TTT >42天(第4四分位)的患者相比,PFS显著延长(36.7 vs. 30.9个月,p< 0.01),但 OS 的差异仍不显著(115.8 vs. 124.4个月,p= 0.33)(图3和4)。
单变量分析发现,与 TTT ≤33天的患者相比,TTT >33天患者 PFS 的HR= 1.17(p< 0.03)。作者随后进行多变量分析以确定 TTT 延长是否是 MM 患者 PFS 缩短的独立风险因素,模型考虑了年龄、移植前的生化缓解、预处理剂量和诊断时的 FISH 结果,结果发现 TTT 延长患者 PFS 缩短的风险增加 (HR= 1.19,p< 0.03)。
然后作者将患者分为四分位,并将第1四分位与第4四分位进行比较,结果PFS 的单变量分析显示 TTT 第4四分位患者的HR= 1.37(p< 0.01),多变量分析显示HR= 1.34(p< 0.01)。
作者又根据移植前获得的生化缓解进行亚组分析,将患者分为“良好”缓解者(≥VGPR)和“不良”缓解者(<VGPR)。对于良好缓解组,基于中位 TTT 的PFS 和 OS 无显著差异(分别为36.4 vs.37.3个月,p= 0.5和106.9 vs. 112.6个月,p= 0.81);在四分位比较中,与第4四分位组相比,第一四分位组患者的 PFS 显著延长(36.4 vs. 33.8个月,p< 0.03),OS则仍无显著差异(96.9 vs. 107.2个月,p= 0.93)(图5和6)。

在不良缓解组中,与 TTT >33天的患者相比,TTT ≤33天患者的 PFS 同样显著延长(30.5 vs. 27个月,p< 0.03),但 OS 相似(129 vs. 125个月,p= 0.96)(图7和8)。在四分位比较方面,与第4四分位组相比,第1四分位组患者的 PFS 显著延长(37.7 vs. 28.7个月,p< 0.04);OS则未发现显著差异(129 vs. 132个月,p= 0.26)(图9和10)。

讨论
本研究是首次在新诊断、适合移植的 MM 患者中探索末次化疗日期和干细胞输注日期之间的时间间隔对临床相关结局的影响,结果表明该时间间隔在接受自体干细胞移植的 MM 患者的PFS 中起重要作用。
本研究中位 TTT 为33天, TTT 延长(>33天)的患者的 PFS 显著差于末次化疗日期后33天内输注干细胞的患者,因此TTT第4四分位(>42天)患者的 PFS 显著差于第1四分位(≤27天)患者。此外根据诱导时达到的 IMWG 生化缓解情况对患者进行分组后发现不利影响更明显:移植前未获得>PR 缓解的患者PFS的差异最显著,表明这一队列可能更受益于强化疗方案,从而使其病程中不会导致治疗间隔延长。
本研究中一致的 PFS 差异未转化为OS的差异,可能原因在于接受诱导治疗存在显著差异。此外大多数队列并不常规使用移植后维持,且挽救治疗不统一。
TTT在当下的临床研究中并不常规报告,大多数 NDMM 移植合格患者的随机对照试验方案仅需报告至动员时间。根据本研究结果,未来的试验将 TTT 纳入患者评估可能是有益的,尤其是对于在干细胞输注前显示复发体征的患者
总的来说,本研究证明了 TTT 在 NDMM 患者临床结局中的重要作用。与更紧密的化疗方案(≤27天)相比,TTT延长(>42天)与结局较差相关,且该结果在诱导治疗时低于 VGPR 的患者中尤其严重,在多变量分析也具有预后意义。虽然仍需进一步的前瞻性研究来验证 TTT 对临床相关结局的影响,但作者建议在干细胞输注前不应给予患者太久的无化疗期,因其可能对病程产生不利影响。
参考文献
Charalampous C,Goel U,Gertz M,et al.Impact of the time interval between end of induction and autologous hematopoietic transplantation in newly diagnosed patients with multiple myeloma.Bone Marrow Transplant . 2022 Oct 6. doi: 10.1038/s41409-022-01835-y
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言