罗氏PD-L1单抗Tecentriq联合靶向疗法:获FDA批准治疗晚期黑色素瘤
2020-08-01 MedSci原创 MedSci原创
该组合治疗改善了患者的中位无进展生存期(PFS)至15.1个月,而安慰剂组为10.6个月。
罗氏公司宣布美国食品药品监督管理局(FDA)已批准其PD-L1单抗Tecentriq联合MEK抑制剂Cotellic(cobimetinib)和BRAF抑制剂Zelboraf(vemurafenib),用于治疗BRAF V600突变阳性的晚期黑色素瘤患者。在几乎所有黑色素瘤患者中,BRAF蛋白均发生突变。
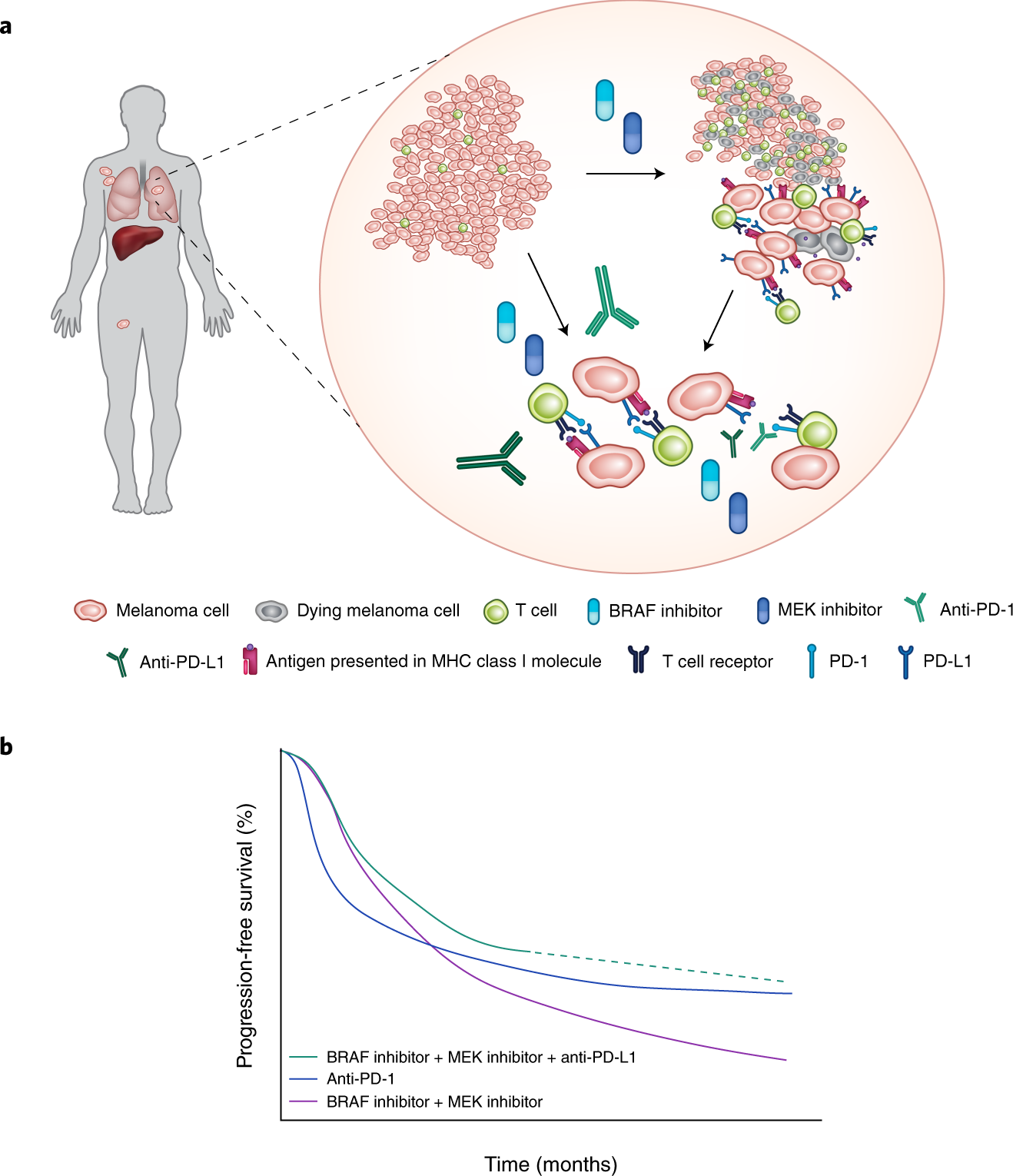
图片来源:https://www.nature.com/articles/s41591-019-0482-7?utm_source=nm_etoc&utm_medium=email&utm_campaign=toc_41591_25_6&utm_content=20190611&WT.ec_id=NM-201906&sap-outbound-id=50F55675FCE609D28CF2EA96DB76D70633ADCB4D
此次批准基于3期研究Imspire150的结果,该组合治疗改善了患者的中位无进展生存期(PFS)至15.1个月,而安慰剂组为10.6个月。
罗氏Genentech首席医学官Levi Garraway表示:“将癌症免疫疗法与靶向疗法联合使用,BRAF V600突变阳性的晚期黑色素瘤患者可以存活超过15个月且疾病不恶化。FDA对Tecentriq组合的批准是晚期黑素瘤治疗的重要一步。”
然而,罗氏可能会面临来自竞争对手默克公司的Keytruda(pembrolizumab)和百时美施贵宝的Opdivo的激烈竞争,这些药物作为治疗黑素瘤的药物已经上市多年。Keytruda早在2014年9月就被批准用于治疗晚期黑色素瘤,当时它成为PD-1/L1类药物中首个在美国获得批准的药物。Opdivo也在2015年获批治疗晚期黑色素瘤患者。
除了黑色素瘤,罗氏的Tecentriq还在肺癌,泌尿生殖道,皮肤,乳腺癌,胃肠道,妇科和头颈癌方面正在进行或计划了多个3期研究。
原始出处:
http://www.pmlive.com/pharma_news/roches_tecentriq_combo_scores_fda_approval_in_melanoma_1346047
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#罗氏PD-L1单抗#
42
#联合靶向#
40
#TEC#
40
#FDA批准#
40
#色素#
38
不错
105
#PD-L1#
28
#靶向疗法#
45
#PD-L1单抗Tecentriq#
37
#Tecentriq#
43