指南更新 | 宫颈癌NCCN(2025.V1)一线治疗免疫推荐再丰富!
2024-12-24 e路新干线 e路新干线 发表于陕西省
2025.V1 宫颈癌 NCCN 指南 12.19 更新,放化疗、一线及二线治疗药物方案有新增与级别调整,基于相关研究结果,为宫颈癌治疗提供更多选择与优化策略。
2025.V1-2024.12.19
宫颈癌
NCCN指南
2024年12月19日,宫颈癌NCCN指南更新至2025.V1,此次药物治疗更新的主要内容是宫颈癌全身治疗放化疗的首选方案正式新增“顺铂+帕博利珠单抗(1类:FIGO 2014 Ⅲ-ⅣA期;2B类:FIGO 2018 Ⅲ-ⅣA期)”、“如果顺铂不耐受,卡铂+帕博利珠单抗(1类:FIGO 2014 Ⅲ-ⅣA期;2B类:FIGO 2018 Ⅲ-ⅣA期)”;一线治疗首选方案新增“阿替利珠单抗+顺铂/紫杉醇+贝伐珠单抗(1类)”、“阿替利珠单抗+卡铂/紫杉醇+贝伐珠单抗(1类)”;二线或后续治疗某些情况下有用,PD-L1阳性肿瘤新增“tisotumab vedotin-tftv+帕博利珠单抗”、新增“HER2突变肿瘤:奈拉替尼”、NTRK基因融合阳性肿瘤新增“瑞普替尼”。详细更新内容如下:
01 更新内容
宫颈癌全身治疗——鳞状细胞癌、腺癌、腺鳞癌
放化疗
🔹首选方案正式新增“顺铂+帕博利珠单抗(1类:FIGO 2014 Ⅲ-ⅣA期;2B类:FIGO 2018 Ⅲ-ⅣA期)”、“如果顺铂不耐受,卡铂+帕博利珠单抗(1类:FIGO 2014 Ⅲ-ⅣA期;2B类:FIGO 2018 Ⅲ-ⅣA期)”
🔹其他推荐方案修改:“如果单药顺铂和卡铂不可用”
一线治疗
🔹首选方案新增“阿替利珠单抗+顺铂/紫杉醇+贝伐珠单抗(1类)”、“阿替利珠单抗+卡铂/紫杉醇+贝伐珠单抗(1类)”
二线或后续治疗
🔹首选方案“tisotumab vedotin-tftv”由2A类推荐调整为1类推荐
🔹其他推荐方案“西米普利单抗”由首选方案调整为其他推荐方案
🔹某些情况下有用,PD-L1阳性肿瘤新增“tisotumab vedotin-tftv+帕博利珠单抗”、新增“HER2突变肿瘤:奈拉替尼”、NTRK基因融合阳性肿瘤新增“瑞普替尼”
🔹脚注a修改:FDA获批的生物类似物是贝伐珠单抗的适当替代品。FDA获批的生物类似物是NCCN指南中任何推荐的全身生物治疗的适当替代品(也适用于CERV-F 2/3)
🔹脚注d修改:同步EBRT联合含铂化疗,使用顺铂作为单一药物(如果顺铂不耐受则使用卡铂)。帕博利珠单抗可与CRT同步应用:顺铂(或卡铂)/RT联合帕博利珠单抗(FIGO 2014 Ⅲ-ⅣA期:1类);顺铂(或卡铂)/RT联合帕博利珠单抗(FIGO 2018 Ⅲ-ⅣA期:2B类)。帕博利珠单抗可联合单独CRT用于FIGO 2014 Ⅲ-ⅣA期宫颈癌患者。KEYNOTE-A18(NCT04221945)是一项多中心、随机、双盲、安慰剂对照试验,纳入598例既往未接受过根治性手术、放疗或全身治疗的FIGO 2014 Ⅲ-ⅣA期宫颈癌患者,评估了顺铂与帕博利珠单抗联合EBRT的疗效。处方信息:https://www.accessdata.fda.gov/drugsatfda_docs/label/2024/125514s147lbl.pdf
🔹脚注h修改:推荐用于肿瘤表达PD-L1(CPS≥1)的患者,经FDA批准的检测或在CLIA认证的实验室进行的检测确定
🔹新增脚注i:皮下注射阿替利珠单抗和hyaluronidase-tqjs注射液可替代静脉注射阿替利珠单抗。与静脉注射阿替利珠单抗相比,皮下注射阿替利珠单抗和hyaluronidase-tqjs注射液具有不同的剂量和给药说明
🔹脚注k修改:用于不可切除或转移性肿瘤突变负荷高(TMB-H)(≥10突变/兆碱基[mut/Mb])肿瘤患者的治疗,经FDA批准的检测或在CLIA认证的实验室进行的检测确定,这些患者在既往治疗后进展并且没有令人满意的替代治疗方案
🔹新增脚注l:对于PD-L1阳性且未接受过免疫(IO)治疗的患者
🔹新增脚注m:既往未接受过NTRK靶向治疗或在既往NTRK治疗中进展的NTRK阳性肿瘤
🔹删除脚注:当顺铂和卡铂不可及时,可以考虑使用这些药物


02 新增依据
一线治疗首选方案“阿替利珠单抗+顺铂/紫杉醇+贝伐珠单抗(1类)”、“阿替利珠单抗+卡铂/紫杉醇+贝伐珠单抗(1类)”的新增基于一项随机、开放、Ⅲ期研究(BEATcc研究;NCT03556839)1,研究旨在评估阿替利珠单抗联合贝伐珠单抗和铂基化疗一线治疗复发或转移性宫颈癌患者的疗效和安全性。
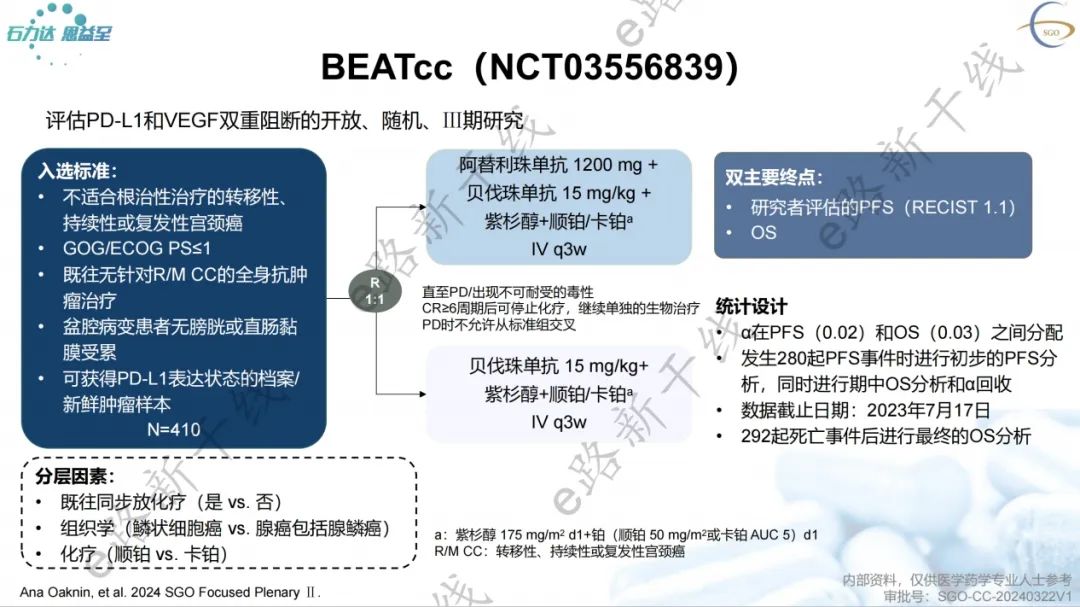
2024 SGO年会报告了该研究的主要结果,研究结果显示,中位随访32.9个月,BEATcc研究达到了双主要终点,与安慰剂组相比,阿替利珠单抗组PFS有统计学显著和临床意义的改善(13.7个月 vs. 10.4个月;HR=0.62,95% CI 0.49-0.78;p<0.0001);与安慰剂组相比,阿替利珠单抗组OS也有统计学显著和临床意义的改善(32.1个月 vs. 22.8个月;HR=0.68,95% CI 0.52-0.88;p=0.0046)。
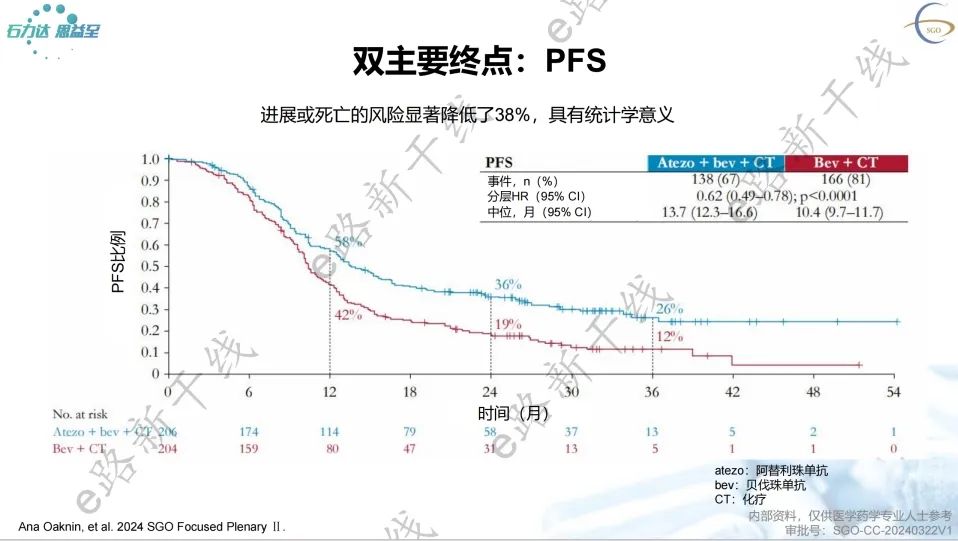
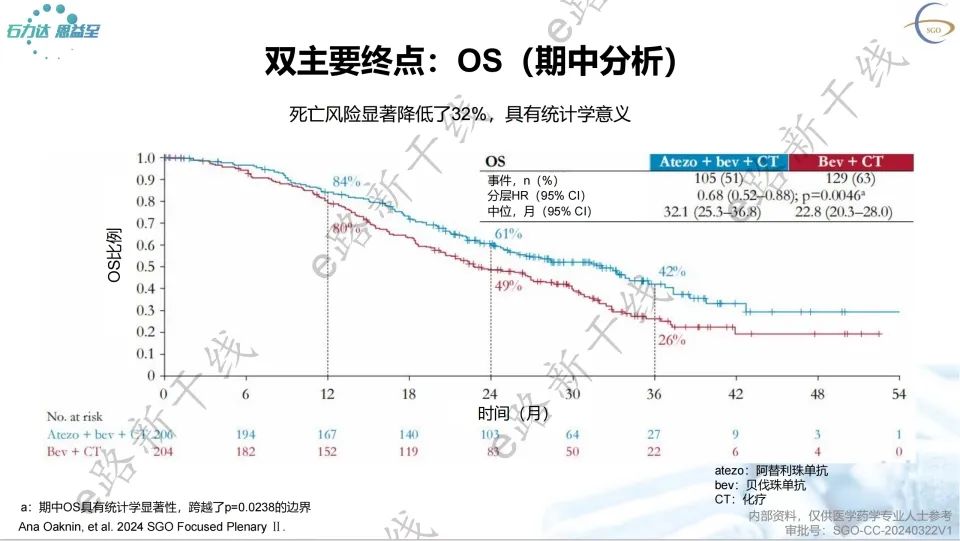
关键次要终点ORR和DoR也观察到有意义的改善。
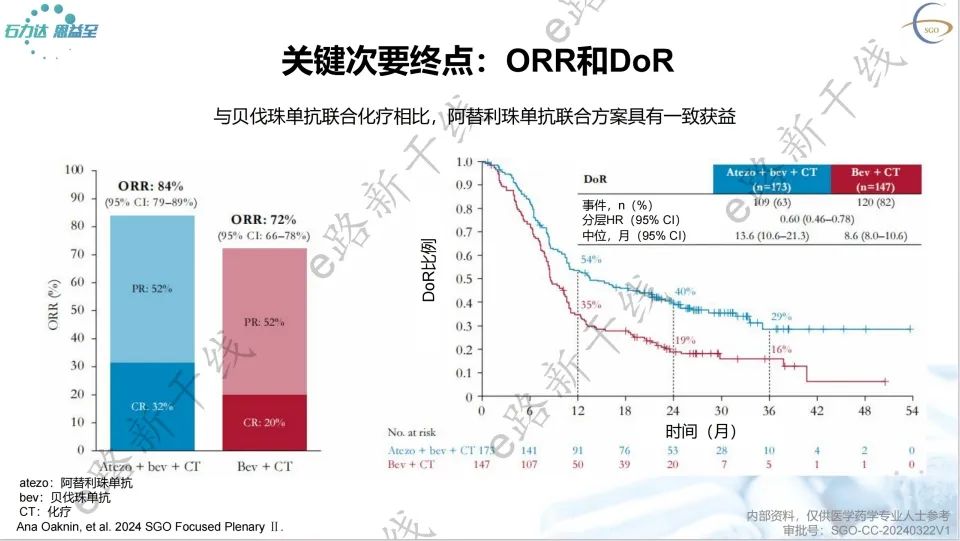
阿替利珠单抗联合贝伐珠单抗和铂基化疗具有可预测和可控的安全性,且没有新的安全性事件发生。
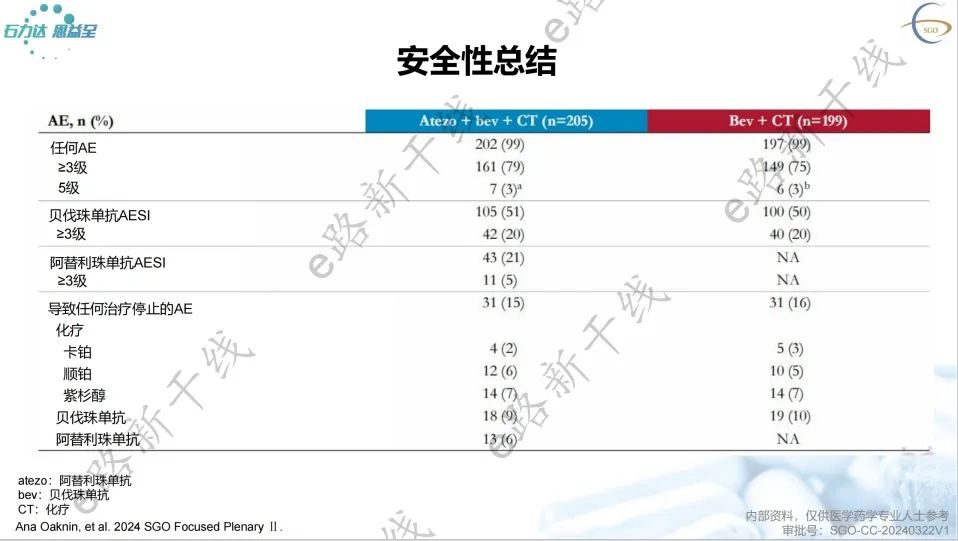
03 总结
此次NCCN指南更新主要是对免疫治疗药物和靶向治疗药物方案的新增和推荐级别的调整。放化疗的“顺铂/卡铂+帕博利珠单抗”方案由脚注部分正式成为首选方案的推荐;基于BEATcc研究的结果,“阿替利珠单抗+顺铂/卡铂+紫杉醇+贝伐珠单抗”成为宫颈癌一线治疗的首选方案;二线或后续治疗方案也有所新增和调整。期待更多研究结果的公布,进一步丰富宫颈癌治疗的格局!
参考文献:
1. Ana Oaknin, et al. 2024 SGO Focused Plenary Ⅱ.
2. NCCN指南:宫颈癌(2025.V1).
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#药物治疗# #宫颈癌#
6