类器官 VS 组织样本 VS 动物模型
类器官技术始于2009年,荷兰Hubrecht研究所的Clevers团队成功的将成体干细胞培养成为小肠的隐窝和绒毛结构。
2013年,来自日本、德国、美国的科研人员分别构建出肝芽、迷你肾和微型大脑,使该领域获得了国际的广泛关注。Science 将其评选为2013年的十大突破。
2017年,Nature Methods 将类器官(Organoids)评选为当年最受瞩目、最具影响力的年度技术。Nature Methods如此评价该技术:利用干细胞直接诱导生成三维组织模型,为人类生物学研究提供了强大的方法。
2019年,Science、Nature、CELL,全球生命科学三大顶级神刊不约而同地推出了关于类器官技术的特刊。Science 特刊内的四篇重磅文献围绕干细胞发展史、类器官模型应用、类器官技术与类器官芯片技术前景等展开论述。
2019年,NEJM(新英格兰医学杂志)发表Organoids-Preclinical Models of Human Disease,指出类器官技术是人类疾病研究的临床前模型,是临床治疗的新手段。
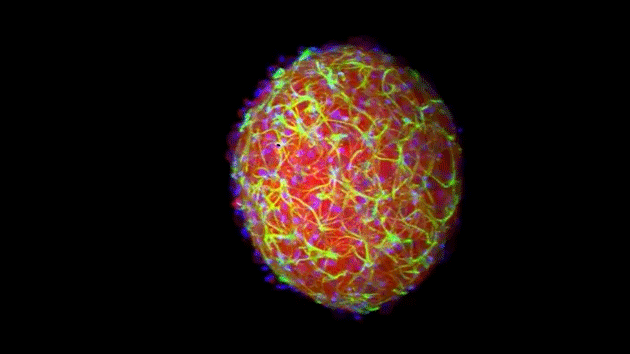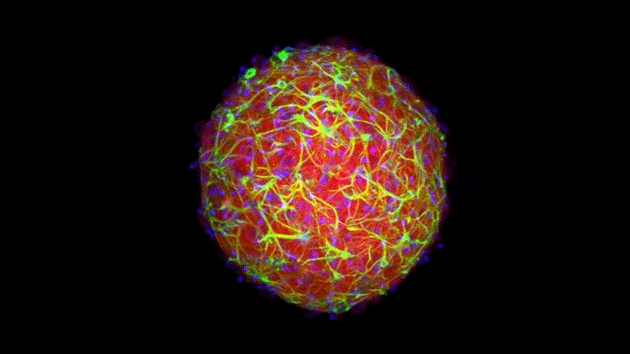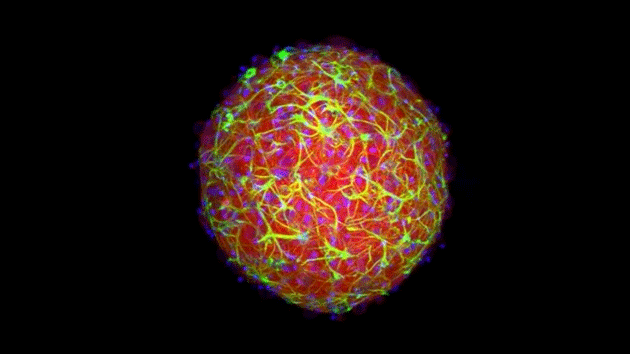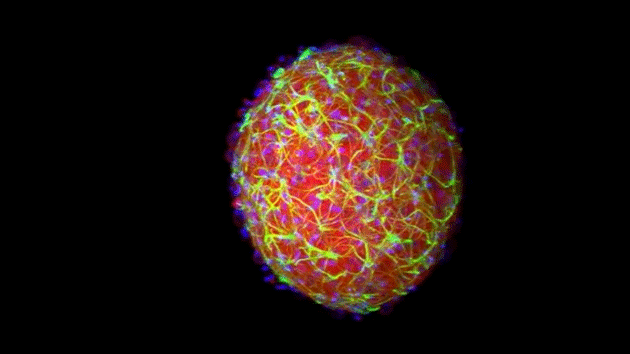 大脑类器官
大脑类器官
类器官技术,作为近10年来生物学界和临床医学最热门的前沿技术之一,备受医学科研领域的关注,并有望冲刺下一个诺奖。-01-
关于类器官有很多定义,有些过于狭窄,我们认为类器官就是由干细胞或器官特异性祖细胞在体外发育成具有复杂三维结构、展现类似体内器官结构和功能的细胞团。

目前类器官培养技术已经成功培养出大量具有部分关键生理结构和功能的类组织器官,比如:肾脏、肝脏、肺脏、小肠、脑、前列腺、胰腺和视网膜等。

从干细胞到类器官
成人干细胞衍生的类器官培养,通常是通过将分离的成人干细胞或所需器官培养的单细胞悬浮液,嵌入到细胞外基质(ECM)水凝胶三维环境中来建立的。
例如肠道器官,从小肠或结肠分离出的隐窝细胞足以培养出类器官,也可以从分离的成人肠干细胞中培养出类器官。上皮类器官培养基是以附加与器官相关的生长因子的培养基为基础的。因此,从其他组织(如呼吸道、肝脏、胰腺、皮肤、膀胱、大脑、心脏)提取的细胞要求在培养中补充相关生长因子。
大脑类器官培养过程:胚胎干细胞在神经诱导介质中生长,产生神经外胚层,嵌入Matrigel中,并在旋转生物反应器或轨道摇床中生长,以更好地扩散,获得三维脑器官。在暴露于维甲酸的情况下,大脑器官通过自我组装模式,形成自缔和组织,形成包括放射状胶质细胞在内的不同种群的神经祖细胞,这些神经祖细胞扩展形成大脑结构。
二是个性化药物筛选和药敏检测。以肿瘤为例,首先将患者来源的肿瘤样本组织通过机械剪切得到肿瘤细胞团,再将细胞团酶消化成单细胞。分离消化后,将细胞嵌入到基质胶中并在96/384孔板上进行胶滴的种接,再覆盖以培养基和细胞因子培养。类器官培养至直径几百微米的细胞小球即可用于药筛。
国内外目前共有超过40项类器官临床相关研究。有研究发现:在预测抗癌药物的有效性上,类器官技术具有100%的敏感性,93%的特异性,88%的阳性预测值以及100%的阴性预测值。
三是再生医学。基于类器官作为具有再生能力的组织的无限来源的潜力,研究表明将体外扩增的类器官移植到动物中以修复受损器官具有可行性。
类器官面临的挑战
然而,类器官培养也有其局限性,应该非常谨慎地使用。人体组织器官通常由不同类型的细胞组成,通常由不同的胚层产生,在模拟给定的组织时需要考虑这些。缺乏功能性的血管系统、神经系统或免疫系统是类器官的缺点,这些缺点使类器官远远比不上体内模型。
干细胞诱导形成器官,就类似于调制一杯鸡尾酒,还有很长的路要走 。
《自然 · 综述》:T细胞在衰老中的角色相关链接间充质干细胞治疗(一):国际视野间充质干细胞治疗(二):先进制造工艺间充质干细胞治疗(三):质控体系间充质干细胞治疗(四):效力评价 临床级间充质干细胞的技术壁垒:国际纵览临床级间充质干细胞的技术壁垒:工艺制造临床级间充质干细胞的技术壁垒:给药方式临床级间充质干细胞的技术壁垒:患者选择
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言