Blood | BOVen 方案:靶向治疗 TP53 突变型套细胞淋巴瘤为患者带来新希望
2024-10-27 daikun MedSci原创 发表于上海
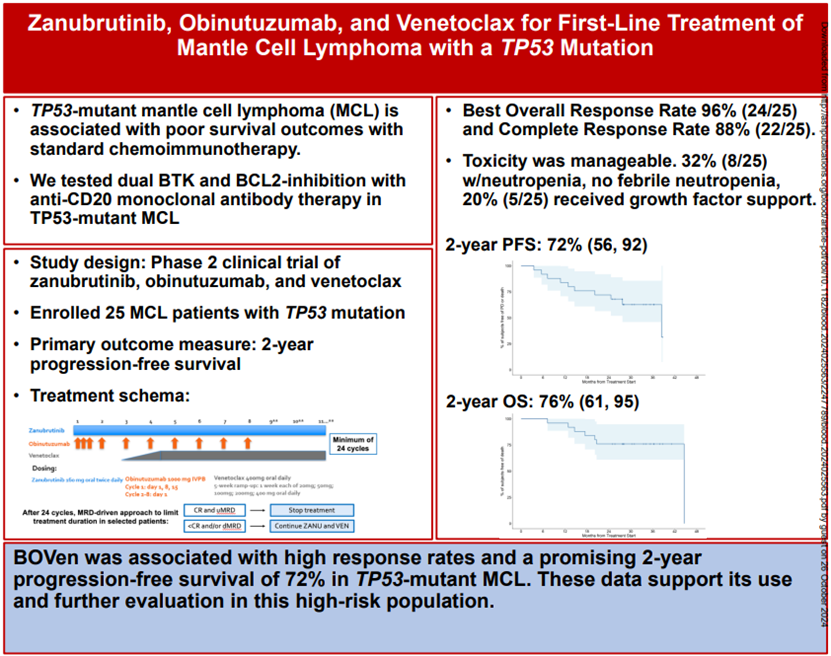
该研究旨在评估泽布替尼、奥妥珠单抗联和维奈克拉(BOVen)联合方案在TP53突变的未经治疗的MCL患者中的疗效和安全性,BOVen方案在TP53突变的未经治疗的MCL患者中具有良好耐受性和高活性。
MCL是一种罕见的、不可治愈的 B 细胞非霍奇金淋巴瘤亚型,其临床和生物学特征具有异质性,MCL 的特征性染色体易位是 t(11;14)(q13;q32),导致细胞周期蛋白 D1 过表达,除了这一标志性易位,MCL还存在其他遗传改变,包括 TP53、CDKN2A、ATM、MYC 和 NOTCH 基因的异常,TP53 基因突变 是 MCL 最重要的不良预后因素之一,大约 10-20% 的新诊断 MCL 患者存在 TP53 突变,TP53 突变与化疗耐药和明显较差的生存结果相关,标准治疗方法是化疗免疫疗法,但 TP53 突变的 MCL 患者即使接受最佳的治疗方案,包括包含阿糖胞苷的诱导化疗和巩固性自体干细胞移植,其无进展生存期 (PFS) 仍然不到一年,因此,这类高风险患者缺乏标准治疗方案,通常建议参加临床试验,BTK 抑制剂和 BCL2 抑制剂治疗复发或难治性 MCL 方面取得了显著进展,并越来越多地应用于一线治疗方案,与第一代 BTK 抑制剂伊布替尼相比,第二代 BTK 抑制剂泽布替尼具有更高的 BTK 特异性,对白介素-2 诱导的 T 细胞激酶 (IL2-ITK) 的抑制作用最小 (IL2-ITK 对抗体依赖性细胞毒性至关重要),并且脱靶相关不良事件更少,随机 3 期临床试验表明,与伊布替尼相比,泽布替尼具有更良好的安全性特征,心脏不良事件发生率更低,治疗中断率更低,泽布替尼在复发或难治性 MCL 中表现出高活性,总缓解率 (ORR) 和完全缓解率 (CR) 分别为 84% 和 25-78%,中位 PFS 为 21.1-33.0 个月,因此,泽布替尼是一种很有吸引力的 BTK 抑制剂,可以与维奈克拉-奥妥珠单抗联合用于 MCL 的治疗,微小残留病 (MRD) 是 MCL 中的一个强大预后指标,可以用于限制无限期靶向治疗的治疗持续时间,该研究旨在评估泽布替尼、奥妥珠单抗联和维奈克拉 (BOVen) 联合方案在 TP53 突变的未经治疗的 MCL 患者中的疗效和安全性。

方法
该研究纳入了25 名既往未经治疗的 TP53 突变的 MCL 患者,患者接受泽布替尼: 160mg 口服,每日两次,从第 1 个周期第 1 天 (C1D1) 开始;奥妥珠单抗: C1D1、第 1 个周期的第 8 天和第 15 天以及第 2-8 个周期的第 1 天给予 1000mg 静脉注射;维奈克拉: 从 C3D1 开始使用五周剂量递增方案 (20mg 至 400mg),然后每日口服 400mg,治疗持续时间:至少 24 个周期,如果患者在 24 个周期后达到完全缓解 (CR) 并使用免疫测序方法检测不到最小残留病 (MRD)(灵敏度水平为 1x10-6),则停止治疗,主要终点为 2 年 PFS 率。
研究结果
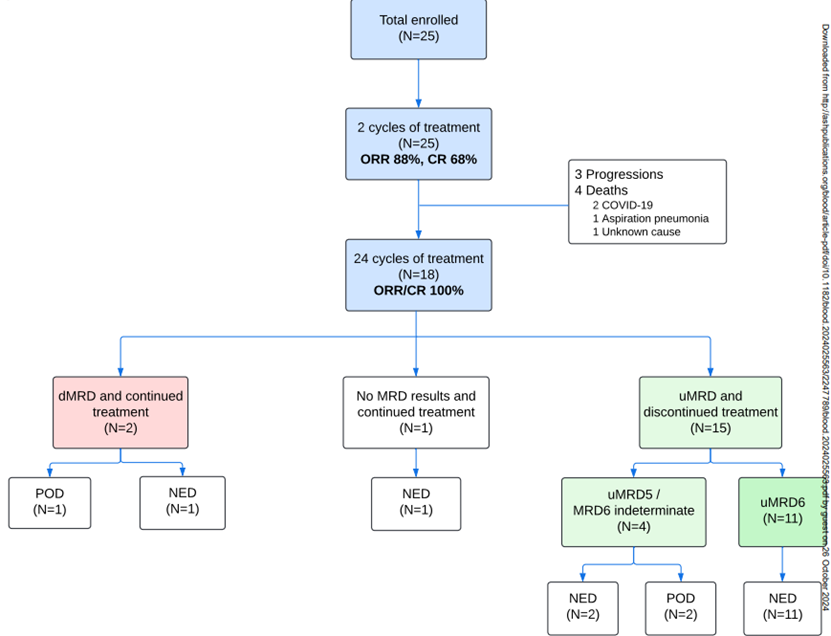
中位随访 28.2 个月时,ORR 为 96% (24/25),CR 率为 88% (22/25),2 年 PFS 率为 72% (95% CI,56 至 92),2 年 OS 率为 76% (95% CI,61 至 95),2 年 DSS 率为 91% (95% CI,79 至 100),在 24 个周期后,18 名患者 (72%) 达到 CR 并停止治疗,6 名患者出现疾病进展,其中 3 名在完成 24 个周期治疗后进展,11 名患者在外周血和骨髓中达到 uMRD6 并在治疗结束后保持缓解。
安全性分析
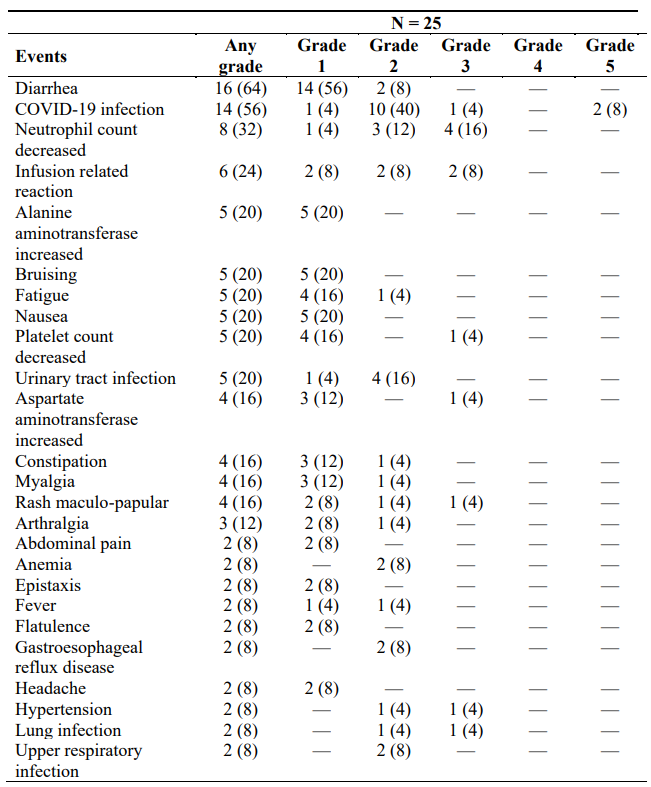
最常见的不良事件是腹泻 (64%)、COVID-19 感染 (56%)、中性粒细胞减少 (32%) 和输注相关反应 (24%),16% 的患者出现 3 级中性粒细胞减少,但可逆,没有出现发热性中性粒细胞减少,5 名患者 (20%) 在治疗期间接受了生长因子支持,1 名患者 (4%) 出现 3 级或更高的血小板减少,并通过剂量减少得到解决,48% 的患者出现严重不良事件,包括 COVID-19 感染 (n=6)、房颤 (n=1)、无中性粒细胞减少的发热 (n=1)、肺炎 (n=3)、皮疹 (n=1) 和肿瘤溶解综合征 (n=1),心脏毒性很少见,仅 1 名患者因 3 级房颤而停止使用泽布替尼。
结论
BOVen 方案在 TP53 突变的未经治疗的 MCL 患者中具有良好的耐受性和高活性,该方案达到了主要终点,2 年 PFS 率为 72%,与化疗免疫疗法相比具有优势,这些数据支持将 BOVen 方案用于 TP53 突变的 MCL 的一线治疗,并需要进一步评估其在高风险人群中的应用。
原始出处
Kumar A, et al. 2024. Zanubrutinib, Obinutuzumab, and Venetoclax for First-Line Treatment of Mantle Cell Lymphoma with a TP53 Mutation. Blood:blood.2024025563.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#TP53突变# #MCL# #BOVen方案#
22