《Nature》子刊:先诺欣活性成分先诺特韦发现过程及临床前研究结果
2023-10-17 梅斯医学 梅斯医学 发表于上海
目前,先诺欣已覆盖全国32个省、306个市及超2500家医疗机构,以每月数百万人份的药品可及能力,为新型冠状病毒常态化防控提供重要保障。
2023年10月13日,具有自主知识产权的国产口服小分子抗新冠病毒药物先诺欣活性成分先诺特韦的发现过程及其临床前研究结果首次在线发表于全球权威科学期刊《自然-通讯》(Nature Communications)。

图1. 《自然-通讯》(Nature Communications)发表截图
先诺欣(先诺特韦片/利托那韦片组合包装)是由先声药业(2096.HK)与中国科学院上海药物所、武汉病毒研究所联合研发的国家1类创新药,于2023年1月28日获得国家药监局附条件批准上市,用于轻中度成年患者新型冠状病毒感染的治疗,是国内首款上市的口服3CL蛋白酶抑制剂。
本次刊登在《自然-通讯》的研究结果显示,先诺特韦(SIM0417/SSD8432/simnotrelvir)对3CL蛋白酶具有强抑制活性,可广谱抑制不同新冠病毒的变异株,联合利托那韦可有效抑制Delta(德尔塔)毒株感染的转基因小鼠肺部和脑部病毒复制,在大鼠和猴体内表现出良好的药代动力学和安全性,体内外安全性评价试验中未发现遗传学毒性。
先诺特韦对不同新冠病毒变异株均有效
病毒蛋白酶是抗病毒药物研发的重要靶标,在新冠病毒出现之前,已有数十个HCV、HIV蛋白酶抑制剂先后获批上市,用于病毒感染治疗。因此,寻找新冠病毒3CL蛋白酶小分子抑制剂是抗新冠病毒药物研发的一个重要途径。
在新冠疫情初期,上海药物研究所研发团队发现已上市可口服HCV蛋白酶抑制剂博赛泼维(boceprevir)能够抑制新冠病毒3CL蛋白酶活性(IC50 = 8596 nM),于是根据它与新冠病毒3CL蛋白酶的复合物晶体结构,对其开展了药物设计与优化工作(图2),最终发现先诺特韦(SIM0417/SSD8432/simnotrelvir)具有显著的3CL蛋白酶抑制活性(IC50 = 9 nM),并且可以强效抑制新冠病毒WIV04、Delta(德尔塔)及Omicron(奥密克戎)毒株复制在细胞中的复制(EC50 分别为 26 nM、34 nM及43 nM)。
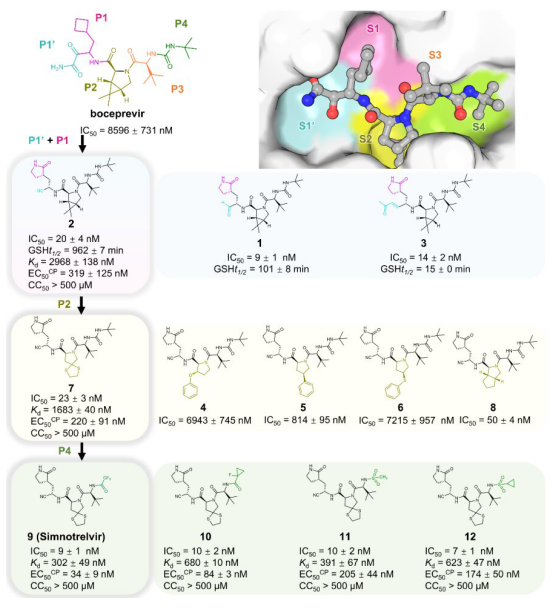
图2. 先诺特韦的理性设计与优化过程
研究结果还显示,先诺特韦对野生型和包括P132H在内的突变型3CL蛋白酶,展现出同等水平的抑制活性。先声药业研发团队在另外的研究中也发现,先诺特韦能够强效抑制近期流行的多种Omicron(奥密克戎)变异株的复制,包括BA.4、BA.5、XBB1.5和CH.1.1,其抑制活性与Omicron(奥密克戎)原始株相当。因此,先诺特韦可广谱抑制新冠病毒不同变异株的复制。此外,先诺特韦对SARS-CoV和MERS-CoV等其它6种可感染人体的冠状病毒3CL蛋白酶也有强抑制活性,提示其具有作为广谱抗冠状病毒药物使用的潜力。
先诺特韦+利托那韦
显著减轻病毒感染引起的肺部损伤
研究表明,口服先诺特韦(200 mg/kg,BID)和利托那韦(50 mg/kg,BID)可有效抑制Delta(德尔塔)毒株感染的转基因小鼠肺部和脑部的病毒复制,显著减轻病毒感染引起的肺部损伤,在损伤保护方面显著优于辉瑞的奈玛特韦(图3)。
值得一提的是,先诺特韦具有较好的血脑屏障穿透能力,在小鼠脑部可维持超过24小时的有效暴露(图4)。在更低的给药剂量下(50 mg/kg)即可完全清除小鼠脑部病毒。已有大量研究表明,新冠病毒会造成海马体损伤,引起味觉、嗅觉障碍等中枢神经症状。研究显示,先诺特韦具有清除脑部病毒的优势,提示其可在人体实现更好的脑损伤保护作用。
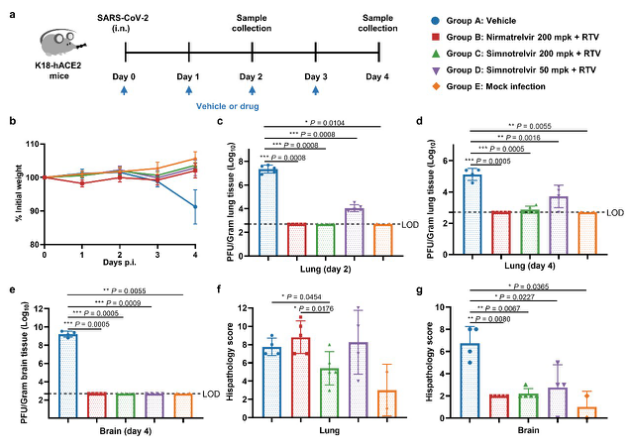
图3. 先诺特韦的小鼠体内药效评价
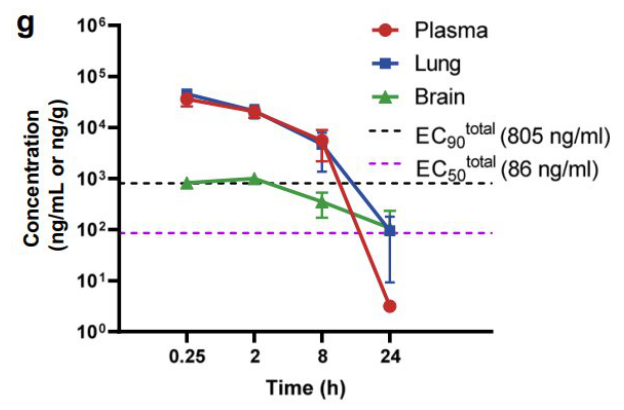
图4. 先诺特韦在小鼠组织中的分布和代谢
此外,先诺特韦的安全性也得到良好验证。研究结果表明,先诺特韦对6种人体蛋白酶、413种激酶、7个CYP酶及47个药品不良反应潜在靶点等均具有良好的选择性,且在体内外安全性评价试验中未发现遗传学毒性。
先诺特韦的发现过程突显了以结构为基础开发病毒蛋白酶抑制剂的可行性,提供了一种有效对抗人类冠状病毒的小分子疗法。本次先诺特韦临床前研究结果在《自然-通讯》(Nature Communications)的发表,体现出学术界对中国新冠药物研发的关注,以及对先诺特韦与利托那韦联用的安全性及有效性的高度认可。
目前,先诺欣已覆盖全国32个省、306个市及超2500家医疗机构,以每月数百万人份的药品可及能力,为新型冠状病毒常态化防控提供重要保障。
唐任宏博士(先声药业)、张磊砢研究员(武汉病毒所)、沈敬山研究员(上海药物研究所)和许叶春研究员(上海药物研究所)为本研究论文的共同通讯作者。蒋翔锐研究员(上海药物研究所)、苏海霞副研究员(上海药物研究所)、尚卫娟实验师(武汉病毒所)、周峰博士(先声药业)、张岩助理研究员(上海药物研究所)和赵文峰博士(上海药物研究所)为本研究论文的共同第一作者。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言