SFDA发布药品不良反应2010年度报告
2011-05-02 MedSci原创 MedSci原创
4月25日,国家食品药品监管局(SFDA)发布2010年药品不良反应(ADR)年度报告,从ADR报告总体概况、ADR统计分析、严重ADR报告统计分析等方面进行通报。从2010年ADR报告的统计数据看,我国药品安全风险仍主要集中在抗感染药和中药注射剂。因此,抗感染药和中药注射剂的安全性,仍是今后药品安全监管的重要目标,也是临床合理用药应关注的重点。 一、ADR报告总体概况 2010年
4月25日,国家食品药品监管局(SFDA)发布2010年药品不良反应(ADR)年度报告,从ADR报告总体概况、ADR统计分析、严重ADR报告统计分析等方面进行通报。从2010年ADR报告的统计数据看,我国药品安全风险仍主要集中在抗感染药和中药注射剂。因此,抗感染药和中药注射剂的安全性,仍是今后药品安全监管的重要目标,也是临床合理用药应关注的重点。
一、ADR报告总体概况
2010年ADR报告数量、新的和严重ADR报告数量保持了持续、稳定的增长趋势,报告数量和可利用性进一步提高。通过全国药品不良反应监测网络(以下简称“监测网”)报告ADR的用户继续增加,监测网络的覆盖面越来越广泛。
2010年国家药品不良反应监测中心共收到ADR报告692904份,较2009年增长8.4%。其中,新的和严重的ADR报告109991份,较 2009年增长16.2%,占报告总数的15.9%。ADR报告来源基本稳定(见图1)。2010年,每百万人口平均病例报告数量达到533份,较 2009年增加8.4%。
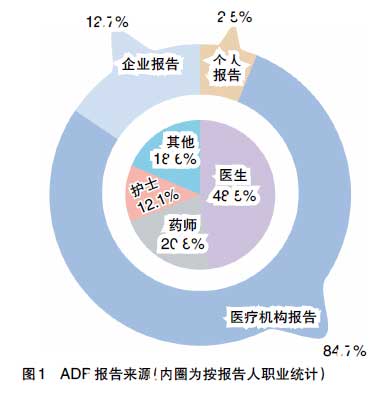
2010年通过监测网报告ADR的用户继续增加,共新增网络基层用户7170个。截至2010年12月31日,监测网在线基层用户40826个,其中医疗机构用户占53.4%,企业用户占39.0%,监测机构用户占6.4%,其他用户占1.2%。
二、ADR报告统计分析
2010年ADR报告中,患者情况、涉及药品、累及系统和不良反应表现与2009年相比无明显变化。其中,化学药和中成药涉及药品类别排名较2009年稍有差异,抗感染药ADR报告比例较2009年下降了1.6%,注射剂型仍占较高比例。
1.涉及药品的种类及排名 2010年ADR报告中,化学药涉及病例报告占总报告的86.2%,其中生物制品涉及病例报告占化学药报告的1.3%。中药涉及病例报告占总报告的13.8%,其中中成药占99.7%,饮片不足0.4%。ADR报告中,涉及化学药排名见图2。中成药排名前5位的类别分别是理血剂中活血化瘀药、解表剂中辛凉解表药、清热剂中清热解毒药、开窍剂中凉开药、补益剂中益气养阴药。
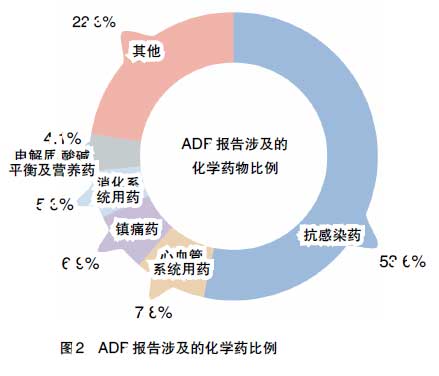
化学药报告数量排名前20位的品种中,抗感染药有15个品种,前3位分别是左氧氟沙星、阿奇霉素、头孢曲松。中成药报告数量排名前20位的品种中,中药注射剂有17个品种,前3位分别是双黄连注射剂、清开灵注射剂、参麦注射剂。
2.药品剂型和给药途径分布 2010年ADR报告的剂型分布仍以注射剂为主,占59.5%,口服剂型占37.0%,其他剂型占3.5%。化学药、中成药报告中,注射剂占有比例分别为61.0%和50.9%,与总体情况基本一致。注射剂构成高于其他剂型,仍是ADR监测的重点。
3.ADR累及系统 2010年报告的ADR中,累及系统排名前3位的是皮肤及其附件损害(占28.9%)、胃肠系统损害(占26.1%)和全身性损害(占13.6%),与2009年累及系统排名一致。注射剂型累及系统前3位与总体报告一致,口服制剂累及系统第一位为胃肠系统损害,其次为皮肤及其附件损害、中枢及外周神经系统损害。
三、严重ADR报告统计分析
2010年共收到严重ADR报告28021份,较2009年增加15.4%。严重报告比例占全部报告的4.0%。2010年严重报告的总体情况与2009年相比无明显变化。
1.涉及药品的种类及排名 2010年严重ADR报告中,化学药涉及病例报告24600余例,占全部严重报告的87.8%,其中生物制品涉及病例报告500余例,占化学药病例报告的2.3%。中药涉及病例报告近3400例,占全部严重病例报告的12.2%(见图3、图4)。
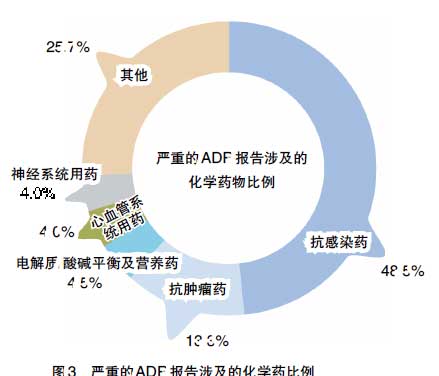
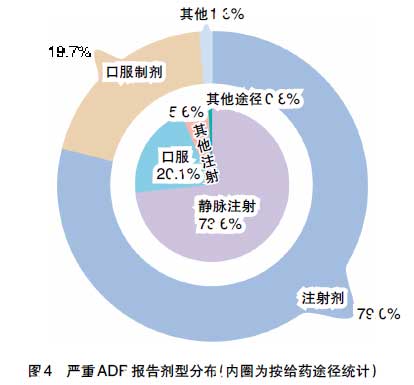
中成药严重ADR报告中,中药注射剂占87.2%,较2009年增加3.1%,提示中药注射剂依然是中药制剂的主要风险。报告数排名前5位的类别分别是理血剂中的活血化瘀药、补益剂中的益气养阴药、开窍剂中的凉开药、解表剂中的辛凉解表药、清热剂中的清热解毒药。
化学药严重ADR报告数量排名前20位的品种中,抗感染药有15个品种,前3位分别是头孢曲松、左氧氟沙星、青霉素。中成药排名前20位的品种均为中药注射剂,提示中药注射剂的风险依然很高。
2.累及系统及ADR表现 严重ADR中,累及系统排名前3位的分别是全身性损害(33.9%)、呼吸系统损害(15.0%)、皮肤及其附件损害(9.7%)。与总体报告累及系统比较,严重ADR中,呼吸系统损害和全身性损害更加突出。
化学药注射剂主要严重ADR表现多为过敏性休克、过敏样反应、呼吸困难、寒战、发热、骨髓抑制等。化学药口服制剂主要严重ADR表现多为肝功能异常、皮疹、瘙痒、白细胞减少、过敏性休克、过敏样反应、呼吸困难、胃肠道出血等。中药注射剂主要严重ADR表现多为呼吸困难、过敏样反应、过敏性休克、寒战、心悸等。中药口服制剂主要严重ADR表现多为皮疹、肝功能异常、过敏性休克、过敏样反应、间质性肾炎、腹泻等。
特别说明
该年度报告中的数据来源于监测网中2010年1月1日至2010年12月31日各地区上报的数据。与采用自发报告模式的其他国家一样,我国ADR监测网络收集的数据也存在局限性,如漏报、报告不规范、缺乏细节信息、无法计算发生率等问题。在抽取数据时,其中一些严重报告、死亡报告尚在调查和评价的过程中,所有统计结果均为数据收集情况的真实反映,并不代表评价的结果。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#不良反应#
40
#SFDA#
36
#药品不良反应#
35