Sci Adv:中国科学院施剑林团队研究提出一种基于工程和杂交微生物的肿瘤免疫治疗方法,可用于高选择性和超声可控的肿瘤催化治疗
2024-11-04 iNature iNature 发表于上海
该研究提出了一种基于工程和杂交微生物的肿瘤免疫治疗方法,可用于高选择性和超声可控的肿瘤催化治疗。
生物疗法是一种新兴的抗肿瘤方式,具有选择性的活微生物和有效的治疗方法。然而,原始微生物对肿瘤的治疗作用有限。微生物与多功能纳米催化剂的杂交对实现肿瘤强化催化治疗具有重要意义。
2024年10月30日,中国科学院施剑林,霍敏锋共同通讯在Science Advances 在线发表题为“Hybridized and engineered microbe for catalytic generation of peroxynitrite and cancer immunotherapy under sonopiezo initiation”的研究论文。该研究提出了一种基于工程和杂交微生物的肿瘤免疫治疗方法,可用于高选择性和超声可控的肿瘤催化治疗。
研究利用一氧化氮合酶(NOS)工程的大肠杆菌菌株MG1655 (NOBac)与声压催化BaTiO3纳米颗粒(BTO NPs)杂交,实现了高效的肿瘤靶向积累和抗肿瘤治疗。超声照射下,BTO NPs压电催化反应产生的超氧阴离子可立即与NOBac产生的一氧化氮(NO)发生级联反应,生成高度氧化的过氧亚硝酸盐ONOO−,产生强大的肿瘤压电催化治疗效果,同时促进显著且持续的抗肿瘤免疫激活。

生物疗法是一种新兴疗法,通过利用活细胞的设计可控性、多功能性和复杂敏感性的优势,用于多种医学目的,在生物医学工程的前沿治疗持续性或慢性疾病。生物疗法利用天然或生物工程微生物、酵母和真核生物,它们能够产生治疗物质或试剂,调节病理微环境以治愈疾病。例如,恶性肿瘤具有复杂的遗传和分子微环境,包括特征性的缺氧特征、积极的血液供应、强烈的免疫抑制以及从邻近组织捕获营养的能力。给药后,这些活微生物可以选择性地在肿瘤区域内定植和增殖,表现出明显的器官选择性,肿瘤/肝脏积聚比高于1000:1,赋予了活微生物与专性或兼性厌氧菌的肿瘤靶向性能。随着合成生物学的进步,这些活的微生物可以进一步进行基因改造,分泌治疗剂来干预肿瘤的进展。例如,基因工程后,在大肠杆菌表面表达的组蛋白A使这些微生物能够靶向癌症细胞。当给予十字花科蔬菜饮食时,微生物分泌的黑芥子酶会有效地将硫代葡萄糖苷转化为萝卜硫素,产生抗癌作用,从而产生令人满意的肿瘤抑制效果。有研究构建了工程化的表皮葡萄球菌,该葡萄球菌可以在肿瘤组织定植后表达肿瘤抗原,特异性地启动针对黑色素瘤的T细胞反应。鼠伤寒沙门氏菌菌株也可以被改造为分泌创伤弧菌鞭毛蛋白B,在不同类型的肿瘤中诱导强烈的免疫反应。这些研究使活微生物成为生物医学治疗最有前景的候选者。
活微生物与合成成分的杂交可以进一步为目标区域提供多种治疗功能,与未杂交的活微生物相比,可以实现多种相互作用,带来前所未有的治疗机会。例如,有研究将含有红细胞(RBC)的超顺磁性氧化铁纳米颗粒与大肠杆菌MG1655结合,以获得生物杂化微抗体。凭借细菌的自主和推进性能,这些微型吸管可以在磁场的引导下将货物运送到指定位置。光激活热疗可以消除过多的细菌。此外,在大肠杆菌中设计了产生一氧化氮(NO)的酶,并将其与光催化氮化碳结合用于光引发的肿瘤治疗,从而抑制了80%的肿瘤生长。然而,具有光控制的杂交活微生物存在组织穿透不足的缺点,从而降低了它们的治疗效果。超声(US)是一种常规的诊断和治疗辐射源,适用于多种应用,包括成像、溶栓、热疗和声动力学治疗。在非敏感分子或纳米材料存在的情况下,可以产生超氧阴离子自由基。然而,这些自由基可以被超氧化物歧化酶迅速消除,从而破坏声动力疗法的治疗效果。过氧化亚硝酸盐(ONOO-)是一种相对长寿命的活性氮物种(RNS),可以诱导对肿瘤的强效细胞杀伤作用,这是由超氧阴离子自由基(O2-)和一氧化氮(NO)之间的自由基反应自然产生的。通过直接氧化或自由基介导的氧化反应,ONOO-表现出比羟基自由基等活性氧(ROS)更高的氧化电位。尽管NO和O2−之间的反应具有较大的反应常数(~1010 M−1 s−1),但在生理条件下,这些物种很容易被氧肌红蛋白和超氧化物歧化酶消除。因此,ONOO-的持续瘤内生成对有效的肿瘤治疗非常有吸引力。
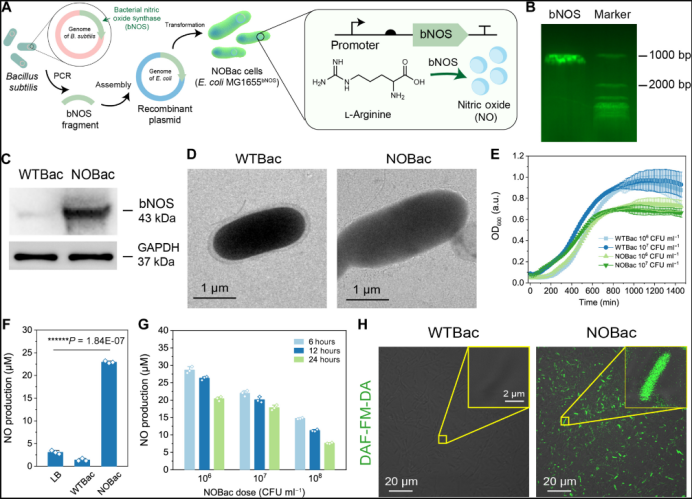
NOBac的构建与表征(图源自Science Advances )
研究最初用细菌一氧化氮合酶(bNOS)对靶向大肠杆菌MG1655微生物的肿瘤进行基因工程改造,以形成产生NO的活微生物NOBac。然后将NOBac与声压敏感的BaTiO3纳米粒子(BTO NP)杂交,通过声压催化下BTO NP产生的超氧阴离子自由基与NOBac产生的NO气体分子之间的反应,实现ONOO−的产生。同时,在肿瘤破坏后,BTONPs@NOBac可以激活肿瘤区域内的先天性和适应性免疫反应,通过杂交工程微生物呈现出优于肿瘤治疗的策略。
参考消息:
https://www.science.org/doi/10.1126/sciadv.adp7540
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#肿瘤免疫治疗# #杂交微生物#
15