Front Immunol:用于天疱疮研究的人桥粒蛋白3 ec5结构域特异性单克隆抗体的质量控制鉴定
2024-10-30 从医路漫漫 MedSci原创 发表于上海
寻常型天疱疮(PV)是一种危及生命的自身免疫性水疱疾病,主要由IgG自身抗体(auto-abs)对抗钙粘蛋白型黏附分子desmoglin (Dsg) 1和3引起。
天疱疮是一种潜在致命的IgG自身抗体(auto-ab)驱动的自身免疫性疾病,影响粘膜和皮肤。天疱疮的auto-ab反应是多克隆的。虽然免疫球蛋白4 (IgG4)抗体主要存在于活动性天疱疮患者的血清中,但抗原特异性IgG1与IgG2和IgG3经常与起始或缓解期相关。在单克隆抗体和致病性抗体中,切换IgG1和IgG4亚类并不直接影响其抗原结合或致病性。

天疱疮可分为两种主要亚型,取决于所涉及的自身抗原谱。叶状天疱疮的特征是桥蛋白1 (Dsg1)特异性自身抗体,可诱导表皮角膜下形成水疱。然而,在寻常型天疱疮(PV)中,主要是dsg3特异性自身抗体诱导粘膜基底层和基上层的棘层溶解,导致疼痛和愈合缓慢的疮。桥粒蛋白属于桥粒体钙粘蛋白,其主要功能赋予表皮角化细胞粘附。在人类中,不同的基因编码四种桥粒蛋白(Dsg1-Dsg4)。它们包括5个细胞外钙粘蛋白结构域(EC1- ec5),一个单次跨膜结构域(TMD)和一个与桥粒体斑块蛋白相关的细胞内结构域。Dsg3的EC1- ec3结构域与Dsg1的EC1- 3高度同源(75-80%同源性)。一些研究表明,大多数天疱疮特异性auto-ab特异性结合Dsg3的n端EC1结构域,该结构域也作为同源和异源性相互作用的主要介质。dsg3特异性IgG反应性与疾病活动性相关,大约80%的PV患者表现出针对EC1-2结构域的血清IgG,其次是EC3(15%)、EC4(21%)和EC5(17%)。
最初由Mahoney、Amagai和Stanley提出的粘粒蛋白补偿理论认为,Dsg3补偿了粘膜中Dsg1的损失,只导致临床活跃的皮肤侵蚀。相反,由于Dsg1在粘膜表皮的低表达,抗Dsg3 IgG导致粘膜表皮粘附受损,不能完全补偿Dsg3粘附的损失。尽管Dsg补偿理论很好地反映了天疱疮的临床特征,但最近越来越多的研究表明,更多样化的抗原特异性图景可能有助于个体抗体的发病机制。这强调了在制定治疗策略时需要更高程度的个性化医疗,将auto-ab概况考虑在内。此外,致病性和非致病性粘粒蛋白特异性IgG之间的相互作用可能潜在地增加协同效应,例如,通过引起p38依赖性抗原聚类。虽然大多数抗ec1或-EC2抗体由于其致病性直接导致临床表型,但针对EC3-5的抗体主要被认为是“协同和半致病性”自身抗体。在体外和体内研究中,通常使用ec1特异性致病抗体,如广泛分布的小鼠单克隆IgG抗体AK23。在Hudemann等人的研究中,描述了一种新的ec5特异性抗dsg3 ab (2G4)。在这项研究中,全面的证据表明,与Dsg3的EC5结构域结合会导致人和小鼠皮肤表皮粘附丧失,并伴有脱落毒素,挑战了仅针对Dsg3的EC1亚结构域的IgG是致病的概念。进一步的机制分析显示,在角蛋白收缩和桥粒数量减少方面的作用与AK23相似,而只有AK23介导的作用可以通过抑制Src而改善,而2G4则不能。
在天疱疮等研究领域,由于用于离体和体内研究的工具种类有限,实验室的质量保证至关重要。我们认为PV样本或抗体的标准化分布对于可靠和准确的临床和临床前结果至关重要。本研究的目的是建立和验证协调活动,以指导和控制2G4 IgG的产生,作为天疱疮研究的潜在中心工具,允许在不同的实验室地点和时间内产生恒定质量的可比数据。因此,我们实施了一个分析管道,包括标准分子分析(凝胶电泳,ELISA,质谱),然后使用间接免疫荧光对猴子食管和人体组织进行常规诊断分析,并通过单层解离测定(MDA)验证致病性,以确保功能性产品允许下游临床和临床前样品的标准化分析。这种质量控制机制的引入将有可能协调天疱疮的研究。
方法:之前,我们已经介绍了一种名为2G4的新型Dsg3 ec5结合抗体,它可能成为许多PV相关分析的优越工具。本研究的目的是开发一种质量控制的生产和验证过程,以允许I)持续的质量改进,以及II)在各种天疱疮检测中,每批生产中病原抗原特异性结合的验证和可理解的整体质量。
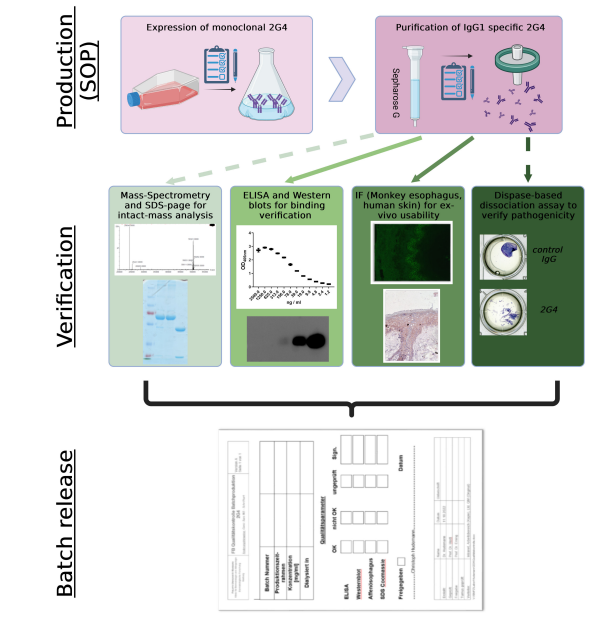
简化受控2G4 IgG的生产和验证流程
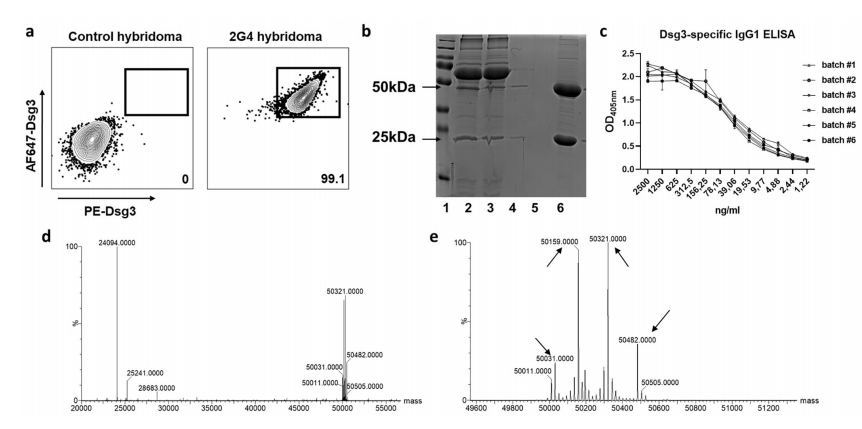
杂交瘤的鉴定和抗体的大小和结构验证。(A) 2G4杂交瘤细胞系代表性流式细胞术。细胞被门控为生命单线CD138+ IgG+, dsg3特异性细胞被鉴定为Dsg3-AF647和Dsg3-PE双染色。(B)举例还原SDS-page用于纯度分析。Lane 1=标记,2/3=琼脂糖结合前后的培养基,4/5=流动槽,6=洗脱(IgG纯度>90%)。(C) Dsg3酶联免疫吸附试验,采用稀释系列2G4批次#1-6(光密度[OD]在405 nm)。(D)质谱分析证实了单克隆抗体的存在。用二硫苏糖醇还原导致重链和轻链分离。(E)放大重链显示箭头所示的4个糖基化位点。
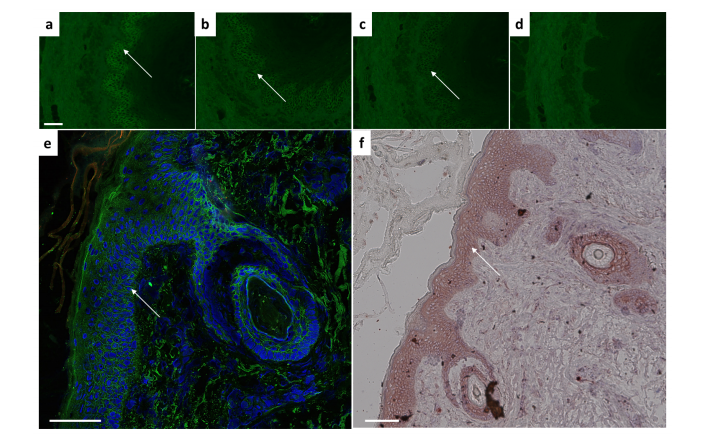
用猴子食道或人体皮肤切片进行离体结合验证。以2G4为一抗,在(A) 1:1000, (B) 1:5000, (C) 1:10 000(箭头所示)稀释时,可见猴食管特征性细胞间上皮染色。(D)对照样本为阴性。(E)冷冻切片(IgG绿色,DAPI蓝色)或(F)石蜡包埋切片上可见的人体皮肤的特征基底和直接基底上皮肤层。比例尺= 100µm。
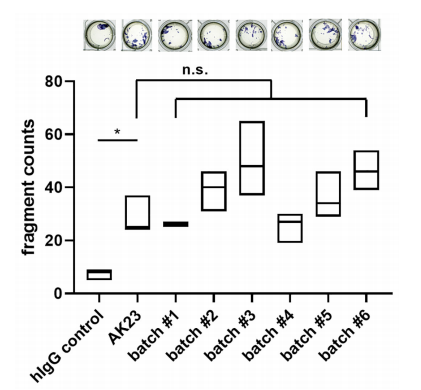
批依赖的2G4分析证实了基于桥粒破坏的类似致病性。用2G4、AK23或人对照IgG处理人htert永生化角质形成细胞(均以75µg/ml处理24 h)进行单层解离实验,n= 3次/批。
结果:建立了基于标准化操作程序的工作流程。这包括纯度和体外结合能力(SDS-page,直接和间接免疫荧光)作为主要参数的验证,以及质谱分析的大小和单层解离实验的离体致病性。
结论:我们在这里提出了一个广泛的逐点质量控制的IgG生产方案,这将作为PV研究中标准化抗体评估的基础。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#单克隆抗体# #天疱疮# #人桥粒蛋白#
50