Nat Biomed Eng:CRISPR今年没拿诺奖,但它离人类基因疗法又近了一步
2017-10-03 佚名 药明康德
毫无疑问,CRISPR-Cas9基因编辑系统是本世纪以来生物技术领域的最大突破。尽管昨日的诺贝尔生理学或医学奖授予了“昼夜节律的分子机制”,但这并没有浇灭CRISPR-Cas9支持者的热情。他们相信,诺奖荣誉也许会迟到,但不会缺席。
一些冷静的粉丝则指出,这一突破性技术想要问鼎诺奖,或许还要等上一些时候。诚然,CRISPR-Cas9书写了基因编辑技术的光辉新篇章,但它要从实验室的细胞与动物走入人体,还有很长的路。其中,研究人员们亟需解决的一个问题,是如何让CRISPR-Cas9系统送入人体,让它生效。
许多人或许曾有过用CRISPR-Cas9基因编辑技术任意修改人类基因,从根源解决疾病的梦想。但真正的治疗在操作上远没有这么简单。从机理上看,CRISPR-Cas9系统有两种潜在的基因编辑和治疗手段,一种是非同源的,它能永久“沉默”掉致病的基因;另一种是同源的,它能将错误的基因改写成正常的基因。显然,后者的应用潜力更为广泛。
但基于同源编辑的疗法需要同时将Cas9蛋白、gRNA、以及待插入基因组的供体DNA引入需要编辑的区域。在细胞实验中,科学家们把腺相关病毒(AAV)改造成了“快递员”,让它们来递送这些分子。然而,许多人体内对腺相关病毒具有免疫力。这就好像门卫不让快递员进入小区,CRISPR-Cas9系统也就失去了用武之地。此外,基于腺相关病毒的递送技术还有可能带来预料外的脱靶效应,额外提高基因编辑的风险。因此,想要在人体内真正用上CRISPR-Cas9技术,我们还需要开发一种全新的递送手段。
加州大学伯克利分校的一项研究有望解决这一难题。一支包括CRISPR技术先驱Jennifer Doudna教授在内的团队开发了一种全新的纳米颗粒,用来代替应用潜力有限的腺相关病毒。这一成果今日在线发表在了《自然》子刊《Nature Biomedical Engineering》上。
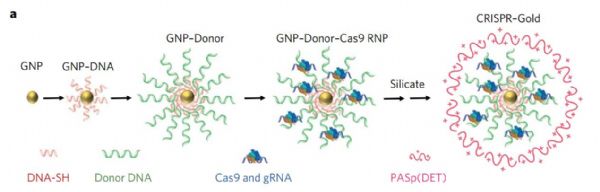
在这篇论文里,研究人员提到,他们将纳米金颗粒作为核心,让它与不同的CRISPR组件相结合。这样一来,无论是Cas9蛋白、gRNA、还是供体DNA,都能紧紧靠近纳米金颗粒,一同递送。随后,研究人员们又在外部套上一层具有保护性的聚合物,让它更为稳固。
按设想,在需要基因编辑的部位,研究人员可以特异性地注入具有编辑功能的纳米颗粒。这些颗粒会被细胞内吞,并在细胞体内释放出CRISPR的关键组件。这些组件会进一步进入细胞核,进行有效而安全的基因编辑。
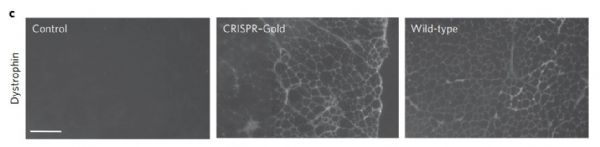
为了验证这一颗粒的实际临床应用价值,研究人员们又进一步用它去治疗罹患杜氏肌营养不良症的小鼠。这些小鼠体内的mdx基因出现了突变,无法正常合成抗肌萎缩蛋白(dystrophin)。让研究人员们感到鼓舞的是,在使用纳米颗粒递送CRISPR-Cas9基因编辑系统后,这些小鼠mdx基因的突变得到了修复,它们也能够继续表达抗肌萎缩蛋白。此外,这些小鼠肌肉组织内的脱靶效应也降到了最低。这些成功的数据为我们打开了一扇大门,门的另一侧,是通往人体应用的康庄大道。
“在这篇论文中,我们通过基于同源修复的方法,能把错误的基因修正成为正确的野生型,”本论文的主要负责人之一Niren Murthy教授说道:“目前,(针对杜氏肌营养不良症的)另一种疗法是‘外显子’跳跃,让你跳过一些错误的外显子,使得这个蛋白依旧可以被生产。但这些蛋白的功能不如野生型的蛋白。”
“为了实现同源修复,你必须给细胞提供Cas9蛋白、gRNA、以及一大段模板DNA,”该研究的另一名主要负责人Irina Conboy教授说道:“它们必须在同一个时间出现在同一个地点,才能起作用。我们的纳米颗粒系统就能同时将三个关键成分递送到需要它们的位置。”
正如我们相信CRISPR-Cas9技术终能斩获诺贝尔奖一样,我们也坚信它将在人体中得到广泛的应用。本次研究让我们离实现这个目标又近了一步!未来,我们期待听到更多令人振奋的好消息。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#Bio#
35
#Nat#
27
#Eng#
38
#CRISPR#
25
#诺奖#
34
#Med#
21
学习了新知识
56