ESMO 2022:Trastuzumab Deruxtecan在转移性胃癌/GEJ癌中维持临床获益(DESTINY-Gastric02研究)
2022-09-12 MedSci原创 MedSci原创
来自2期DESTINY-Gastric02研究(NCT04014075)的更长期随访数据显示,fam-Trastuzumab Deruxtecan-nxki(Enhertu)在接受基于曲妥珠单抗(赫赛
来自2期DESTINY-Gastric02研究(NCT04014075)的更长期随访数据显示,fam-Trastuzumab Deruxtecan-nxki(Enhertu)在接受基于曲妥珠单抗(赫赛汀)方案治疗的局部晚期或转移性HER2阳性胃或胃食管交界处(GEJ)腺癌患者中,继续表现出临床获益和可耐受的安全性特征。

在中位随访10.2个月(0.7-22.1)时,79例接受治疗的患者中经证实的客观缓解率(ORR)为41.8%(95%CI:30.8%-53.4%)。4例患者(5.1%)报告完全缓解,29例患者(36.7%)报告部分缓解。中位缓解持续时间为8.1个月(95%CI,5.9-无法估计)。主要分析的疾病控制率维持在81.0%(95%CI,70.6%-89.0%)。
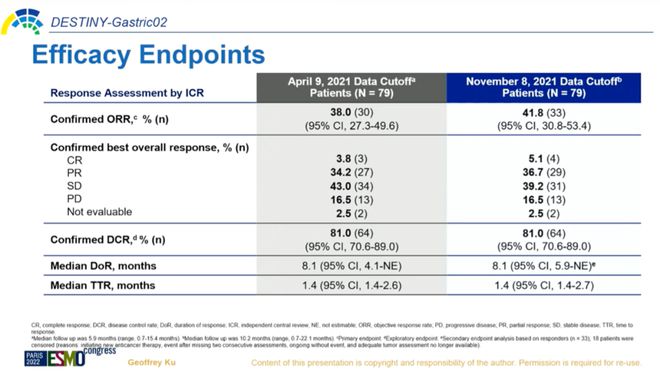
“DESTINY-Gastric02的主要结果是基于2021年04月09日的数据截止日期,它证明了当时确认的ORR为38.0%[95%CI,27.3%-49.5],主要分析达到了主要终点,即确认的ORR。” 美国纪念斯隆凯特琳癌症中心的Geoffrey Y. Ku博士在介绍研究结果时表示。
他强调,与之前报告的数据相比,该药物的临床获益得以维持。“缓解往往是持久且迅速发生的,中位至缓解时间为1.4个月[95%CI,1.4-2.6]。”Ku说。
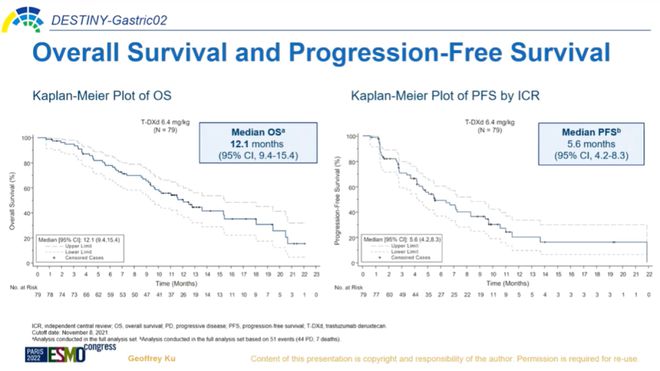
更新的生存期数据显示,接受Trastuzumab Deruxtecan治疗的患者的中位总生存期为12.1个月(95%CI,9.4-15.4),中位无进展生存期为5.6个月(95%CI,4.2-8.3)。
安全性特征与Trastuzumab Deruxtecan的既定特征基本一致。中位治疗持续时间为4.3个月(0.7-22.1),最常见的治疗中出现的不良反应(TEAE)为恶心(67.1%)、呕吐(44.3%)和疲乏(41.8%)。
55.7%的患者报告3级或以上TEAE,30.4%与药物相关。严重TEAE的发生率为41.8%,其中12.7%与Trastuzumab Deruxtecan相关。导致停药、剂量降低或死亡的TEAE发生率分别为19.0%、21.5%和13.9%。导致10例患者中止治疗、14例患者降低剂量和2例患者死亡的药物相关TEAE。2例死亡均与判定的间质性肺疾病(ILD)/肺炎相关,1例死亡发生在开始给药后171天,第2例发生在353天后。
2例患者发生1级判定的药物相关ILD/肺炎,4例患者发生2级判定的药物相关ILD/肺炎。至发作的中位时间为80.5天(42-344天),中位持续时间为36天(15-142天)。
患者报告结局方面(数据截止日期:2021年4月9日),研究者使用了EQ-5D VAS以及FACT-Ga进行评估,评估至用药第7个周期。从数据上可以看到,用药至第7个周期内,患者的生活质量没有出现明显的下降。总体来说,T-DXd显示出持续的临床获益以及可接受的安全性。
DESTINY-Gastric02是一项非随机研究,入组了经病理学证实的胃癌或GEJ癌患者,这些患者有中心证实的HER2阳性疾病,定义为免疫组化(IHC)3+或IHC2+/原位杂交阳性。患者必须在接受含曲妥珠单抗的治疗方案期间发生疾病进展,ECOG体能状态为0或1。受试者接受6.4mg/kg Trastuzumab Deruxtecan静脉给药,每3周一次。
79例入组患者既往报告的基线特征显示,该人群的中位年龄为60.7岁(20.3-77.8),大多数患者的ECOG体能状态为1(63.3%)。HER2表达主要为IHC 3+(86.1%),12.7%为IHC 2+/ISH+疾病,1.3%不可评价。在组织学方面,34.2%的患者患有胃癌,65.8%的患者患有GEJ.2大多数患者有2个或2个以上的转移部位(93.7%)。自诊断的中位时间为14.2个月(3.6-88.5)。
该试验是一项在西方患者中开展的验证性研究,在获得2期DESTINY-Gastric01(NCT03329690)阳性数据后开展,该研究是一项随机研究,在既往接受过至少2种治疗方案(包括曲妥珠单抗、氟尿嘧啶和含铂化疗)后发生进展的患者中,比较Trastuzumab Deruxtecan与医生选择的化疗。该试验在日本和韩国入组患者。该结果支持FDA于2021年1月批准Trastuzumab Deruxtecan用于既往接受过含曲妥珠单抗方案治疗的患者。
DESTINY-Gastric04(NCT04704934)是一项在接受含曲妥珠单抗方案治疗期间或治疗后发生进展的HER2阳性胃癌或GEJ癌患者中,比较Trastuzumab Deruxtecan与ramucirumab(Cyramza)+紫杉醇的III期试验。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#EST#
0
#转移性胃癌#
40
#mAb#
51
#临床获益#
38
#GAS#
61
#AST#
51
#TRA#
49
#deruxtecan#
34
#TEC#
62
#gastric#
55