Redox Biol 山东大学齐鲁医院陈玉国/徐峰/薛丽教授团队揭示ALDH2调控动脉粥样硬化进展的新机制
2024-09-12 论道心血管 论道心血管 发表于上海
山东大学齐鲁医院团队发表研究,揭示 ALDH2 活性缺陷致巨噬细胞极化促动脉粥样硬化机制,为防治提供新思路及靶点。
动脉粥样硬化(AS)是一种慢性炎症性疾病,是心血管事件的重大危险因素,威胁人类健康。2024年8月17日,山东大学齐鲁医院陈玉国/徐峰/薛丽教授团队在Redox Biology上发表了题为“ALDH2 deficiency augments atherosclerosis through the USP14-cGAS-dependent polarization of proinflammatory macrophages”的研究论文。该论文为陈玉国教授团队醛代谢紊乱系列研究的新原创性成果,揭示了ALDH2活性缺陷致毒性醛4-HNE大量积聚,引发巨噬细胞极化和炎症反应促进AS病变发生和发展,为ALDH2 rs671突变增加心血管疾病风险提供了新解释和新依据;并且鉴定出去泛素化酶USP14对cGAS的泛素化调控为其中关键机制,为AS防治提供了新思路及靶点,在ALDH2 rs671突变人群中尤为重要。

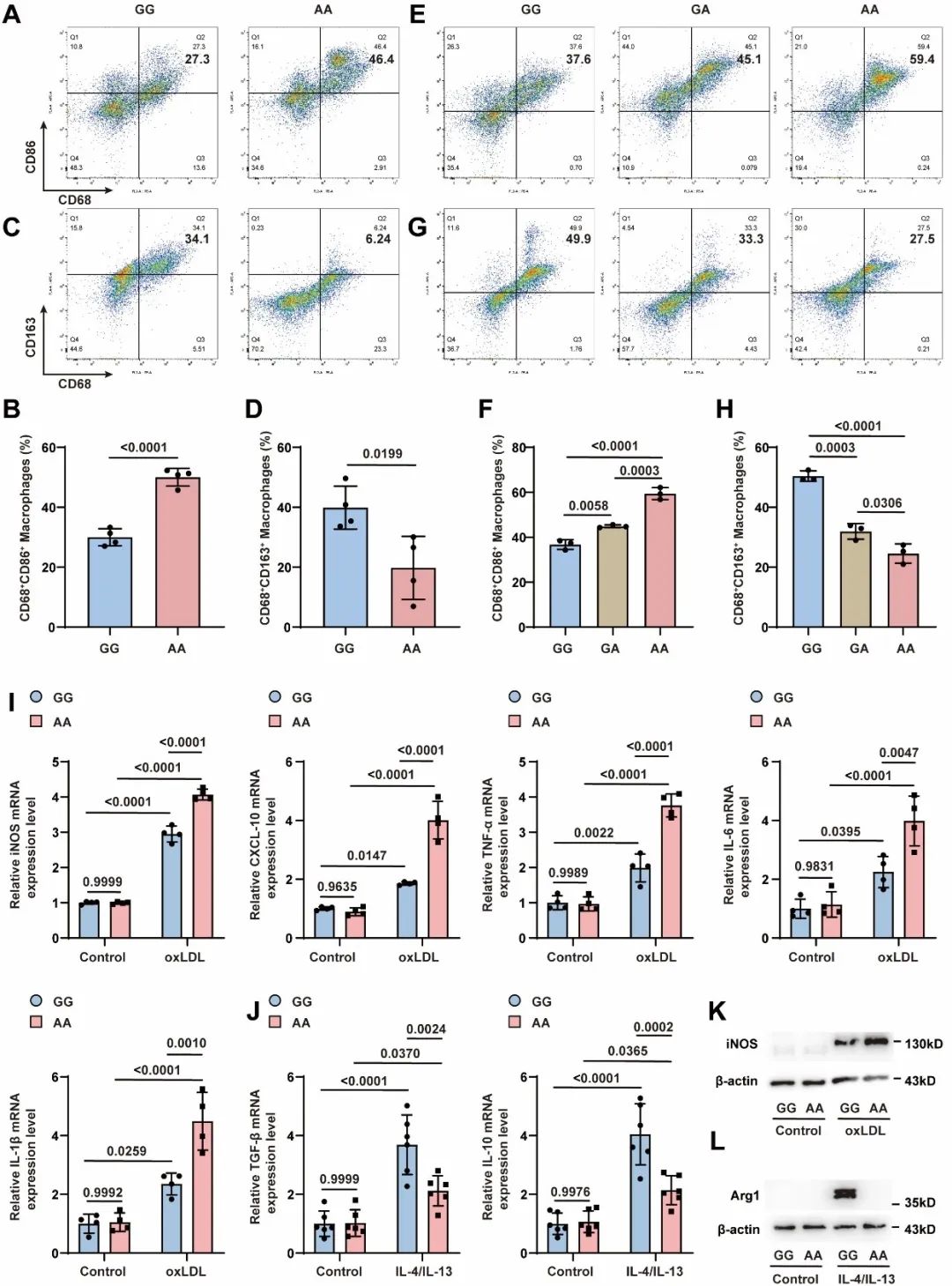
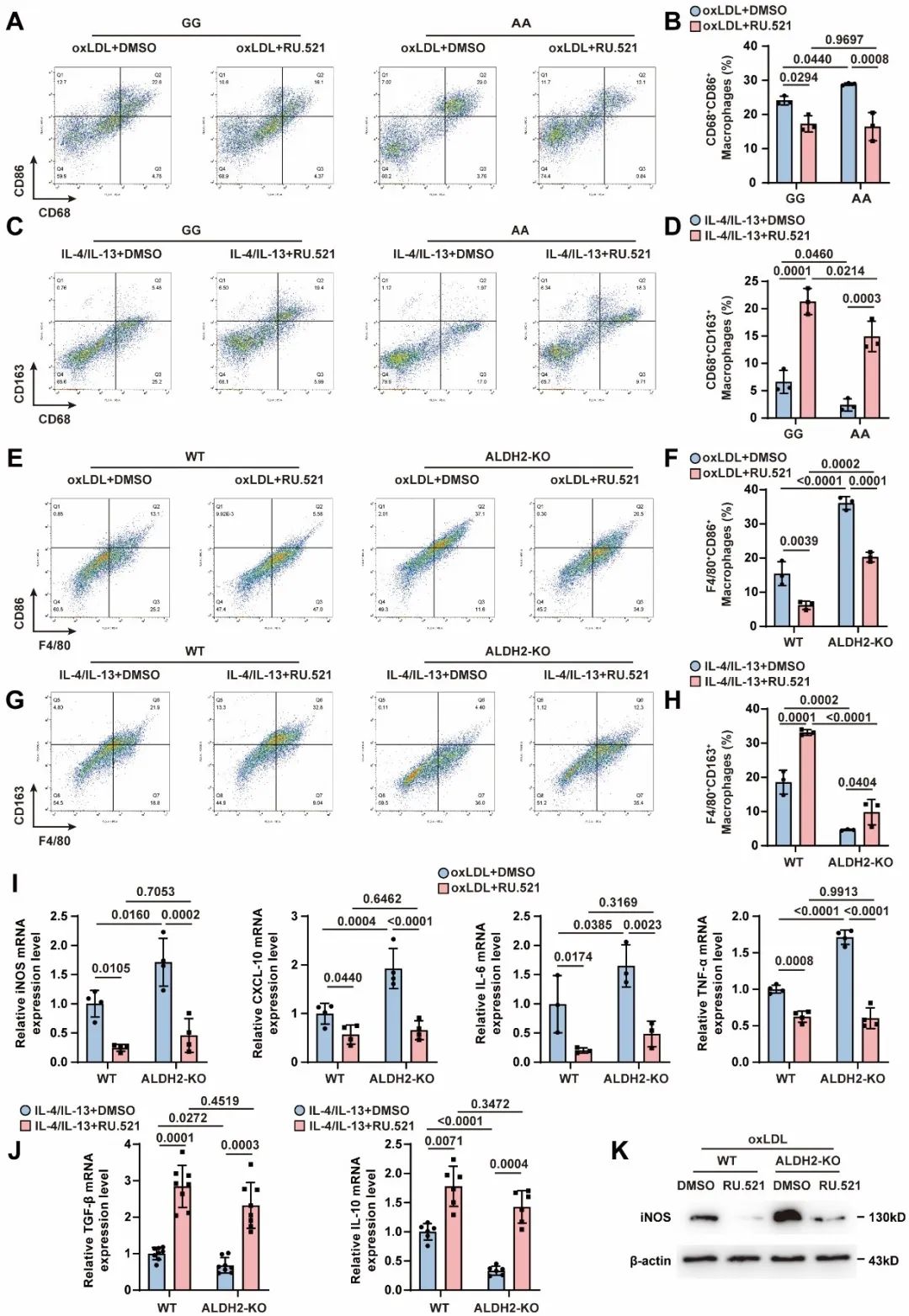
为明确ALDH2 rs671突变在巨噬细胞极化中的作用,研究者通过诱导ALDH2 rs671突变个体外周血和ALDH2-KO小鼠骨髓来源单核巨噬细胞极化,发现ALDH2基因突变或者缺失可促进巨噬细胞向M1型(促炎)极化,抑制其M2型(抗炎)极化。
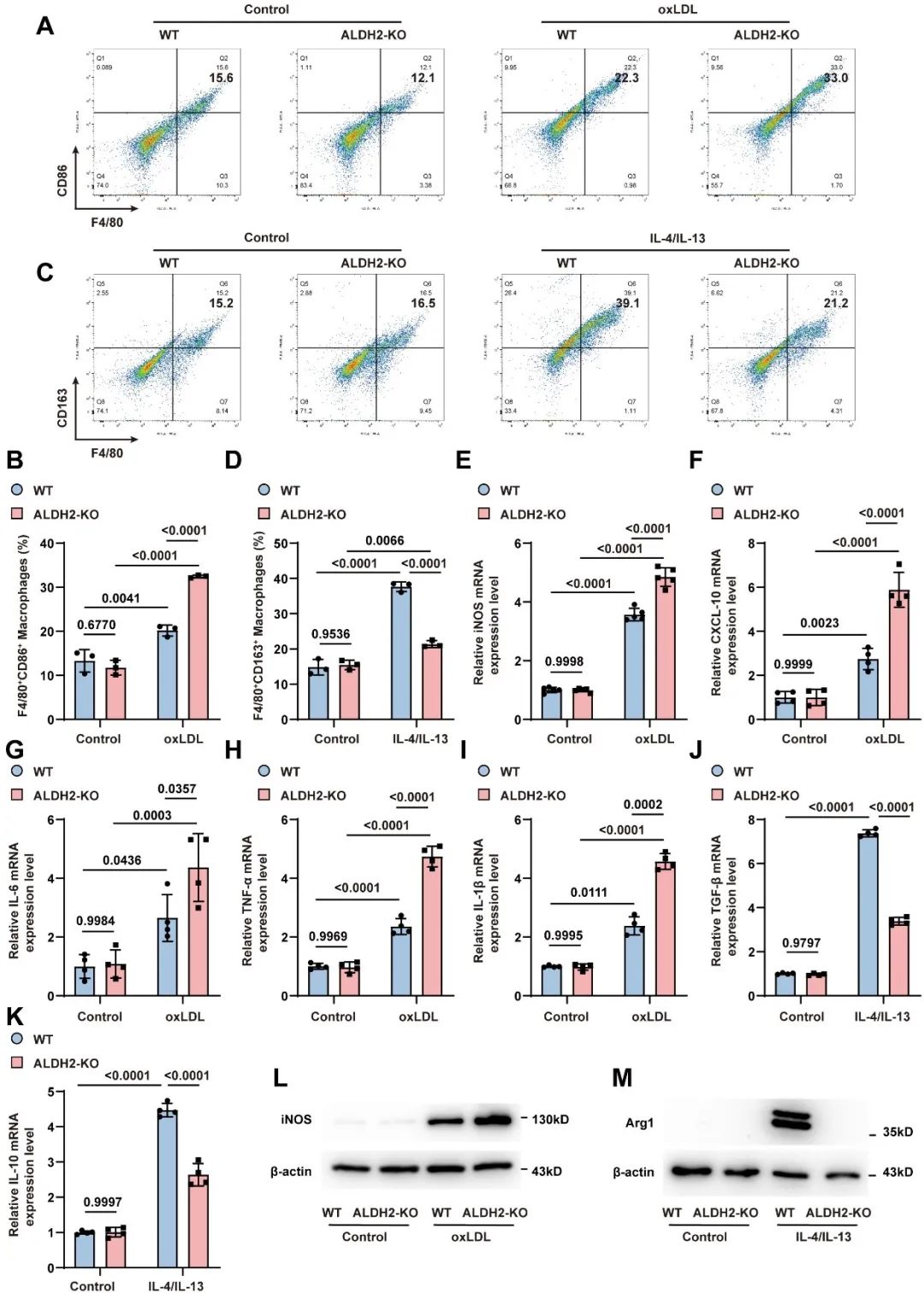
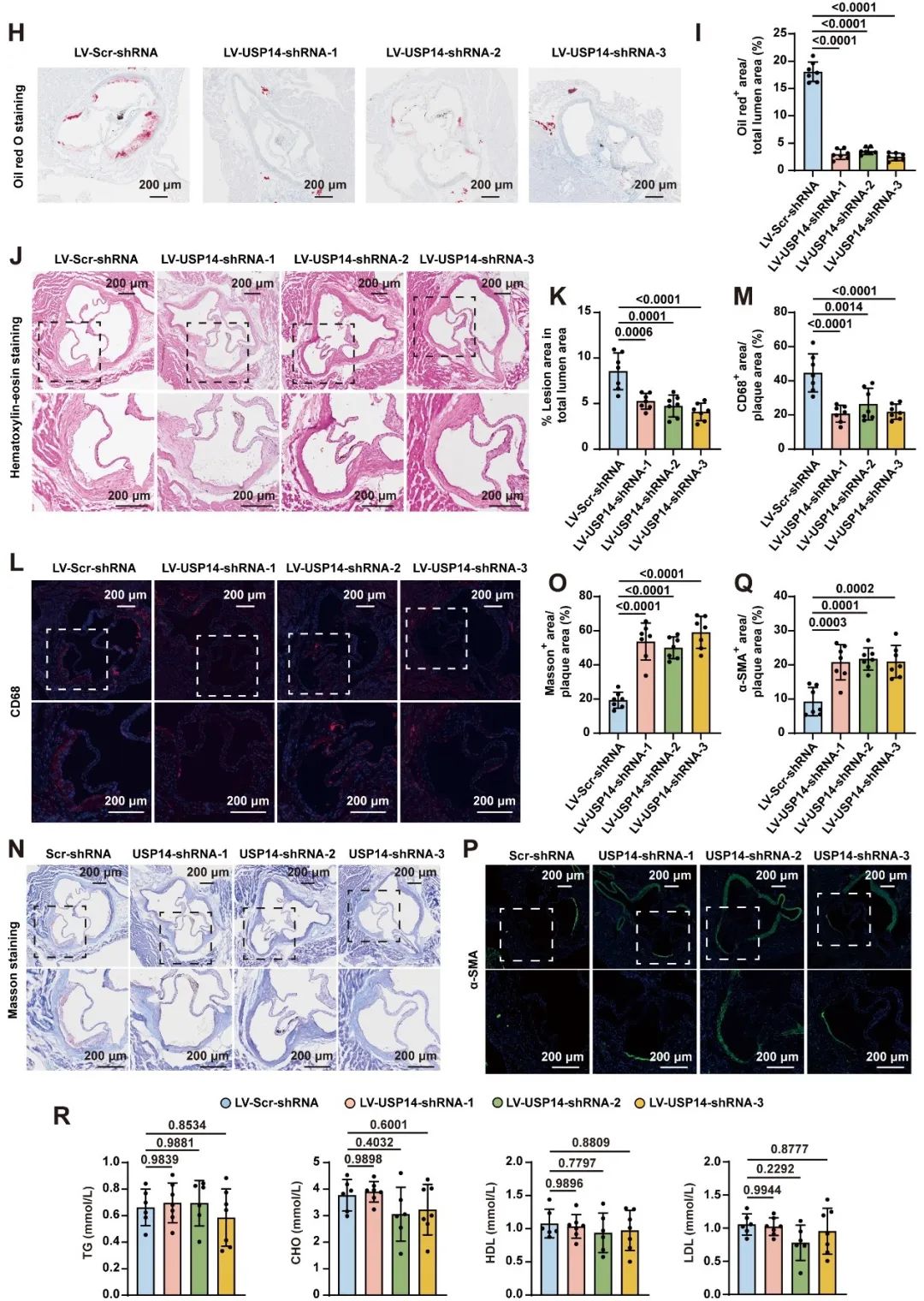
为进一步明确ALDH2在巨噬细胞炎性极化和AS中的作用,研究者构建了小鼠骨髓移植模型,分别将ALDH2-/-ApoE-/-小鼠和ApoE-/-小鼠的骨髓移植到ApoE-/-小鼠体内,随后进行为期16周的普食或高脂喂养,发现移植了ALDH2-/-ApoE-/-小鼠骨髓的小鼠中,斑块生长和促炎巨噬细胞极化明显增强。这表明ALDH2通过调控巨噬细胞极化参与AS进展。
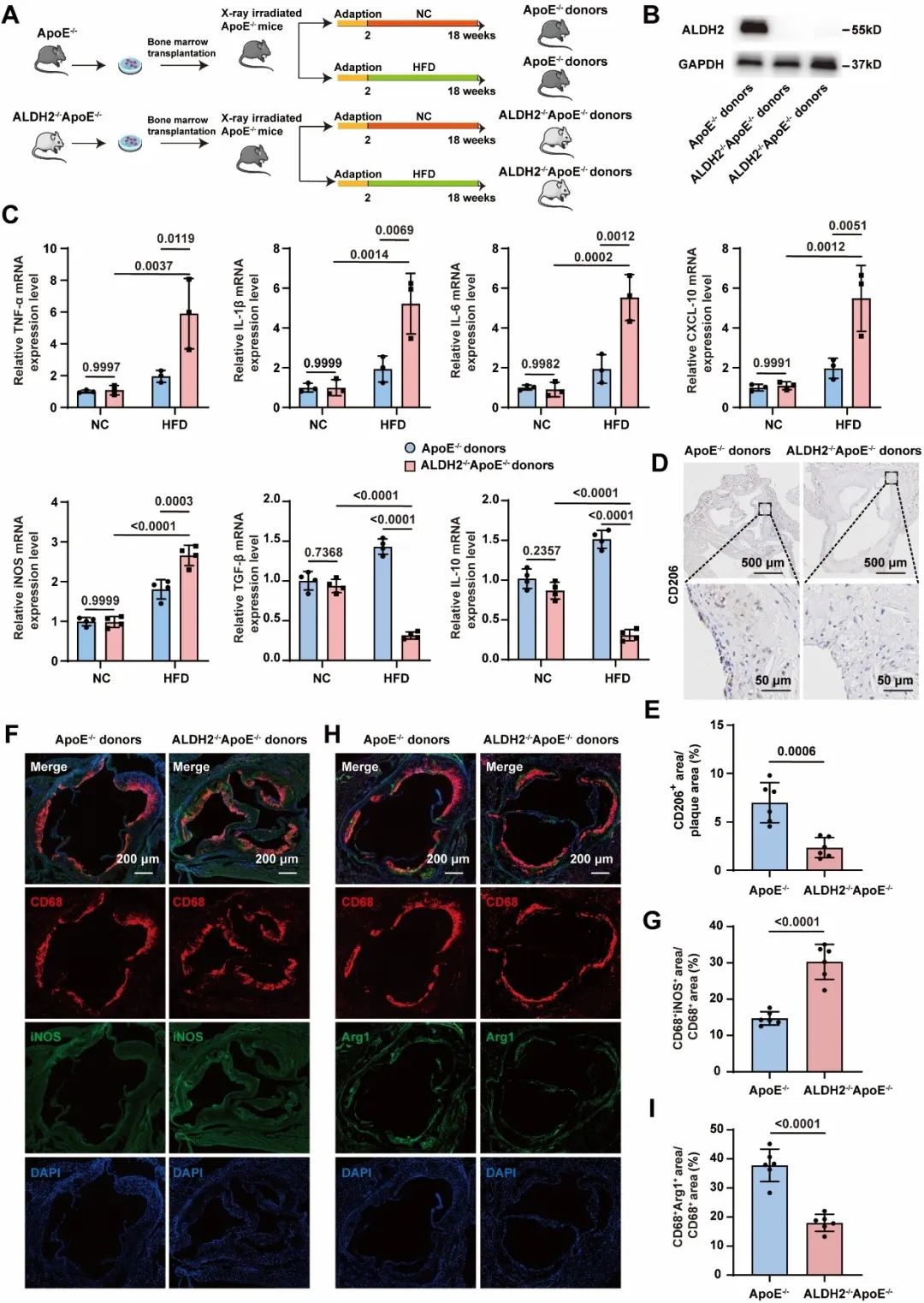
cGAS-STING信号通路在先天免疫反应中具有重要作用,除抵抗致病性感染外,还参与多系统的非感染性疾病。在心血管疾病中,病变部位的细胞损伤可导致细胞内DNA释放,激活该通路。研究者发现,cGAS-STING通路在人类和小鼠AS病变巨噬细胞中被激活。值得注意的是,相较于移植ApoE-/-骨髓的ApoE-/-小鼠,移植了ALDH2-/-ApoE-/-骨髓的ApoE-/-小鼠主动脉中cGAS-STING信号通路被进一步激活,加剧了斑块进展。此外,特异性抑制cGAS-STING通路可降低促炎型巨噬细胞比例,增加抗炎型巨噬细胞比例。这些结果表明,cGAS-STING通路是参与ALDH2调控巨噬细胞表型转化的重要分子机制。
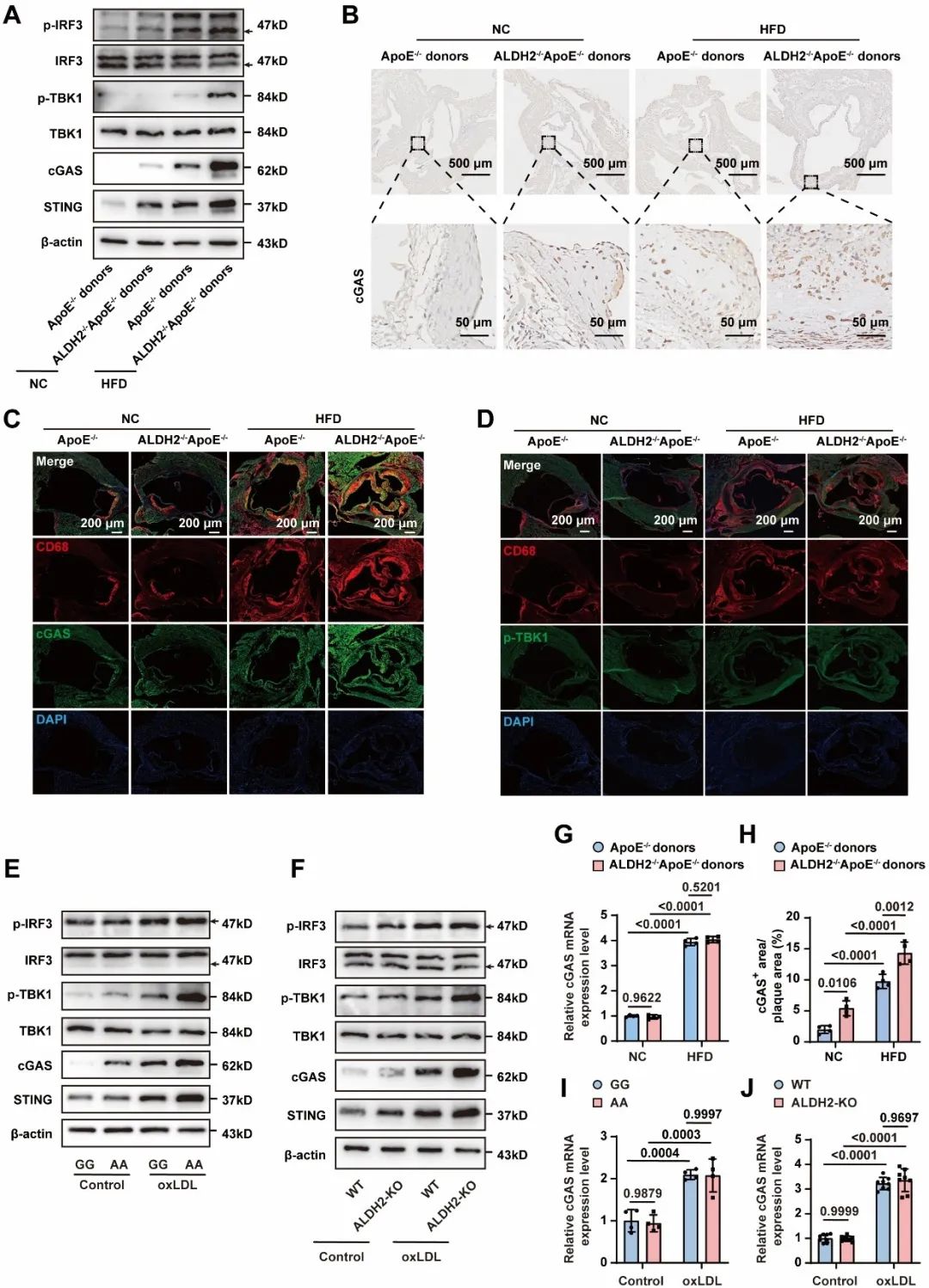
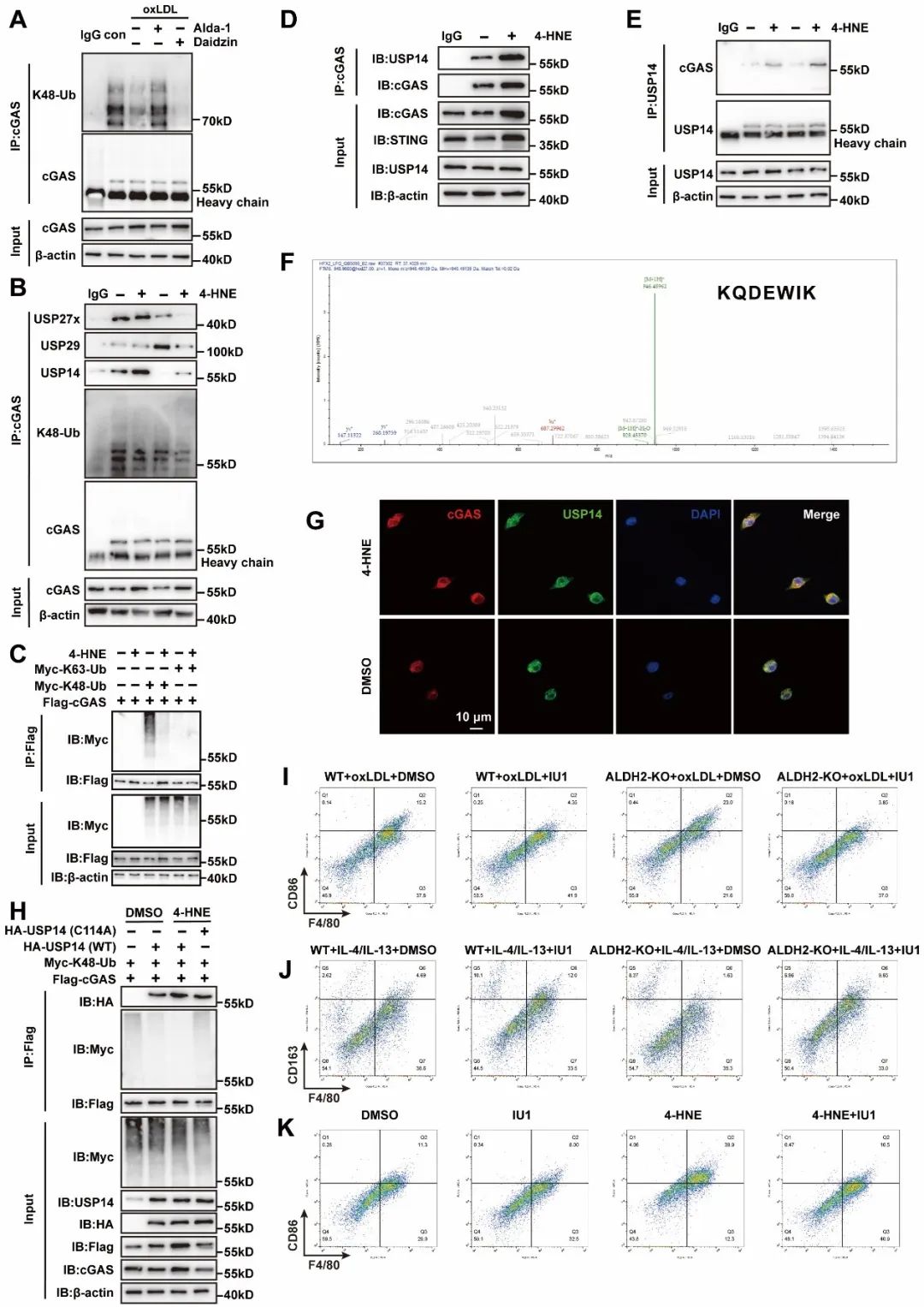
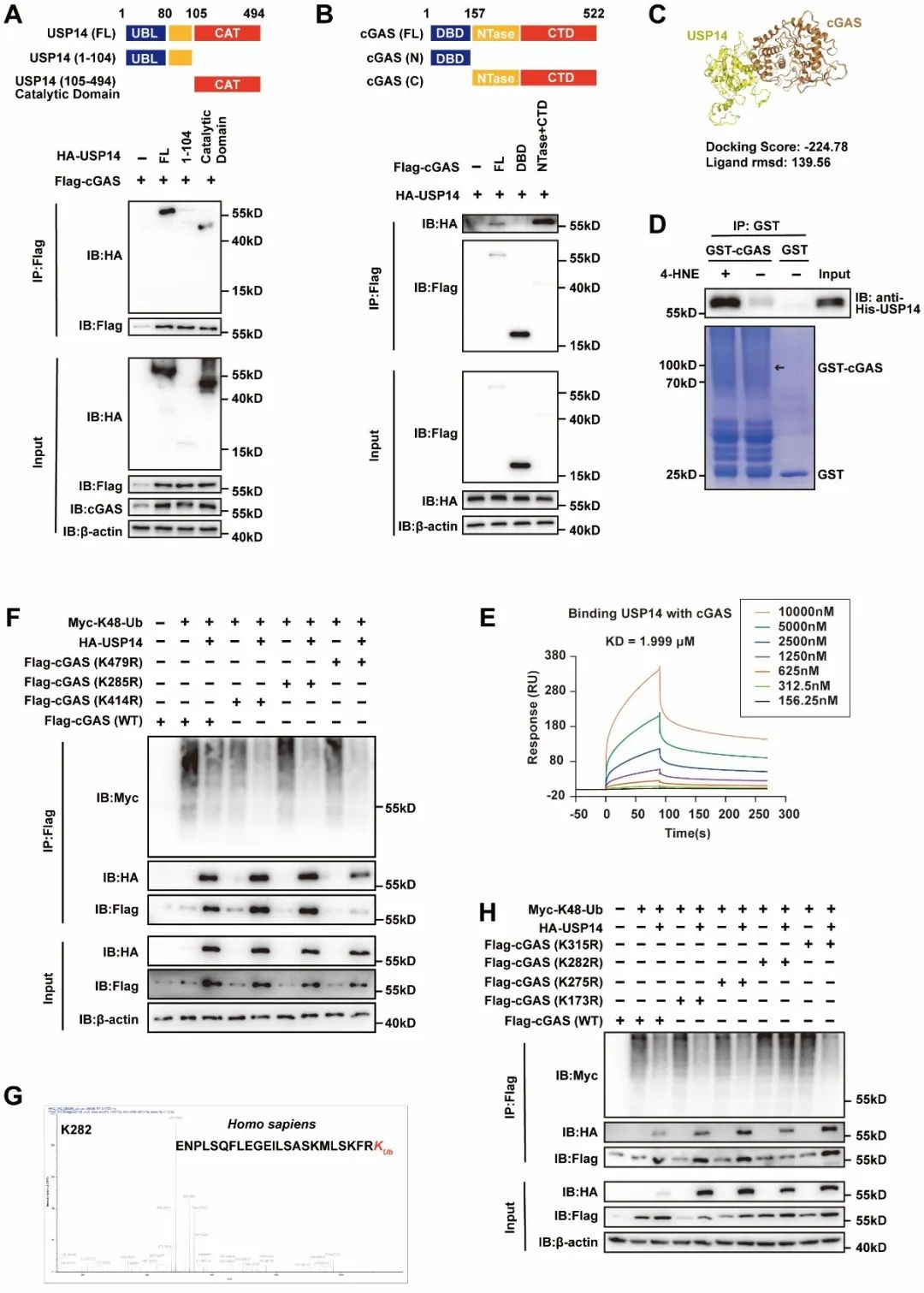
研究者接下来探究ALDH2调控cGAS-STING信号通路的分子机制,发现ALDH2失活增加cGAS的蛋白表达水平但并不影响其mRNA变化。进一步实验发现,毒性醛4-HNE促进了USP14与cGAS结合,从而抑制cGAS的K48泛素化修饰,阻抑cGAS蛋白降解,进而激活下游STING信号通路;而ALDH2通过代谢4-HNE,促进cGAS泛素化修饰增强其降解,抑制STING信号通路。为明确USP14对cGAS作用的泛素化位点,作者构建了cGAS的泛素化修饰位点突变的质粒进行免疫共沉淀。结果表明,cGAS K282是USP14调控cGAS泛素化修饰的关键位点。
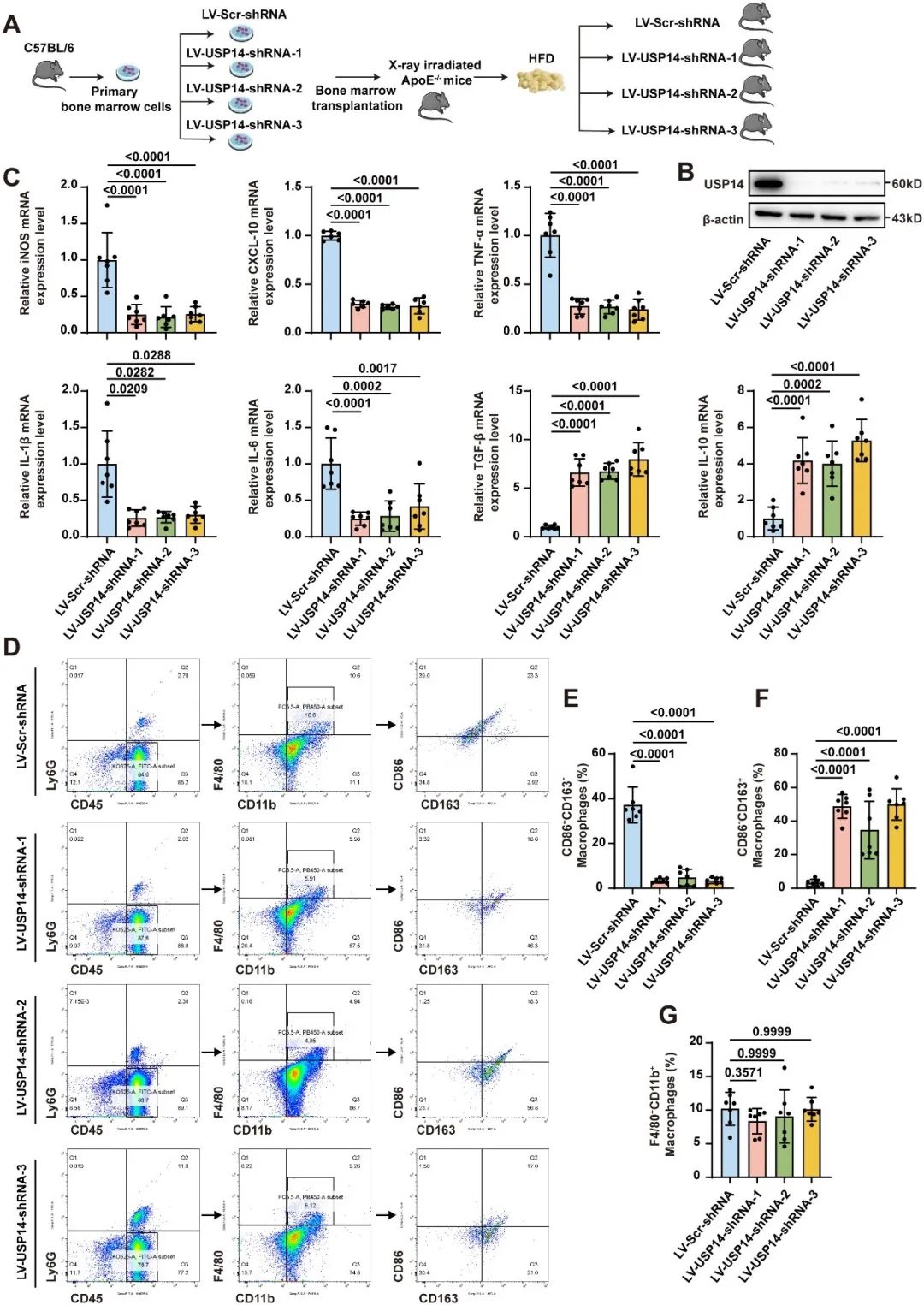
最后,在动物实验中,研究者通过骨髓移植将特异性敲低了USP14表达的骨髓巨噬细胞回输至ApoE-/-小鼠体内,随后构建AS模型,结果证实敲低USP14,特别是在巨噬细胞中,显著增加了巨噬细胞抗炎表型,减少了巨噬细胞促炎表型,抑制了巨噬细胞的炎症反应,减轻AS进展。
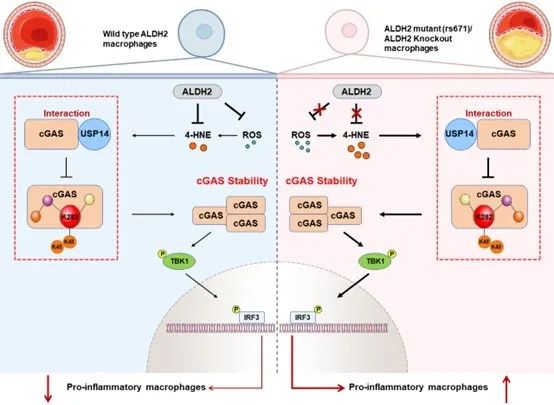
综上所述,本研究揭示了ALDH2调控AS进展的新机制,ALDH2通过代谢毒性醛4-HNE抑制去泛素化酶USP14与cGAS的结合,促进了cGAS K282位点的K48泛素化修饰,导致cGAS蛋白降解增多,从而抑制了cGAS-STING信号通路的激活以及随后的炎症反应,减轻了AS的发生发展,为AS防治提供了新思路及靶点。
山东大学齐鲁医院为第一和通讯作者单位。山东大学齐鲁医院陈玉国教授、徐峰教授、薛丽教授为该论文的通讯作者,山东大学齐鲁医院急诊医学博士研究生芮海英、于华祥为论文的共同第一作者。该研究工作得到了国家自然科学基金重点项目、国家重点研发计划等项目的资助。
原文链接:
https://doi.org/10.1016/j.redox.2024.103318
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#动脉粥样硬化# #ALDH2#
58