Axicabtagene-ciloleucel作为不适合移植的大B细胞淋巴瘤的二线治疗——II期ALYCANTE研究
2023-11-12 淋立尽治 淋立尽治 发表于上海
ALYCANTE是一项开放标签的2期研究,在62例被认为不符合HDCT/HSCT的R/R LBCL 患者中评价 axi-cel 作为二线治疗的疗效和安全性。
研究背景
Axicabtagene ciloleucel (axi-cel)作为二线治疗被认为在适合自体干细胞移植(ASCT)的高风险复发/难治性(R/R)大B细胞淋巴瘤(LBCL)患者的疗效优于标准治疗;然而,在临床实践中,大约一半的R/R LBCL患者被认为不适合进行ASCT。axi-cel 在不适合移植的患者中的疗效仍有待确定。
ALYCANTE是一项开放标签的2期研究,在62例被认为不符合HDCT/HSCT的R/R LBCL 患者中评价 axi-cel 作为二线治疗的疗效和安全性。
研究方法
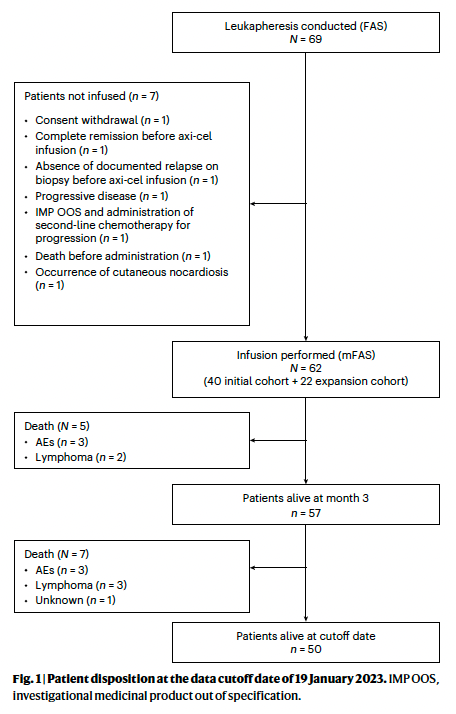
在2021年3月19日至2022年5月4日期间,共有69名患者入组并接受了白细胞分离术。在这69例患者中,62例(89.8%)在2021年4月26日至2022年6月16日期间接受了单axi-cel细胞输注,因此被纳入修改的完整分析集(mFAS)。
总体而言,有7例患者接受了白细胞分离术,但由于疾病进展(n = 1)、临床试验药品不合格(n = 1)、基于研究者评估的轴细胞输注前的CMR (n = 1)、axi-cel输注前活检未记录复发(n = 1)、同意退出(n = 1)、皮肤诺卡病(n = 1)和淋巴瘤相关死亡(n = 1)而未接受axi-cel细胞输注。截至2023年1月19日的数据截止日期,从纳入研究到axi-cel细胞输注的中位时间为41.5天(四分位数间距(IQR), 38.0-48.0),axi-cel细胞输注的中位随访时间为12.0个月(IQR, 9.1-12.6)。
研究终点
主要终点是研究者评估的axi-cel细胞输注后3个月的完全代谢反应(CMR)。
次要终点为axi-cel细胞输注后3个月的客观缓解率(ORR)、axi-cel细胞输注后6个月的CMR、最佳ORR、最佳CMR、反应持续时间(DOR)、白细胞分离后的EFS、输注后的PFS、输注后的OS以及不良事件的发生率、性质和严重程度。本文中未报道的其他计划次要终点包括与健康相关的生活质量和axi-cel的细胞产物特性和细胞动力学。
在最初的研究方案中,我们计算出40例侵袭性B细胞非霍奇金淋巴瘤患者的样本量,这些患者在一线化学免疫治疗后不超过12个月复发,并且根据医生的评估不适合进行HDCT/ASCT,这足以测试axi-cel细胞输注的疗效。该研究初始部分(n = 40)达到了主要终点,研究者评估的CMR在输注后3个月为67.5%。
随后对该方案进行了修订,纳入了更多的患者,以便对不同年龄亚组(<70岁和≥70岁)的axi-cel细胞的疗效和毒性进行平衡比较。最终,本研究报告了62例接受轴细胞输注的患者的研究结果。重要的是,初始队列(n = 40)和扩展队列(n = 62)的患者特征和结局相似。
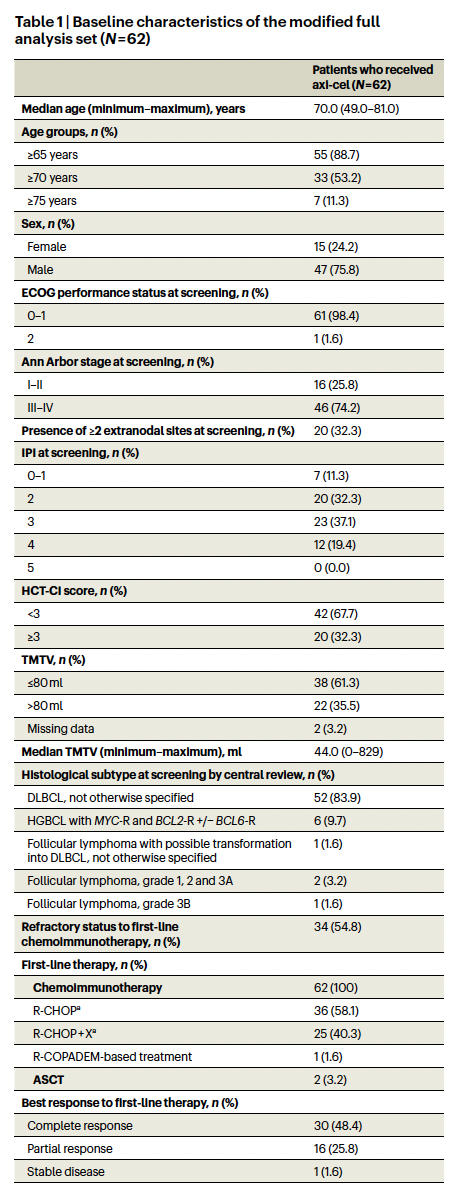
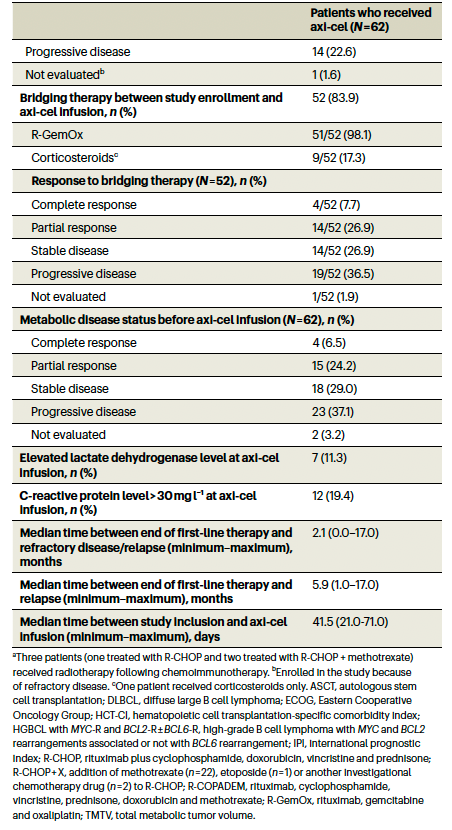
研究结果
所有患者中位年龄为70岁(49-81岁),女性15例(24.2%),国际预后指数(IPI)为3及以上的35例(56.5%)。几乎所有患者的ECOG评分为0或1 (n=61;98.4%)。大多数患者(n=52;83.9%)组织学诊断为弥漫性大B细胞淋巴瘤(DLBCL)。共有34例(54.8%)患者对一线化疗免疫治疗有难治性。由于年龄≥65岁(88.7%),高造血细胞移植特异性合病指数(HCT-CI)评分≥3(32.3%)和/或既往ASCT(3.2%),患者被认为不适合进行HDCT/ASCT检查。52例患者(83.9%)在研究者的判断下接受了白细胞分离术后的桥接治疗。52例患者中有51例(98.1%)采用了R-GemOx桥接治疗,疗程为1个周期(n = 25)、2个周期(n = 25)或3个周期(n = 1)。此外,52例患者中有9例(17.3%)接受了皮质类固醇治疗,其中1例患者仅接受皮质类固醇治疗,不使用R-GemOx。在接受桥接治疗的患者中,63.4%没有反应(疾病稳定或进展)。
主要疗效结果
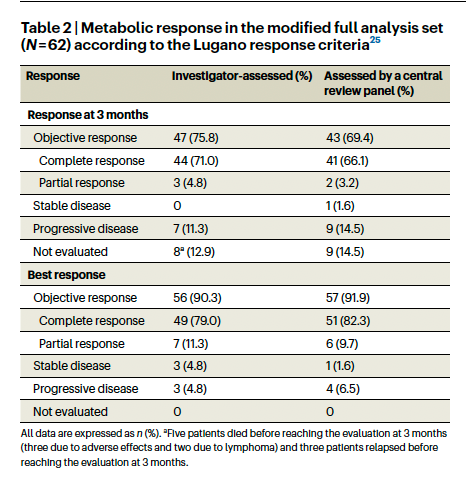
研究者根据Lugano评估,axi-cel细胞输注后3个月的CMR在mFAS (N = 62)中为71.0%(95%置信区间(CI), 58.1-81.8%)(表2)。与mFAS相比,FAS (N = 69)的敏感性分析显示,3个月时研究者评估的CMR无显著差异,为66.7% (95% CI, 54.3-77.6%)。同样,一项排除了2例1-3A级滤泡性淋巴瘤患者和4例通过桥接治疗获得完全缓解的患者的事后分析发现,研究者评估的3个月CMR为67.9% (95% CI, 54.0-79.7%),与mFAS报告的3个月CMR相当。值得注意的是,在axi-cel细胞输注后1个月出现部分代谢反应(PMR)的10例患者中,有5例患者在3个月时不经任何额外治疗转为CMR。
次要疗效结果
在axi-cel细胞输注后3个月,研究者评估的ORR为75.8% (95% CI, 63.3-85.8%)。根据研究者的评估,在axi-cel细胞输注6个月后,总共有37名患者(59.7%)仍处于CMR状态(95% CI, 46.5-72.0%)。研究者评估的最佳ORR和最佳CMR分别为90.3%和79.0%。当中央评审小组评估时,3个月时CMR和ORR分别为66.1% (95% CI, 53.0-77.7%)和69.4% (95% CI, 56.4-80.4%)。中央评审小组评估的最佳ORR和最佳CMR分别为91.9%和82.3%。
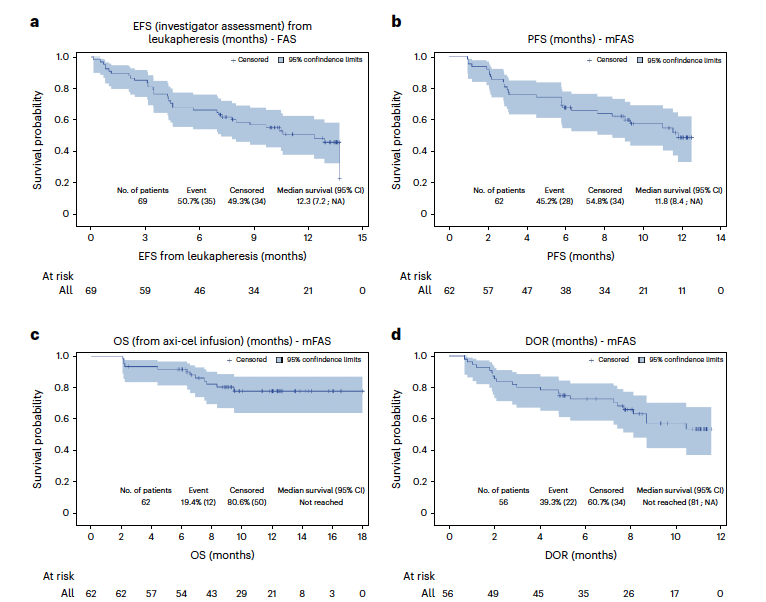
在中位随访12.0个月时,接受白细胞分离术的患者的中位EFS为12.3个月(95% CI, 7.2 -未达到;图2a) (n = 69)。6个月和12个月的估计EFS发生率分别为66.7% (95% CI, 54.2-76.4%)和51.2% (95% CI, 38.2-62.8%)。axi-cel细胞输注患者的中位PFS为11.8个月(95% CI, 8.4 -未达到;mFAS (N = 62)图2b)。估计6个月和12个月的PFS率分别为67.7% (95% CI, 54.5-77.8%)和48.8% (95% CI, 34.0-62.0%)。在mFAS (N = 62)中,axi-cel细胞输注未达到中位OS (图2c)。6个月和12个月的估计OS率分别为91.9% (95% CI, 81.6-96.5%)和78.3% (95% CI, 64.7-87.1%)。中位DOR未达到(图2d)。
安全性
所有的研究参与者至少有一种不同程度的不良反应。62例患者中有59例(95.2%)出现3级或以上不良反应。最常报道的3级或以上不良反应是中性粒细胞减少症(66.1%的患者发生)、贫血(38.7%)和血小板减少症(38.7%)。发生各种程度感染(COVID-19、尿路感染、败血症、呼吸道感染、皮肤感染)33例(53.2%)。最常见的感染是COVID-19, 15例(24.2%),其中≥3级7例,5级2例。
与CAR-T细胞毒性相关的特殊不良反应见表3。93.5%的患者发生细胞因子释放综合征(CRS), 8.1%的患者报告CRS为≥3级。axi-cel细胞输注后至CRS发生的中位时间为1.5天(IQR, 1.0-3.0),中位CRS持续时间为5.0天(IQR, 4.0-9.0)。51.6%的患者发生了免疫效应细胞相关神经毒性综合征(ICANS), 14.5%的患者发生了3级或以上的ICANS。axi-cel细胞输注后ICANS发生的中位时间为6.0天(IQR, 5.0 - 8.0), ICANS持续的中位时间为5.0天(IQR, 3.0-8.0)。没有发生与CRS相关的死亡或神经系统事件。CAR-T细胞毒性主要通过白细胞介素-6受体拮抗剂tocilizumab(77.4%的患者使用)和/或皮质类固醇(64.5%的患者使用)来控制。共有16例患者(25.8%)因CAR-T细胞毒性入住重症监护病房(ICU)。62例患者中有23例(37.1%)出现3级或更严重的延长性细胞减少(定义为在axi-cel细胞输注后30天未解决的贫血、中性粒细胞减少和/或血小板减少的≥3级实验室结果)。
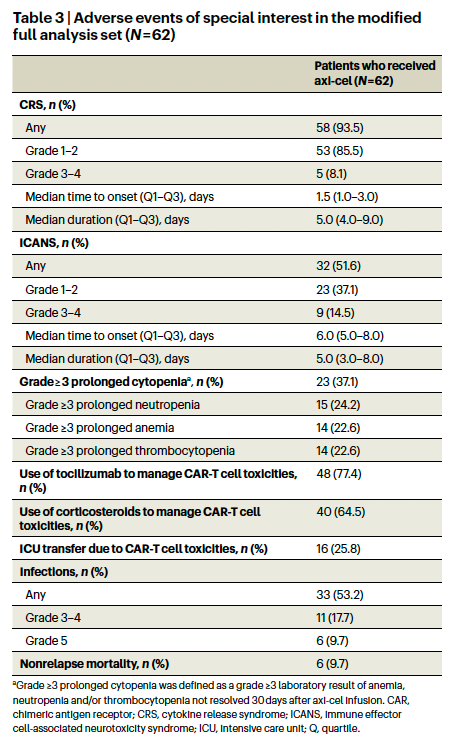
表3
亚组分析
我们调查了axis -cel的疗效和安全性在不同患者群体中是否一致,特别是在年龄≥70岁且HCT-CI评分≥3的合并症患者中。在≥70岁的患者(n = 33)中,3个月的CMR为72.7%,而<70岁的患者(n = 29)为69.0%。<70岁和≥70岁患者的生存结局和DOR具有可比性(图3)。年龄≥70岁的患者与年龄<70岁的患者相比,毒性没有增加,CRS、ICANS和ICU转移率相似。同样,HCT-CI评分≥3的患者(n = 20)报告的3个月CMR为80.0%,与HCT-CI评分< 3的患者(n = 42)相比,生存率相似,毒性没有增加(扩展数据表表5)。最后,除了一个亚组外,所有评估的亚组在3个月时观察到类似的研究者评估CMR。唯一的例外是总代谢肿瘤体积(TMTV),因为在纳入时TMTV体积高(80ml)与3个月时CMR降低相关。
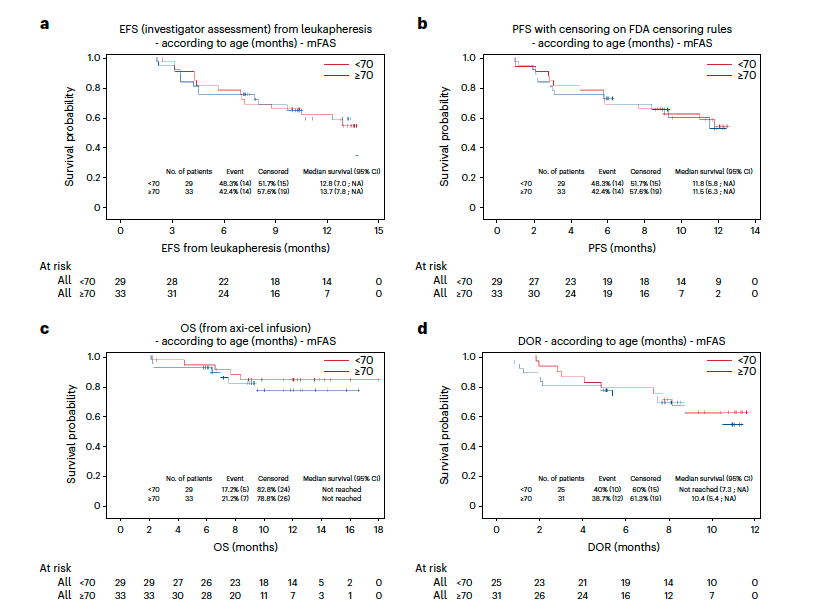
图3
研究结论
对于预后不佳且不符合HDCT/ASCT条件的高风险R/R LBCL患者,axis-cel细胞作为二线治疗可获得高缓解率和持久缓解。此外, axis-cel在不适合HDCT/ASCT的高龄和具有合并症人群中具有可接受的安全性。总之,这些结果支持axis-cel作为不适合HDCT/ASCT的R/R LBCL患者的二线治疗。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言