中心静脉压能否帮助识别机械通气危重患者的急性右心室功能障碍?
2024-08-05 呼吸机从入门到精通 呼吸机从入门到精通 发表于上海
探讨重症机械通气患者中心静脉压(CVP)与急性右心室(RV)功能障碍的关系。

这篇文章是一项回顾性队列研究,探讨了中心静脉压(CVP)在识别机械通气危重患者急性右心室功能障碍(RVD)及其伴随的全身静脉充血方面的效用。研究纳入了518名患者,通过超声心动图评估了右心室功能,并根据三尖瓣环平面收缩期位移(TAPSE)、面积变化分数(FAC)和三尖瓣环侧向收缩期速度波(S')等指标,将患者分为三组:正常右心室功能组、单纯右心室功能障碍组和右心室功能障碍伴充血组。研究结果显示,CVP对于鉴别伴有充血的右心室功能障碍具有较好的鉴别能力,最佳CVP截断值为10 mm Hg,灵敏度为79.2%,特异度为69.4%,阴性预测值为96.7%,阳性预测值为22.8%。然而,CVP在识别所有右心室功能障碍方面的辨别能力较低,存在较大的灰色区域,表明CVP作为单一诊断工具的局限性。研究还发现,CVP与TAPSE、FAC和S'之间存在弱相关性,提示CVP可能在一定程度上反映右心室功能状态。此外,多元逻辑回归分析显示CVP和ARDS的存在是伴有充血的RV功能障碍的独立预测因素。尽管CVP在诊断伴有充血的右心室功能障碍方面具有潜在价值,但研究者强调了其准确性的局限性,并建议CVP不应单独用于识别一般的右心室功能障碍。研究建议,CVP应被视为潜在RV受损的警告信号,并需要结合超声心动图等更全面的评估。这篇文章为临床医生提供了重要的见解,特别是在重症监护环境中,CVP的监测可以作为一个有用的工具来辅助诊断和治疗决策。然而,由于其局限性,CVP的测量结果需要谨慎解读,并结合其他临床和诊断信息。看法及展望:
- 尽管CVP是一个容易获取的参数,但其在诊断右心室功能障碍时的准确性有限,需要结合其他诊断工具。
- 临床医生应意识到CVP的局限性,并在评估患者时应考虑多种因素。
- 未来的研究应探索如何结合CVP与其他血流动力学参数,以提高对右心室功能障碍的诊断准确性。
- 需要进一步研究CVP与其他潜在的生物标志物或影像学技术结合使用的效果。
- 考虑到CVP在不同患者群体中的变异性,应开展更多前瞻性研究来验证其在不同临床情境中的效用。
目的
探讨重症机械通气患者中心静脉压(CVP)与急性右心室(RV)功能障碍的关系。
方法
本研究回顾性分析了接受经胸超声心动图检查和CVP监测的危重机械通气患者,收集了包括三尖瓣环平面收缩期位移(TAPSE)、面积变化分数(FAC)和三尖瓣环侧向收缩期速度波(S')在内的超声心动图指标以评估右心室功能。然后根据患者的 RV 功能和全身静脉充血的存在情况(通过下腔静脉直径 (IVCD) 和肝静脉 (HV) 多普勒进行评估)将患者分为三组:正常 RV 功能(TAPSE ≥ 17 mm、FAC ≥ 35% 和 S' ≥9.5 cm/sec),单独 RV 功能障碍(TAPSE < 17 mm 或 FAC < 35% 或 S' <9.5 cm/sec,IVCD ≤ 20 mm 或 HV S ≥ D))和伴有充血的 RV 功能障碍(TAPSE < 17 mm 或 FAC < 35% 或 S' <9.5 cm/sec,IVCD > 20 mm 和 HV S < D)。
结果
共纳入518例患者,其中301例为正常右心室功能组,164例为单纯右心室功能障碍组,53例为右心室功能障碍伴充血组。受试者工作特征分析显示CVP对右心室功能障碍和充血患者有良好的鉴别能力(AUC 0.839;95% CI:0.795–0.883;p < 0.001)。最佳CVP截断值为10 mm Hg,灵敏度为79.2%,特异度为69.4%,阴性预测值为96.7%,阳性预测值为22.8%。9 mm Hg和12 mm Hg之间存在较大的灰色区域,涵盖95例患者(18.3%)。对于识别所有患有右心室功能障碍的患者,CVP 表现出较低的辨别能力(AUC 0.616;95% CI:0.567–0.665;p < 0.001)。此外,灰色区域甚至更大,范围从 5 毫米汞柱到 12 毫米汞柱,包括 349 名患者(67.4%)。
结论
对于使用机械通气的重症患者,CVP 可能是诊断急性右心室功能障碍并伴有全身静脉充血的有用指标,但其准确性有限。CVP 小于 10 mm Hg 几乎可以排除伴有充血的右心室功能障碍。相反,CVP 不应用于识别一般的右心室功能障碍。
背景
近年来,右心室 (RV) 已成为血流动力学和预后的关键决定因素 [ 1、2、3、4 ]。其主要功能是将接收到的所有血液逐搏输送到肺循环,而不会导致中心静脉压 (CVP) 升高 [ 5 ]。CVP 有时可作为静脉回流和 RV 调节能力之间平衡的标志 [ 6 ]。然而,作为腔内压力,CVP 会受到胸内压、心包压和腹内压的影响,这些因素在重症患者中更容易升高 [ 7 ]。
尽管已确定右心室功能在血流动力学中的作用,但对于评估右心室功能障碍的最佳 CVP 阈值仍然存在知识空白 [ 3 ]。Bech-Hanssen 等人建议 CVP ≥ 10 mmHg 作为左心室疾病患者严重右心室功能障碍的标准 [ 8 ]。对于使用左心室辅助装置的患者,CVP 超过 15 或 16mmHg 被认为是右心室衰竭的征兆 [ 9 , 10 ]。尽管如此,Vieillard-Baron 认为右心室扩张和 CVP ≥ 8 mmHg 定义右心室功能障碍,并可能对脓毒症休克患者的容量管理产生影响 [ 11 ]。本研究旨在探讨 CVP 在识别危重患者急性右心室功能障碍方面的效用。本研究的目的是阐明使用机械通气的危重患者中 CVP 与急性右心室功能障碍之间的关系。
患者和方法
研究人群
这项回顾性队列研究调查了 2018 年 8 月至 2024 年 1 月期间入住三级医院重症监护病房 (ICU) 的患者。纳入标准包括入院后 24 小时内接受经胸超声心动图 (TTE) 检查的使用机械通气的危重患者。
我们排除患有慢性心力衰竭、心脏手术、中度至重度慢性肺动脉高压、缩窄性心包炎、心房颤动或缺乏 CVP 监测或 TTE 视图不足的患者。
本研究遵循赫尔辛基宣言,经我院伦理委员会批准(批准号:I-23PJ1278),并取得患者近亲属书面同意对患者医疗资料进行查阅和研究。
超声心动图
在该重症监护室中,常规进行 TTE 检查。检查期间同时记录血流动力学和呼吸参数。将图像存档以供离线分析。使用配备 2.5 MHz 相控阵探头的迈瑞超声心动图仪(中国深圳)进行图像采集。根据 PRICES 声明解释超声心动图结果 [ 12 ]。两名拥有 10 多年超声心动图经验的医生独立审查了图像并就结果达成共识。这些研究人员之前曾报告过关键心脏功能测量的观察者内和观察者间差异 [ 13 ]。
使用三尖瓣环平面收缩期位移(TAPSE)、面积变化分数(FAC)和三尖瓣侧面环收缩期速度波(S')评估右心室功能。所有测量值均从心尖四腔心切面获得。将 M 型光标沿三尖瓣环侧面部分放置来测量 TAPSE。使用脉冲波组织多普勒将样本体积放在三尖瓣环侧面来测量 S'。FAC 计算为 [(舒张末期面积―收缩末期面积)/舒张末期面积]×100。右心室功能障碍定义为 TAPSE < 17 mm 或 FAC < 35% 或 S' < 9.5 cm/秒。[ 14 ]。R/LVEDA 比率 > 0.6 被认为是右心室扩张[ 4 ]。急性肺心病(ACP)定义为收缩末期右心室扩张与室间隔矛盾运动相结合[ 15 ]。
使用下腔静脉直径 (IVCD) 和肝静脉 (HV) 多普勒波形评估全身静脉充血。IVCD > 20 毫米且 HV 频谱多普勒模式显示 S 波速度低于 D 波速度 (S < D) 提示充血 [ 16 ]。在呼气末,在肋下纵向视图中测量 IVCD,位于肝静脉起点的上游。还通过将样本体积定位在距其与 IVC 交界处 2-3 厘米处,从肋下视图识别 HV。
采用先前描述的方法获得左心室流出道速度-时间积分 (LVOT-VTI)、左心室射血分数 (LVEF)、二尖瓣峰值 E 速度 (E)、舒张早期二尖瓣环外侧和内侧平均组织多普勒速度 (e')、三尖瓣反流 (TR)、每搏输出量指数和心脏指数[ 13 ]。
随后根据右心室功能和体静脉充血情况将患者分为三组:(1)正常右心室组(TAPSE ≥ 17 mm、FAC ≥ 35% 和 S' ≥9.5 cm/sec);(2)单纯右心室功能障碍组(TAPSE < 17 mm 或 FAC < 35% 或 S' <9.5 cm/sec,IVCD ≤ 20 mm 或 HV S ≥ D);(3)右心室功能障碍 + 充血组(TAPSE < 17 mm 或 FAC < 35% 或 S' <9.5 cm/sec,IVCD > 20 mm 和 HV S < D)。
收集临床数据
我们收集了患者的人口统计学信息、基线急性生理与慢性健康评估 (APACHE) II 评分和序贯器官衰竭评估 (SOFA) 评分。此外,从超声心动图检查期间的数据记录或医疗记录中获得超声心动图检查时的心率 (HR)、平均动脉压 (MAP)、去甲肾上腺素 (NE) 剂量、PEEP、平台压 (Pplat) 和液体平衡。在超声心动图检查后,患者处于仰卧位,换能器精确调零在胸部中部水平,在呼气末期测量 CVP。我们还收集了 30 天死亡率、前 24 小时内最高乳酸水平以及前 24 小时内急性呼吸窘迫综合征 (ARDS) 和急性肾损伤 (AKI) 发病率的数据。根据改善全球肾脏病预后组织 (KDIGO) 共识标准 [ 17 ], AKI 定义为血清肌酐增加至少 26 µmol/L 或增加 50%,或开始肾脏替代治疗。我们排除了尿量标准,因为利尿剂的使用可能会造成混淆,这在 ICU 患者中很常见。
统计分析
基线人口统计学和超声心动图测量结果以中位数(四分位距)表示定量变量,以数目(百分比)表示定性变量,或以平均值±SD表示。使用 Kolmogorov-Smirnov 检验评估连续值的分布是否符合正态性。使用 Kruskal-Wallis 检验比较定量变量,必要时使用 Dunnett 事后检验进行成对比较。使用卡方检验或 Fisher 精确检验(视情况而定)比较分类变量。Spearman 等级相关系数评估相关性。生成了具有 95% 置信区间 (CI) 的接收者操作特性 (ROC) 曲线,以评估 CVP 检测伴有充血的 RV 功能障碍和一般 RV 功能障碍的能力。使用 Youden 指数确定最佳截止值。使用两种方法计算灰色区域:(1)来自 1000 个人口引导法的 Youden 指数的 95% 可信区间,和(2)对应于敏感性或特异性小于 90%(10% 诊断容差)的截止值 [ 18 ]。这两种方法中的最大区间定义了灰色区域。二元逻辑回归确定了充血性右心室功能障碍的预测因子。单变量模型中p值 < 0.1 的基线协变量被纳入多变量模型,并计算了 95% 可信区间的优势比。所有统计分析均使用 SPSS(SPSSInc.,美国伊利诺伊州芝加哥)和 Graphpad Prism(适用于 Windows 的 6.01 版,GraphPad Software,美国加利福尼亚州拉霍亚)进行。双尾p < 0.05 被认为是显着的。
结果
一般特征
共计 836 名患者符合入选条件,其中 318 名被排除(图 1)。在 518 名入选患者中,301 名右心室功能正常,164 名仅有右心室功能障碍,53 名右心室功能障碍伴充血。三组在基线特征方面存在显著差异,包括 APACHE II、SOFA、NE 剂量、HR、Pplat 水平、24 小时最高乳酸水平、液体平衡、非 ICU 天数、ARDS 发生率、AKI 发生率和 30 天死亡率(所有p < 0.05)(表 1)。三组的 CVP 水平有显著差异(p < 0.001)(图 2 A)。
图 1
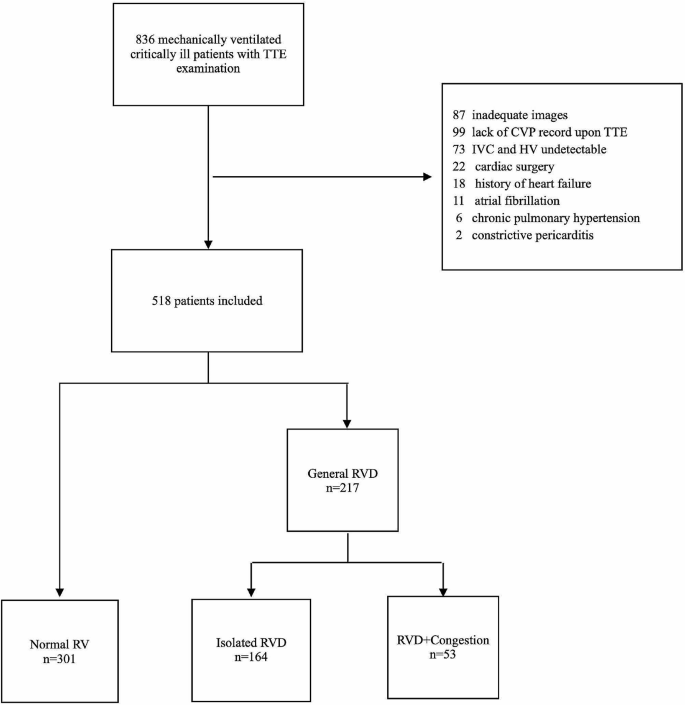
本研究流程图。TTE:经胸超声心动图;CVP:中心静脉压;IVC:下腔静脉;HV:肝静脉;RV:右心室;RVD:右心室功能障碍
表 1 所有患者的一般特征(略)
图 2
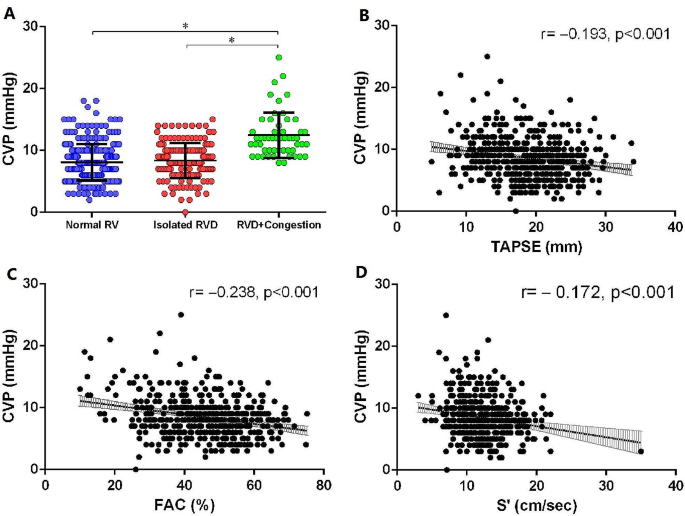
A. CVP 与 RV 功能的关系。RVD + 充血组的 CVP 显著高于单纯 RVD 组和正常 RV 功能组,p < 0.001。B. TAPSE 与 CVP 相关,r =-0.193,p < 0.001。C. FAC 与 CVP 相关,r =-0.238,p < 0.001。D. RV S' 与 CVP 相关,r =-0.172,p < 0.001CVP :中心静脉压;RV:右心室;RVD:右心室功能障碍;TAPSE:三尖瓣环平面收缩期位移;FAC:面积变化分数;S':三尖瓣侧环收缩期速度波
三组超声心动图参数比较
三组 LVEF、MAPSE、E 速度、TAPSE、FAC、RV S'、外侧 e'、内侧 e'、LVOT-VTI 和 IVCD 均有显著差异(p < 0.001)。此外,R/LVEDA、TR、E/e' 和心脏指数也有显著差异(p < 0.05)。RVD 和充血组的 ACP 患病率最高(p < 0.001)(表 2)。
表 2 超声心动图参数(略)
CVP与RV功能的相关性分析
我们观察到 CVP 与 TAPSE、RV FAC 和 RV S' 之间存在弱相关性(分别为r =-0.193、-0.238、-0.172;所有p < 0.001)(图 2B和 D)。
CVP 的 ROC 分析用于检测 RV 功能障碍
ROC 分析显示,CVP 判断所有患者右心室功能障碍伴充血的 AUC 为 0.839(95% CI:0.795–0.883;p < 0.001)。10 mm Hg 的临界值灵敏度为 79.2%,阴性预测值 (NPV) 高达 96.7%,表明其在排除这种合并症方面很有用。然而,阳性预测值 (PPV) 为 22.8%。灰色区域介于 9 mm Hg 和 12 mm Hg 之间,95 名患者(18.3%)位于该区域(表 3;图 3 A 和 B)。
表3 CVP在预测RVD+充血和一般RVD中的ROC分析(略)
图 3
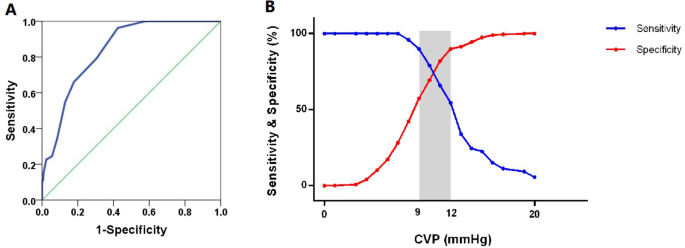
CVP检测 RVD + 充血的 ROC 曲线和敏感性和特异性。A . CVP 检测 RVD + 充血的 ROC 曲线。CVP 确定所有患者的 RV 功能障碍 + 全身静脉充血的 AUC 为 0.839,95% CI:0.795–0.883;p < 0.001。B. CVP检测 RVD + 充血的敏感性和特异性。不确定区域(诊断容差 > 10%)用阴影矩形表示。灰色区域范围在 9 mmHg 和 12 mmHg 之间,其中 95 名(18.3%)患者位于 CVP:中心静脉压;RVD:右心室功能障碍;
ROC 分析显示,与伴有充血的右心室功能障碍相比,CVP 在识别所有右心室功能障碍患者方面的判别能力较低(AUC 0.616;95% CI:0.567–0.665;p < 0.001)。最佳截断值为 9 mm Hg,灵敏度 (58.5%) 和特异性 (59.8%) 均衡。然而,相当一部分患者 (67.4%, n = 349) 处于灰色区域 (5–12 mm Hg),进一步强调了 CVP 作为整体右心室功能障碍的单一诊断工具的局限性(表 3;图 4 A 和 B)。
图 4
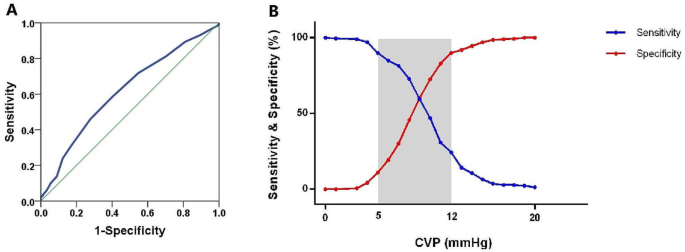
CVP 检测一般 RV 功能障碍的ROC 曲线和敏感性和特异性。A . CVP 检测一般 RVD 的 ROC 曲线。所有患者中 CVP 确定 RVD 的 AUC 为 0.616,95% CI:0.567–0.665;p < 0.001。B. CVP检测一般 RVD 的敏感性和特异性。不确定区域(诊断容差 > 10%)用阴影矩形表示。灰色区域范围在 5 mmHg 和 12 mmHg 之间,349 名(67.4%)患者位于该区域。CVP:中心静脉压;RVD:右心室功能障碍;
多元分析
多元逻辑回归分析调整了 ARDS 的存在、NE 剂量和 Pplat 水平,结果显示 CVP(OR 1.494,95%CI:1.312-1.702;p < 0.001)和 ARDS 的存在(OR 2.494,95%CI:1.118-5.565;p < 0.001)是伴有充血的 RV 功能障碍的独立预测因素(补充表1)。
敏感性分析
为了评估 LVEF 对 CVP 诊断右心室功能障碍伴充血能力的影响,进行了敏感性分析。在 341 名 LVEF ≥ 50% 的患者中,20 名患者确诊为右心室功能障碍伴充血;同样,在 177 名 LVEF < 50% 的患者中,33 名患者确诊为右心室功能障碍伴充血。敏感性分析显示,在 LVEF ≥ 50% 的患者中,CVP 检测右心室功能障碍伴充血的判别能力与在 LVEF < 50% 的患者中相似(AUC 0.864 vs. 0.788,Z = 1.590,p = 0.112)。同样,R/LVEDA ≥ 0.6 的患者的 CVP 表现出与 R/LVEDA < 0.6 的患者相似的辨别能力(AUC 0.883 vs. 0.816,Z = 1.373,p = 0.170)。
讨论
本研究调查了 CVP 在识别机械通气危重患者急性右心室功能障碍和全身静脉充血方面的效用。虽然 CVP 对该综合终点表现出可接受的判别能力(AUC = 0.839),但较大的灰色区域(18.3%)限制了其诊断准确性。此外,仅基于收缩功能,CVP 并不是一般右心室功能障碍的可靠标志。这些发现表明,CVP 可能是识别伴有充血的右心室功能障碍的有用辅助手段,但其局限性需要谨慎对待,尤其是单独使用时。
CVP 测量是 ICU的常规程序,可随时用于危重患者。尽管其在指导液体复苏中的作用一直存在争议,但 CVP 仍然可以作为避免过量液体输注的“停止标志”[ 19、20、21 ]。如果 CVP 较高,上部静脉储液器和毛细血管中的压力会更高,这将显著增加水肿形成 [ 22 ]。因此,人们更加关注 CVP 在指示容量超负荷和随后的器官灌注受损方面的作用 [ 23、24 ] 。然而,CVP 可以反映静脉回流和 RV 功能之间的相互作用。当 RV 功能恶化时,它不能充分处理静脉回流,导致 CVP 升高。鉴于及时发现 RV 功能障碍的重要性,超声心动图由于参数复杂、图像采集和解释而带来了挑战。因此,像 CVP 这样随时可用的工具,如果提示 RV 功能障碍,可以作为临床医生的警报。
虽然缺乏标准化的右心室功能障碍标准,但我们采用了三种常用的超声心动图指标。我们发现 ARDS 是伴有充血的右心室功能障碍的独立预测因子,可能符合欧洲心脏病学会制定的右心室衰竭标准 [ 25 ]。ARDS 是最常见的对右心室构成挑战的疾病之一,具体取决于肺损伤的严重程度和呼吸机设置 [ 4 ]。虽然我们的 ICU 人群是异质性的,但 47.2% 的右心室功能障碍和充血患者患有 ARDS,20.8% 患有 ACP。CVP 升高也可以提示伴有充血的右心室功能障碍,但是,CVP 截断值附近的广泛范围和低阳性预测值(22.8%)突显了其作为唯一诊断工具的局限性。这可能是由于胸内压对危重患者 CVP 的影响所致,尽管各组之间的呼吸机设置没有显著差异。未来结合食管压监测的研究可能会澄清这一假设。我们之前的研究还表明,CVP 升高可以与正常的 RV 收缩功能共存,这在某些患者中表现为 HV 多普勒 S > D [ 26 ]。值得注意的是,测量偏差无法完全消除,这进一步导致了低阳性预测值。重要的是,96.7% 的高阴性预测值表明,对于 CVP 低于 10 mm Hg 的患者,出现伴有全身充血的 RV 功能障碍的可能性很小。此外,12 mm Hg 的 CVP 上限值与之前的研究结果一致 [ 27、28、29 ] 。这些研究表明,高于 13 mm Hg 的 CVP 不太可能表示液体反应性,并且可能与危重患者的预后较差有关。因此,CVP 应被视为潜在 RV受损的警告信号,需要进行包括超声心动图在内的全面评估。此外,鉴于 RV 功能障碍的预后意义,临床医生应努力将危重患者的 CVP 维持在尽可能低的水平。
我们曾假设 CVP 可以反映右心室功能障碍,因为 CVP 是基于 Starling 曲线和 Guyton 理论由静脉回流和心脏功能决定的 [ 30 ]。然而,我们观察到单纯右心室功能障碍患者和右心室功能正常患者的 CVP 值相似,再加上大量的灰色区域,强调了 CVP 在检测一般右心室功能障碍方面的局限性。这与以下概念相一致:右心室充盈可以在其无应力容积以下发生,而扩张压没有显著变化,并且右心室充盈通常与 CVP 无关 [ 31 ]。相反,CVP 上升而右心室每搏输出量稳定或下降提示右心室衰竭,可能成为进一步补液的停止点。因此,CVP 可能更多地提示右心室衰竭而不是右心室功能障碍。此外,我们发现单纯右心室功能障碍患者的 AKI 患病率高于右心室功能正常患者。这可能是因为单纯性右心室功能障碍患者的 CI 低于右心室功能正常的患者(2.7 vs. 3.0 L/min/m 2)。此外,单纯性右心室功能障碍患者更容易出现充血,其肝静脉多普勒异常率更高(7.9% vs. 4.3%)就是明证。虽然机制需要进一步研究,但这一发现表明,检测单纯性右心室功能障碍可能仍具有临床意义。
本研究的一个主要优势在于规模大,并且具备全面的超声心动图和 CVP 监测,确保了 RV 相关参数的高测量率。然而,这项研究有几个局限性。首先,回顾性设计限制了结论的说服力。此外,纳入标准将研究人群限制为使用 TTE 的机械通气患者,并由于缺少 CVP 数据或 IVC 图像不充分而排除了大量患者。这可能会限制研究结果的普遍性。其次,虽然该研究侧重于 IVC 和 HV 测量来评估全身充血,但缺乏门静脉和肾内静脉多普勒数据可能无法全面反映静脉血流动力学。尽管如此,IVC 和 HV 与右心直接相关,在很大程度上反映了 RV 功能。先前的研究表明,在心脏手术患者中,肝脏 S/D 比率和门静脉搏动分数之间存在相关性 [ 32 ]。最后,该研究设计仅在单个时间点捕获了 CVP。未来有必要进行具有连续测量的前瞻性研究,以强化这一结论。尽管存在这些局限性,但本研究表明,机械通气患者 CVP 高于 12 毫米汞柱与右心室衰竭的可能性很高。然而,对于 CVP 值在灰色区域内的患者,超声心动图评估应被视为对右心室功能障碍的明确诊断至关重要。
结论
对于使用机械通气的重症患者,CVP 可能有助于诊断急性右心室功能障碍并伴有全身静脉充血,但其准确性有限。CVP 低于 10 毫米汞柱几乎可以排除伴有充血的右心室功能障碍。相反,CVP 不应用于识别一般的右心室功能障碍。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#中心静脉压# #机械通气危# #急性右心室功能障碍#
42