【醉仁心胸】一氧化氮通过体外循环回路输送对成人心脏手术后氧合的影响(NOCARD试验):一项随机对照试验
2024-10-03 古麻今醉网 古麻今醉网 发表于上海
本研究结果表明,基础低氧血症的患者在心脏手术后接受一氧化氮治疗能降低低氧血症发生率并升高PaO2/FiO2。

摘要
[背景]心脏手术中涉及体外循环可引发显著的全身炎症反应,导致多种术后并发症,包括肺功能障碍、心肌和肾脏损伤。
[目的]研究经体外循环回路输送一氧化氮对术后各种结果的影响。
[设计]前瞻性、单中心、双盲、随机对照试验。
[环境]以色列贝利森医院的Rabin医疗中心。
[患者]计划进行择期心脏手术的成年患者随机分配到研究组之一。
[干预措施]试验组经体外循环回路输送40 ppm一氧化氮。对照组则未输送一氧化氮。
[结果测量]主要结果是术后24小时内低氧血症的发生率,定义为动脉氧分压与吸入氧浓度比值小于300。次要结果为术后72小时内低心排血量综合征和急性肾损伤的发生率。
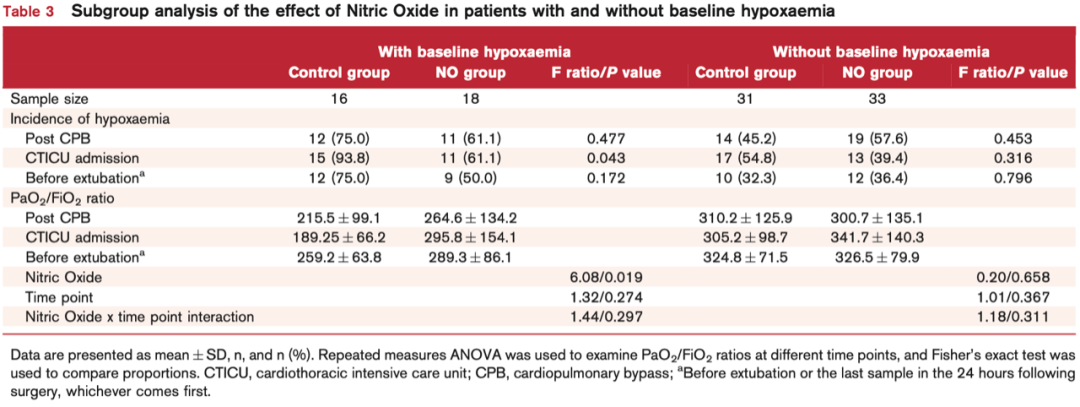
[结果]最终分析中包含98名患者,其中47名分配到对照组,51名分配到试验组。试验组在心胸外科重症监护病房入院时低氧血症的比率显著降低(47.1% vs 68.1%),P = 0.043。然而,这种效果在有无基础低氧血症的患者中有所不同:合并基础低氧血症的试验组患者的术后低氧血症发生率显著降低(61.1% vs 93.8%),P = 0.042,并且所有时间点的PaO2/FiO2高于对照组,F (1,30) = 6.08,P = 0.019。然而,无基础低氧血症的试验组患者中未观察到这种益处。在低心排血量综合征或急性肾损伤的发生率上未观察到显著差异。试验过程中没有发生重大安全隐患,并且没有观察到中毒水平的高铁血红蛋白。
[结论]合并基础低氧血症患者在心脏手术后接受一氧化氮治疗,可以降低术后低氧血症的发生率,并且术后PaO2/FiO2较对照组升高。两组在术后肺部并发症和总体结果方面未发现显著差异。
[关键词]心脏手术;体外循环;一氧化氮;低氧血症;急性肾损伤
引言
应用体外循环(CPB)的心脏手术会引发显著的全身炎症反应。这将导致多种术后并发症,如肺功能障碍、心肌和肾脏损伤。CPB后肺功能障碍是一种常见并发症,主要表现为低氧血症,其报道的发生率高达54%。肺功能障碍可能延长机械通气时间和ICU住院时间,最终带来重大的经济负担。
心脏手术同样存在心肌损伤的风险,临床表现从短暂的亚临床心肌功能障碍到发展为低心排血量综合征(LCOS)。成人LCOS的患病率从2%到27%不等。急性肾损伤(AKI)是心脏手术的另一种常见并发症。报道的发生率为30%-70%,有2%-5%的患者需要肾脏替代治疗(RRT)。其确切机制尚不明确,可能包括肾脏低灌注、溶血、氧化应激和微循环变化等因素。
多年来,为了减少CPB相关的全身炎症反应,人们做了许多尝试和努力。技术改进方面的尝试包括微创CPB、提高回路的生物相容性、使用超滤和白细胞滤过等。药物治疗方面的研究则涉及自由基清除剂和抗炎药物。一氧化氮是一种具有血管舒张、抗氧化和抗炎特性的关键分子,在各种器官和系统中发挥着重要的保护作用。吸入一氧化氮在治疗新生儿低氧性呼吸衰竭、急性呼吸窘迫综合征、肺动脉高压和肺移植方面具有潜在的优势。然而,吸入一氧化氮的效果是局部的、非全身性的,这促使医生寻找替代的给药途径。在过去的十年中,通过CPB回路输送一氧化氮在文献中受到了相当大的关注。先前的研究表明这种治疗有显著的好处,包括心脏和肾脏保护效果:心脏效应特征为心脏标志物水平降低、减少肌力需求和LCOS的发生率;肾脏效应特征为AKI发生率降低和相关生物标志物减少;但肺部保护效果尚不明确。
为了填补这一空白,本研究旨在调查通过CPB回路输送一氧化氮对成人心脏手术后氧合的影响。
材料和方法
研究设计、环境和伦理
这项前瞻性、单中心、双盲、随机对照试验在以色列贝利森医院的Rabin医疗中心进行。研究于2021年3月获得了Rabin医疗中心机构审查委员会(NO. 0056-21RMC,主席Ran Tur-Kaspa)的伦理批准,并根据CONSORT指南进行报告。试验注册于ClinicalTrials.gov(NCT04807413)。所有参与者都获得了书面知情同意。
入组标准
纳入标准包括:年龄至少18岁的患者,计划进行择期冠状动脉旁路移植术(CABG)、瓣膜或联合手术使用CPB。
排除标准包括:术前存在需要血流动力学支持的休克、需要RRT的终末期肾病、实体器官移植史或肝素诱导的血小板减少症。
研究方案
受试者筛选入组后,独立研究者使用计算机生成的随机序列准备区块分配。每个分配被密封在一个不透明的信封中,并在手术当天由灌注师打开。受试者与所有其他手术室人员都不知道分组情况。受试者被随机分配入组,两组比例为1:1。两组均有一氧化氮输送系统(NOxBOX;Bedfont Scientific Harrietsham,英国)放置在屏幕后面,并连接到CPB氧合器的气体进口。使用Stöckert S5心肺机和Sorin Inspire 6F氧合器(LivaNova PLC,英国伦敦)实施CPB。试验组患者接受40ppm的浓度一氧化氮输送;对照组患者则不被输送一氧化氮。
所有参与者根据机构常规接受麻醉和外科护理。手术期间和CTICU期间的机械通气没有严格规定的方案。通常采用保护性肺策略,以维持足够的氧合(SaO2 > 92%)和通气(EtCO2在35-45 mmHg之间)。根据研究人员所在机构的常规,参与者在CPB期间不进行机械通气,此时的氧合由临床灌注师团队维持在PaO2在200-300 mmHg之间的水平。在CTICU,患者进行气管拔管并过渡到常规氧疗。
结果测量和数据收集
主要结果
术后24小时内低氧血症的发生率。低氧血症定义为PaO2/FiO2比值低于300 mmHg,这是围手术期低氧血症、包括心脏手术后的公认定义,并在多项研究中使用过。
次要结果
术后72小时内LCOS和AKI的发生率。具体定义和测量如下:
低心排血量综合征:在整个CTICU住院期间,转入时和至少每8小时抽取一次血液样本,以评估血乳酸水平和氧摄取率。每6小时记录一次Vasoactive-Inotropic Score(VIS)值,直到转出。LCOS通过满足以下标准之一来确认:VIS值至少为15;血乳酸水平超过4 mmol/L,同时氧摄取率高于35%。
急性肾损伤:使用Cockcroft-Gault方程确定基线估计的肾小球滤过率,来定义慢性肾脏病(CKD)阶段。每天测量血肌酐水平,直到术后第三天(POD)。AKI根据血肌酐水平和改善全球肾脏疾病预后组织(KDIGO)临床实践指南定义。
数据收集
研究收集了术前基线数据,包括患者特征(即年龄、性别和BMI);美国麻醉医师协会(ASA)身体状况评分;基线肺部状况(即COPD/哮喘、吸烟状况、基础低氧血症和PaO2/FiO2比值);基线心脏状况[即纽约心脏病学会(NYHA)分类、高血压病史、缺血性心脏病、左心室射血分数(LVEF)、右心室功能障碍和肺动脉高压];基于CKD分期的基线肾脏状况;糖尿病;合并用药(即抗高血压药、他汀类药物、抗血小板药物和利尿剂);以及胸外科医师学会(STS)评分,这是手术死亡率/发病率风险的衡量指标。术中数据包括手术类型(即CABG、瓣膜或联合手术);手术、CPB和主动脉阻断时间;CPB期间的尿量;血制品使用情况。术后数据包括低氧血症、LCOS和AKI的发生率;并发症,包括心脏(例如,心律失常、填塞、机械循环支持);肺部(机械通气时间、延长机械通气时间(>72小时)、拔管后需要高流量鼻氧(HFNO)、再插管率和胸膜积液发生率;中风;和手术部位感染(胸骨或隐静脉);以及术后结局(即再入院率、CTICU和住院时间,以及30天死亡率)。
统计分析
使用直方图和QQ图目测评估变量分布,随后使用Shapiro-Wilk检验检查正态性假设。使用描述性统计数据总结数据。分类变量以计数和百分比表示,而数值变量以均值和标准差或中位数和四分位间距[IQR]表示。
使用Mann-Whitney U检验比较连续变量。Fisher精确检验和卡方检验用于评估分类变量的差异。进行多变量逻辑回归模型分析,其中因变量是术后CPB、CTICU入院和拔管前低氧血症的存在,而自变量包括基础低氧血症、预先存在的哮喘/COPD、手术类型、CPB持续时间和使用一氧化氮。最后,进行亚组分析,以评估一氧化氮对有和无基础低氧血症患者的术后肺部并发症和结果的影响。重复测量方差分析(ANOVA)用于检查在不同时间点测量的PaO2/FiO2比值的差异。双向ANOVA用于评估在单一时间点测量的连续变量之间的差异。所有统计检验的显著性水平为P值小于0.05。使用Python编程语言、MATLAB R2021b软件(The MathWorks,Natick,USA)和RStudio统计软件(版本4.2.2,R Foundation,Vienna,Austria)进行统计分析。
关于样本量计算,鉴于缺乏有关此主题的先前文献,最初根据专家意见和实际考虑建议300名患者的样本量。然而,由于COVID-19大流行大幅减缓了登记速度并限制了可用资源,因此未能实现预期的样本量。最初为这项研究准备的大多数分配的一氧化氮输送系统被用于重症COVID-19患者。这种情况因资金不足而进一步加剧,最终导致在招募了100名患者后过早终止了研究。
为了应对这些情况,研究人员进一步进行了回顾性样本量计算。结果表明,为了检测到低氧血症患者比例的小幅差异(效应量为0.35)和80%的功率,258名患者的样本量,每组129名患者就足够了。为了检测中等到大的效应量(效应量为0.6及以上)和80%的功率,所需的样本量将是88名患者,每组44名(参见补充表S1,http://links.lww.com/EJA/A977和图S1,http://links.lww.com/EJA/A976)。样本量计算是使用PASS 15(2017年能力分析和样本量软件,NCSS,LLC。Kaysville,Utah,USA,ncss.com/software/pass)执行的。
结果
在2021年8月至2023年3月期间,研究人员共筛选了132名患者,其中98名被纳入最终分析。47名患者被分配到对照组,51名被分配到试验组。患者招募图如图1所示。
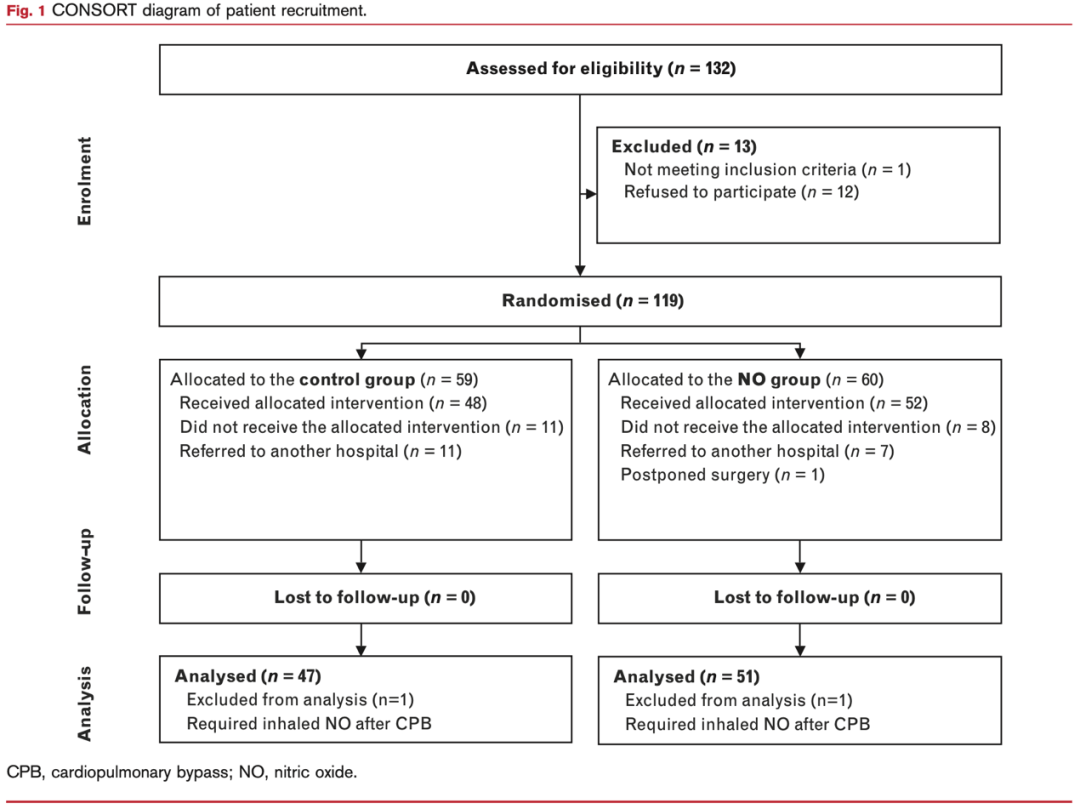
图1 CONSORT患者招募图
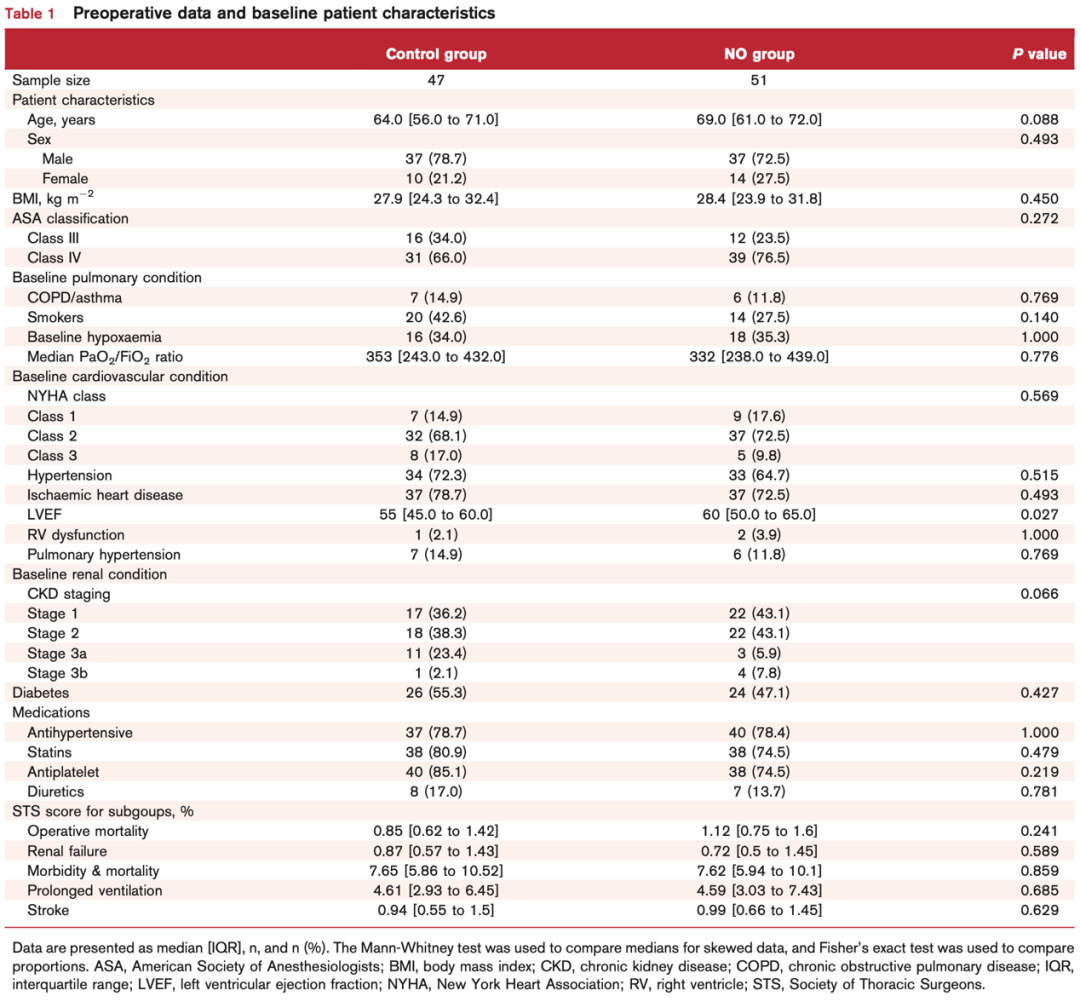
两组之间术前左心室射血分数具有显著差异,对照组为55(45.0-60.0)%,试验组为60(50.0-65.0)%,P = 0.027。但考虑到两个值都在正常范围内,研究人员认为这个差异的临床意义有限。两组之间的其他术前数据和基线特征没有显著差异(表1)。对照组34%的患者和试验组35.3%的患者存在基础低氧血症。
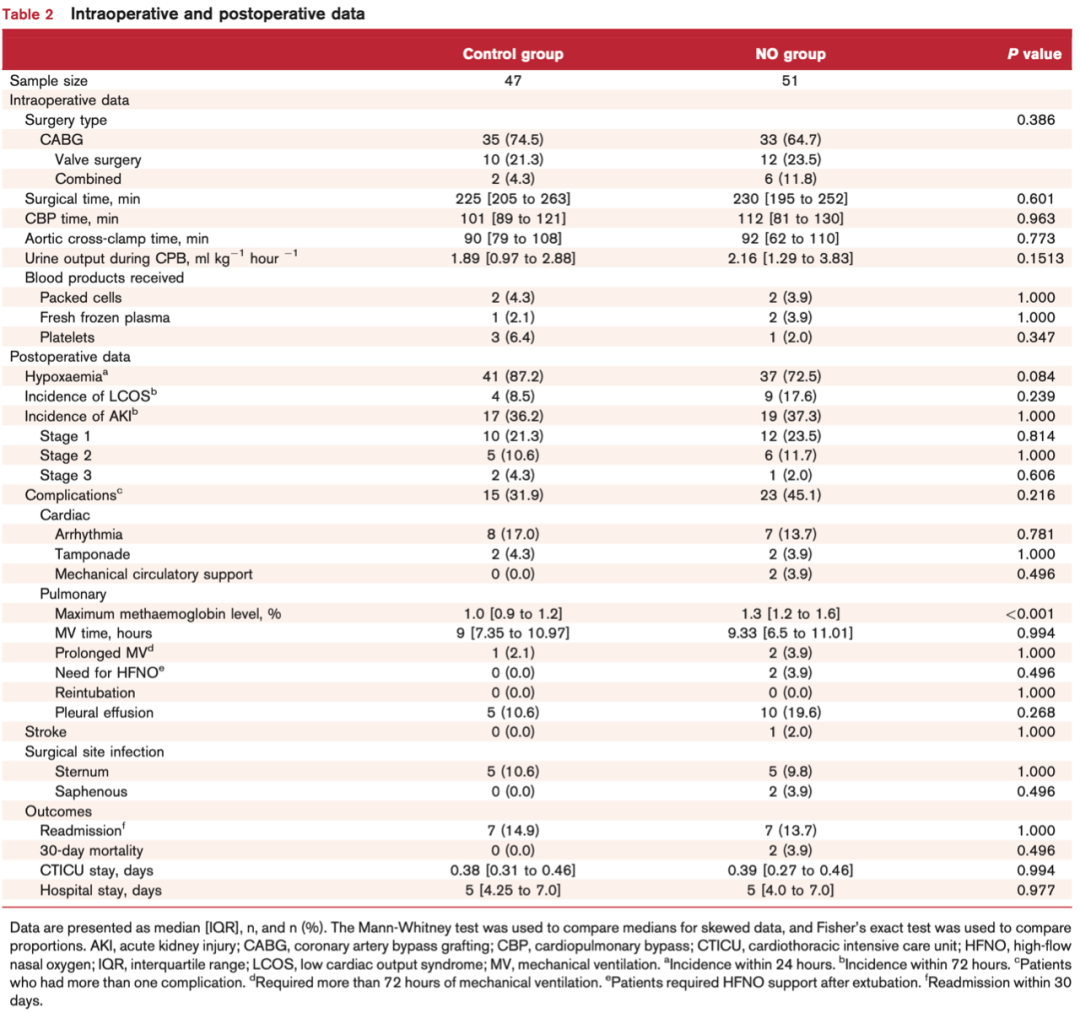
两组的术中数据,包括手术类型、手术持续时间、CPB和主动脉阻断时间、以及血制品使用情况,没有显著差异(表2)。
低氧血症
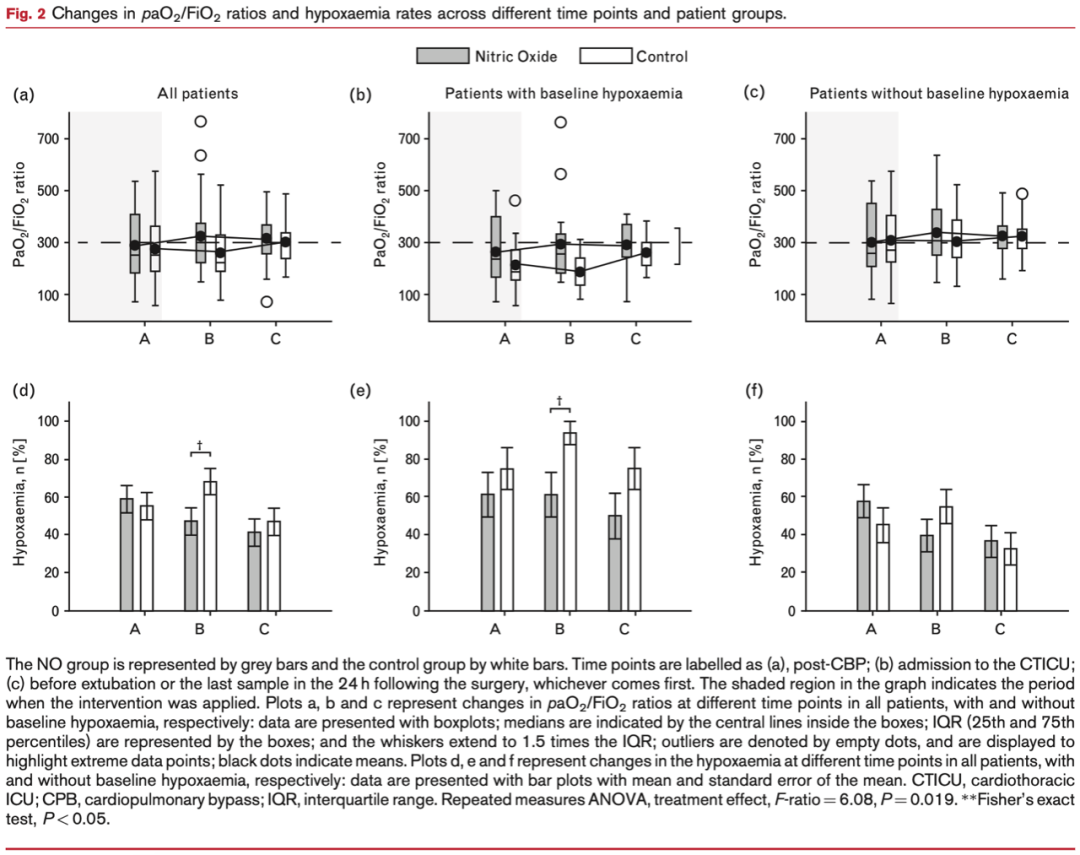
对照组有41(87.2%)的患者发生了低氧血症,试验组有37(72.5%)患者发生,P = 0.084(表2)。在CTICU入院时,试验组表现出更低的低氧血症发生率(47.1% vs 68.1%),P = 0.043,图2d)。但是逻辑回归分析显示一氧化氮(OR 0.29,95% CI = 0.091-0.911,P = 0.034)和基础低氧血症(OR 5.59,95% CI = 1.40-22.4,P = 0.015)对总体低氧血症比率有显著影响。因此,研究人员进行了亚组分析,以阐明一氧化氮对不同基线水平(合并/不合并基础低氧血症)患者的术后结局的影响(表3和表4)。无基础低氧血症患者的总体低氧血症发生率在两组间相似[22 (66.6%) vs 25 (65.6%),P = 0.263]。无基础低氧血症的患者中,对照组和试验组在CTICU入院时的低氧血症比率没有差异,分别为54.8%和39.4%,P = 0.316(图2f)。然而,在有基础低氧血症的患者中,一氧化氮治疗后使低氧血症的发生率显著降低(61.1% vs 93.8%,P = 0.043),效应量为-0.33,95% CI(-0.64,-0.01),P = 0.025(参见补充表S2,http://links.lww.com/EJA/A978)。同样地,无基础低氧血症的患者中没有观察到一氧化氮治疗或PaO2/FiO2测量时间对结果的影响,F (1,62) = 0.20,P = 0.658和F (2,123) = 1.01,P = 0.367,分别(图2c)。然而,在有基础低氧血症的患者中研究结果观察到一氧化氮治疗的显著影响,F (1,30) = 6.08,P = 0.019。
低心排血量综合征
手术后72小时内,对照组有4(8.5%)患者和试验组有9(17.6%)患者发展为LCOS,P = 0.239(表2)。
急性肾损伤
手术后72小时内,对照组有17(36.2%)患者和试验组有19(37.3%)患者发展为AKI,P = 1.000。在对照组中,有10名患者(占21.3%)出现了AKI 1期,试验组有12名患者(占23.5%)出现了同样的情况,但这一差异在统计学上并不显著(P = 0.814)。对于AKI 2期,对照组有5名患者(占10.6%)受到影响,试验组有6名(占11.7%),统计学上同样没有显著差异(P = 1.000)。至于AKI 3期,对照组有2名患者(占4.3%)发生,而试验组仅有1名患者(占2.0%)受到影响,这一差异也不具有统计学意义(P = 0.606)。
术后结局
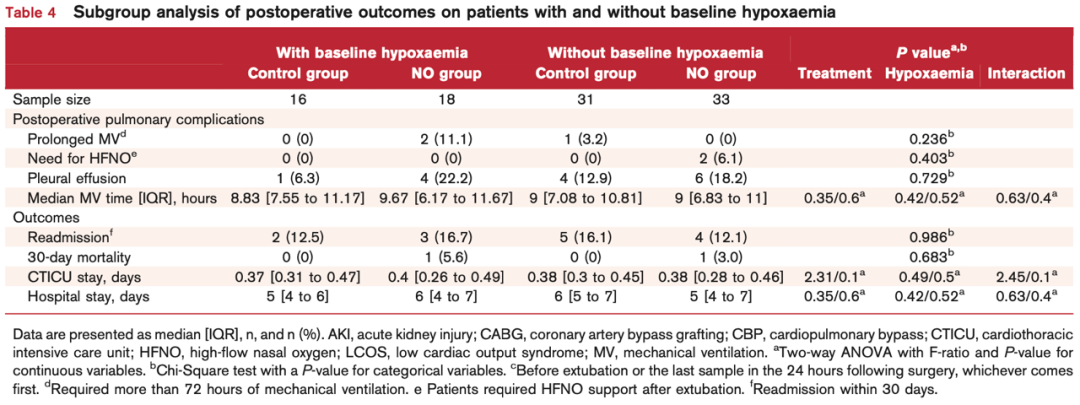
表4展示了有无基础低氧血症的患者在接受一氧化氮治疗后的肺部术后结果。两组在术后并发症发生率上没有显著差异(表2)。总体而言,对照组中有15(31.9%)名患者,试验组中有23(45.1%)名患者出现了不止一种并发症,但这一比例差异在统计学上并不显著(P = 0.216)。除了试验组中有2(3.9%)名患者在拔管后需要接受高流量鼻导管氧疗(HFNO)外,其他患者均接受了常规氧疗,这一差异同样没有统计学意义(P = 0.496)。对照组的高铁血红蛋白的平均最大浓度为1.0(0.9,1.2),试验组为1.3(1.2,1.6),P < 0.001。在机械通气的时间、再插管率、CTICU停留时间以及住院时间方面,两组之间没有观察到明显差异。试验组中有2名患者在30天内死亡。
讨论
低氧血症
低氧血症是CPB期间常见的肺部功能障碍之一,其成因复杂且多样。CPB启动时,肺部除了遭受肺泡塌陷的影响,还可能因为支气管循环供血不足而出现相对缺血。体外循环相中血液与人工管道接触会激发炎症反应,这一过程会激活补体系统和凝血途径,引发炎症细胞因子和氧自由基的释放,最终导致血管内皮细胞受损。这种损伤会破坏肺泡与内皮细胞之间的屏障,引起渗透性肺水肿,影响肺泡表面活性物质的产生,降低肺顺应性。主动脉开放之后,缺血再灌注损伤会进一步加剧炎症反应。此外,由于微血管循环受损和无再流现象,可能会触发细胞凋亡。为了中和肝素,CPB最后通常会使用鱼精蛋白,这会导致肝素-鱼精蛋白复合物的形成。这种复合物可能会增加肺血管的阻力,进而造成通气与血流之间的不匹配。一氧化氮对于器官保护具有重要作用,但在CPB期间,由于非脉冲式血流、全身炎症反应和血管内溶血的影响,一氧化氮的自然产生和利用会减少。因此,在CPB早期给予外源性一氧化氮可能有助于减轻炎症反应,降低器官损伤的风险。此外,一氧化氮的应用还可能有助于缓解由鱼精蛋白引起的肺血管阻力增加。
这是首项探讨经CPB回路输送一氧化氮对成人心脏手术患者低氧血症影响的研究。本研究结果表明,接受一氧化氮治疗的患者低氧血症的发生率显著下降。然而,这种效果在合并/不合并基础低氧血症的患者之间存在差异。具体来说,那些有基础低氧血症的患者在接受一氧化氮治疗后,不仅低氧血症的发生率降低了,而且PaO2/FiO2也有所提高。而在没有基础低氧血症的患者中并没有观察到这种益处。虽然对于肺功能正常的患者而言,这种效果可能在临床上并不显著,但对于肺功能不佳的患者来说,这可能是一个显著的进步。在安全性方面,尽管治疗组的血高铁血红蛋白水平有所上升,但增加的水平仍在安全范围内。然而,尽管这些结果表现出一定的正面趋势,但此次研究未能证实这种治疗在广泛临床应用中的效果,因为在术后肺部并发症和患者总体预后方面并未发现显著差异。
在一项相关研究中,Schlapbach等研究者开展了一项双盲随机临床试验,涉及1371名接受先天性心脏手术的儿童。这项研究旨在评估以20 ppm浓度输送一氧化氮对患者无呼吸机天数的影响。研究结果显示,两组间的无呼吸机天数并没有显著性差异。由于该研究的主要对象是接受先天性心脏手术的儿童,因此其结果难以直接推广至普通人群。
低心排血量综合征
研究人员计划评估72小时内的LCOS发生率,但大多数患者在24小时内出院,因此无法收集后续数据。研究人员推测出院患者未发生LCOS,但未进行深入评估。实际上,只有三名患者在24小时后仍留在CTICU,两名患者在手术后第二天转出,而一名患者在手术后第三天仍然在CTICU。最终,13.3%的患者出现LCOS(对照组8.5%,试验组17.6%),与既往研究一致。尽管试验组LCOS的发生率较高,但差异无统计学意义。
与本次研究的结果不同,James等人在研究中给198名接受先天性心脏手术的儿童在CPB期间使用一氧化氮,他们发现试验组LCOS的发生率较低。然而,这种效果主要见于2岁以下的儿童和那些接受复杂手术的患者。在Kamenshchikov等人的另一项随机临床试验中,他们研究了60名接受冠状动脉旁路移植术(CABG)的成人使用一氧化氮的效果,发现试验组在术后6小时的肌钙蛋白水平和VIS值显著降低。本研究的结果与其他研究不一致的原因可能在于研究人群和手术类型的不同。另一个可能的解释是,试验组中较高的VIS评分可能是由于一氧化氮强烈的血管舒张效应所致。
急性肾损伤
在本研究中,术后AKI的总发生率为36.7%,其中对照组为36.2%,试验组为37.3%,这与以往的研究结果相符。研究结果并未显示一氧化氮对降低术后AKI发生率及其严重程度有保护作用,这与一些其他研究的发现不同。例如,Lei等人在评估一氧化氮对成人多瓣膜心脏手术患者影响的研究中发现,使用一氧化氮能将AKI的发生率从64%降至50%,并减少一年内发展至3期CKD和主要不良肾脏事件的风险。
本研究与Lei等人的研究存在几个关键差异。首先,Lei等人的研究聚焦于瓣膜手术,这类手术本身具有较高的AKI风险。其次,一氧化氮的给药方式和剂量有所不同:本研究在CPB期间使用了40 ppm的剂量,而Lei等人在CPB期间使用了80 ppm的剂量,并在术后继续给予一氧化氮24小时。此外,本研究观察到的AKI发生率明显低于Lei等人报道的初始发生率。
Kamenshchikov等人的另一项研究则比较了60名接受择期心脏手术的成人在给予一氧化氮与标准护理后的效果,发现给予一氧化氮与AKI发生率显著降低相关(41.6% vs 20.8%),并且CPB期间尿量有所增加。导致这些结果差异的可能原因之一是两组研究对象发展为术后AKI的风险不同。尽管本研究的队列特征通常与较高的风险相关,如年龄较大、男性为主、糖尿病、CKD和较差的NYHA分级,但根据预测模型的评估结果,本研究的队列被认为是较低风险的。Kamenshchikov等人使用了克利夫兰诊所评分来预测需要肾脏替代治疗(RRT)的AKI风险,而本研究则使用了STS评分来预测AKI 3期的风险。根据这些预测模型,Kamenshchikov等人的队列风险为中等(1.8%),而本研究的队列为低风险(0.72%)。这种差异可能与手术类型有关,因为Kamenshchikov等人的队列中涉及了更多的联合手术(25%),而本研究中这一比例为11.8%,这显著影响了AKI的风险。
局限性
本项研究存在几个限制。首先,本研究未能达到预期的样本量,而更大的样本量可能会带来更加可靠和确定的研究结果。其次,由于研究仅在单一中心进行,这可能引入了某些偏差,并且可能限制了研究结果在更广泛人群中的应用。第三,缺乏关于机械通气的严格协议,这可能导致了结果的变异性,并可能对研究结论产生了影响;未来的研究若能实施标准化的通气协议,可能会从中受益。最后,在研究人员所在的医疗机构中,进行心脏手术时通常不将心脏指数作为LCOS诊断的一部分,因为并未常规使用高级心脏监测设备。这可能会影响到本项研究结果与其他研究结果的可比性,也可能限制了研究人员发现在更广泛情况下的适用性。
结论
本研究结果表明,基础低氧血症的患者在心脏手术后接受一氧化氮治疗能降低低氧血症发生率并升高PaO2/FiO2。然而,在术后肺部并发症和总体结果上未发现显著差异。未来的大规模研究应该专注于研究这种干预对肺功能受损的患者群体的临床意义。
参考文献
Azem K, Novakovsky D, Krasulya B, et al. Effect of nitric oxide delivery via cardiopulmonary bypass circuit on postoperative oxygenation in adults undergoing cardiac surgery (NOCARD trial): a randomised controlled trial.Eur J Anaesthesiol. 2024;41(9):677-686. doi:10.1097/EJA.0000000000002022
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#心脏手术# #体外循环# #一氧化氮# #低氧血症#
80