Lancet Oncol:帕博利珠单抗联合化疗放疗在局部晚期头颈鳞状细胞癌中的疗效和安全性:KEYNOTE-412 试验结果
2024-06-27 daikun MedSci原创 发表于加利福尼亚
该研究旨在评估帕博利珠单抗联合化疗放疗与单纯化疗放疗相比在局部晚期 HNSCC 患者中的疗效和安全性,帕博利珠单抗联合化疗放疗并未显著改善分子未选择的局部晚期HNSCC患者的无事件生存期。
头颈部鳞状细胞癌(HNSCC)是一种常见的恶性肿瘤,包括口腔、咽部、喉部等部位的癌症,许多患者确诊时已处于局部晚期,化疗放疗或手术加放疗是标准治疗方案,然而,即使接受治疗,许多局部晚期 HNSCC 仍会复发,尤其是非口咽部或人乳头瘤病毒(HPV)阴性口咽部癌症,帕博利珠单抗是一种抗 PD-1 单克隆抗体,已获批用于治疗不可切除的复发性或转移性 HNSCC,早期研究表明,将帕博利珠单抗添加到化疗放疗中是可行的,并且不会限制治愈性放疗或化疗的交付,该研究(KEYNOTE-412)旨在评估帕博利珠单抗联合化疗放疗与单纯化疗放疗相比,在局部晚期 HNSCC 患者中的疗效和安全性。

方法
KEYNOTE-412 试验是一项随机、双盲、3 期临床试验,纳入患者年龄 18 岁或以上,新诊断的、病理证实的、高危、不可切除的局部晚期 HNSCC,之前未接受过治疗,具有可评估的肿瘤负荷, ECOG体能状态为 0 或 1,患者按照 1:1 的比例随机分配到帕博利珠单抗组或安慰剂组。帕博利珠单抗组:帕博利珠单抗 200 mg,每 3 周静脉注射一次,最多 17 剂(化疗放疗前 1 剂,化疗放疗期间 2 剂,化疗放疗后 14 剂作为维持治疗),顺铂 100 mg/m²,每 3 周静脉注射一次,2 或 3 剂加速分割放疗(70 Gy 分 35 次给予)或标准分割放疗(70 Gy 分 35 次给予);安慰剂组:安慰剂每 3 周静脉注射一次,最多 17 剂,化疗放疗方案与帕博利珠单抗组相同。主要终点为无事件生存期(EFS),次要终点为总生存期、安全性。
研究结果
帕博利珠单抗组和安慰剂组的 EFS 中位值分别为未达到(95% CI 44.7 个月–未达到)和 46.6 个月(27.5–未达到),风险比为 0.83(95% CI 0.68–1.03),p 值为 0.043。中位 OS分别为 72%和70%,风险比 (HR)为0.90 (95% CI 0.71–1.15)。
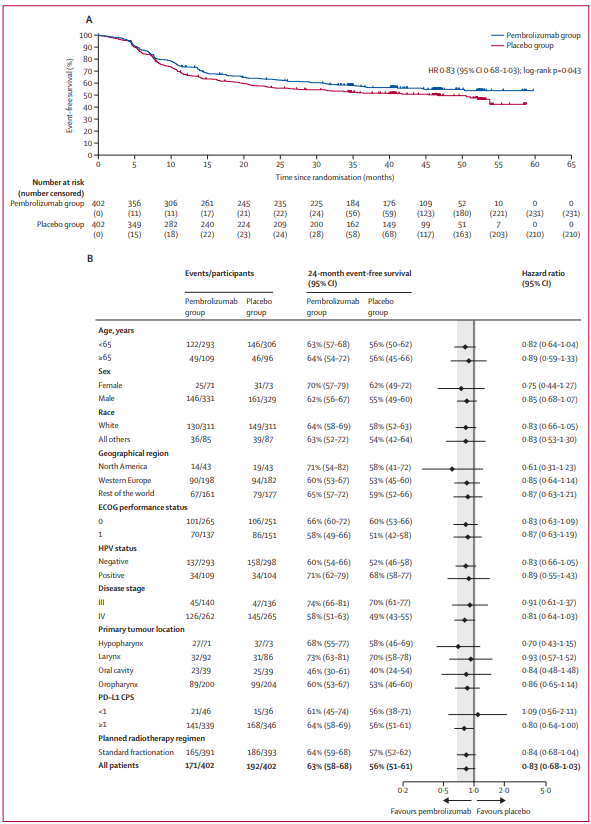

安全性分析
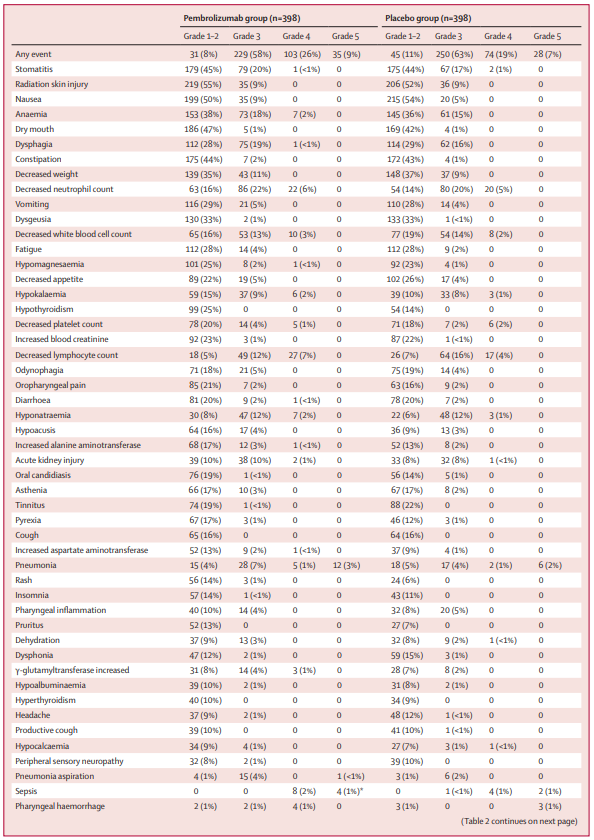
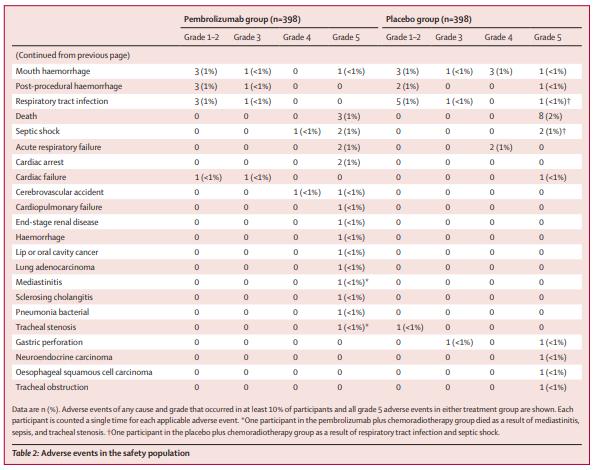
帕博利珠单抗组和安慰剂组分别有 92% 和 88% 的患者出现 3 级或更高级别的副作用,有 62% 和 49% 的患者出现严重不良事件,有 1% 和 2% 的患者死于与治疗相关的不良事件。最常见的 3 级或更高级别不良事件包括:中性粒细胞减少、口腔炎、贫血、吞咽困难、淋巴细胞减少。帕博利珠单抗组和安慰剂组的安全性特征总体上与已知单个治疗成分的不良事件特征一致,没有发现新的安全性信号。
结论
KEYNOTE-412 试验的结果表明,帕博利珠单抗联合化疗放疗并未显著改善分子未选择的局部晚期 HNSCC 患者的无事件生存期,帕博利珠单抗联合化疗放疗的安全性特征总体上与已知单个治疗成分的不良事件特征一致,没有发现新的安全性信号,局部晚期 HNSCC 仍然是一种具有挑战性的疾病,需要更好的治疗方法
原始出处
Machiels J-P, et al. 2024. Pembrolizumab plus concurrent chemoradiotherapy versus placebo plus concurrent chemoradiotherapy in patients with locally advanced squamous cell carcinoma of the head and neck (KEYNOTE-412): a randomised, double-blind, phase 3 trial. The Lancet Oncology 25:572-587.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#放化疗# #头颈鳞状细胞癌# #帕博利珠单抗#
2