Mol Cell:杜立林实验室发现一种新的基因组保护机制
2017-05-31 佚名 北京生命科学研究所
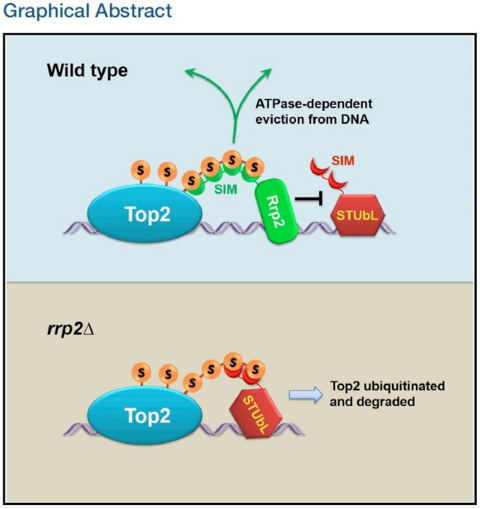
2017 年 5 月 25 日,我所杜立林实验室在《Molecular Cell》在线发表题为“SUMO-Targeted DNA Translocase Rrp2 Protects the Genome from Top2-Induced DNA Damage”的研究论文。该论文发现一个名为 Rrp2 的 DNA 移位酶通过阻止 DNA 拓扑异构酶Ⅱ(Top2)的降解来避免 Top2 毒剂(To
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#Cell#
31
#CEL#
27
高端技术值得好好学习不研究,谢谢作者
51
学习了,谢谢作者分享!
67