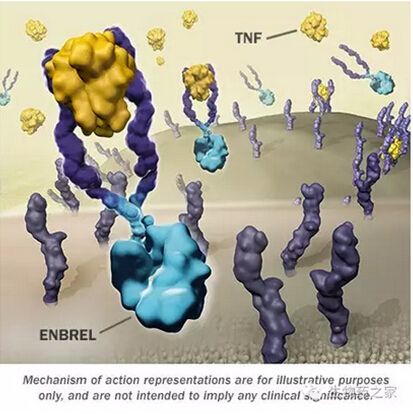
Enbrel生物类似药Erelzi获FDA批准上市
8月30日,FDA宣布批准诺华旗下Sandoz开发的Enbrel(etanercept)生物类似药上市,商品名Erelzi(etanercept-szzs),用于治疗多种炎症疾病,成为FDA批准的第三个生物类似药
生物药之家 - Enbrel,生物类似药,FDA - 2016-08-31
拜耳Eylea新适应症获欧盟批准
拜耳(Bayer)8月29日宣布,眼科药物Eylea(aflibercept,阿柏西普注射液)新适应症申请获欧盟委员会(EC)批准,用于治疗视网膜中央静脉阻塞(central retinal vein这是Eylea在欧洲获批的第二个适应症,此前,Eylea已获EC批准用于湿性年龄相关性黄斑变性(we
生物谷 - 新药,FDA - 2013-08-30
FDA批准儿童使用可穿戴除颤器
FDA批准 LifeVest可穿戴心脏复律除颤器用于有即刻心脏骤停风险的儿童,在特定的医疗条件或父母不同意的情况下不可使用该设备。
MedSci原创 - 除颤,可穿戴,心室颤动 - 2015-12-21
默沙东HIV新药Delstrigo和Pifeltro获得FDA批准上市
MSD的HIV药物Delstrigo和Pifeltro被FDA批准用于没有抗逆转录病毒治疗经验的成年患者。
MedSci原创 - HIV,MSD,FDA,NMRIT - 2018-08-31
欧洲药管局或将批准血液药物Jakavi
诺华公司和Incyte公司表示,欧盟监管机构已被建议批准他们的血液疾病药物Jakavi。 欧洲药品管理局人用药品委员会建议批准Jakavi来治疗患骨髓纤维化这一血液疾病患者的脾肿大。Jakavi的用法为每日两次。
前沿医学 - 欧洲药管局,骨髓纤维化,脾肿大,Jakavi - 2012-04-27
FDA批准单抗药Arzerra治疗复发性CLL
Genmab制药公司称,单抗药物Arzerra(ofatumumab,奥法木单抗)补充生物制品许可(sBLA)获FDA批准,作为至少对二线治疗有反应的复发或进展的慢性淋巴细胞白血病(CLL)患者的维持治疗FDA批准该许可是基于PROLONG (OMB112517)Ⅲ期试验数据,该研究对二三线治疗有反应的CLL患者比较了奥法木单抗维持治疗和不治疗两种情况。该研究共纳入474名患者,研究结果显示,奥
MedSci原创 - FDA,Arzerra,CLL,奥法木单抗 - 2016-01-21
FDA批准下一代测序基因 技术
2月19日,美国药品管理局(FDA)批准了"23 and me"公司发明的,对引起"布鲁姆综合征"(一种可能导致身材矮小并伴随高发性癌症的疾病)的主效基因进行检测手段。
生物谷 - FDA,测序,基因检测 - 2015-02-25
FDA批准美国首个恰加斯病治疗药物
美国食品和药物管理局(FDA)已经加速批准苄硝唑用于治疗患有恰加斯病的2~12岁儿童,成为美国批准用于这种罕见病的首个治疗方法。
环球医学 - FDA,恰加斯病,药物 - 2017-08-30
FDA批准首个治疗Low T鼻用凝胶药物
FDA在5月28日批准了由加拿大生物技术公司Trimel Pharmaceuticals开发的用于治疗男性性腺功能低下症药物Natesto。这也是首个获得批准的利用呼吸道作为给药途径的治疗此类疾病的药物。而对Trimel Pharmaceuticals来说,这一批准更显得弥足珍贵,因为今年年初,公司资金仅剩下1800万美元。
生物谷 - FDA,鼻用凝胶药物 - 2014-06-05
FDA批准Vascepa治疗高甘油三酯血症
2012年7月26日,美国食品与药物管理局(FDA)批准专利合成药乙基二十五碳五烯酸(EPA)(Vascepa,既往称为AMR101)用于治疗高甘油三酯血症,Vascepa成为市场上第二个
医学论坛网 - 高甘油三酯血症,Vascepa,胆固醇 - 2012-08-02
FDA批准转基因鸡,用于生产罕见病药物
美国食品药品监督管理局(FDA)如今批准利用一种转基因鸡产下的蛋制造一种药物Kanuma 。 经12月8日由FDA批准,Kanuma加入了美国市场的一小群“特殊药物”之中。
中国科学报 - FDA,转基因 - 2015-12-14
美批准免疫疗法治疗非小细胞肺癌
中国科学报 - 2016-11-03
关于组织申报2015年度安徽省自然科学基金计划项目的通知
各有关单位:根据《安徽省自然科学基金管理办法》有关规定,现将2015年度省自然科学基金计划的申报组织工作及有关事项通知如下:一、申报项目类别及资助对象本次组织申报的项目类别包括青年科学基金项目(以下简称青年项目
安徽省自然科学基金办 - 自然科学基金,安徽省 - 2014-03-31
FDA初步批准Spectrum治疗淋巴瘤药物Beleodaq
美国FDA最近宣布初步批准由Spectrum生物医药公司开发的用于治疗T细胞淋巴瘤药物belinostat上市,这种药物将以Beleodaq的商品名出售。此次批准的Beleodaq是一种组蛋白脱乙酰酶抑制剂。也是自2009年至今批准的第三种治疗这种疾病的药物。这一药物的批准也意味着Spectrum公
不详 - 淋巴瘤药物,Spectrum - 2014-07-07
为您找到相关结果约500个