浙江大学顾臻、张宇琪等《Adv. Sci.》综述:微针器件介导的细胞疗法
2023-11-02 BioMed科技 BioMed科技 发表于上海
本综述概述了微针介导的细胞递送用于免疫治疗、组织再生和激素调节的最新进展,主要围绕微针制备方法、机械性能、细胞负载能力以及负载细胞的活力和生物活性等方面展开阐述。
近年来,基于微针器件的透皮给药系统作为口服和肠外给药等传统给药途径的替代方案引起越来越多的关注。微针通过物理穿透角质层屏障产生微孔,促进小分子药物、核酸、多肽和蛋白质等治疗性药物有效运输到真皮下层。除了促进传统药物的透皮转运外,微针在近年的研究中也被用于细胞治疗。细胞治疗涉及活细胞的递送或移植,它为疾病提供了前瞻性的治疗选择。然而,细胞的组织渗透和积聚能力有限,并且细胞本身的不稳定性也阻碍了相关细胞疗法的临床转化。

近日,浙江大学顾臻教授/张宇琪研究员团队受《Advanced Science》杂志邀请,发表了题为“Microneedle-Mediated Cell Therapy”的综述文章。顾臻团队在国际上率先将微针递送技术与细胞疗法相结合,本综述概述了微针介导的细胞递送用于免疫治疗、组织再生和激素调节的最新进展,主要围绕微针制备方法、机械性能、细胞负载能力以及负载细胞的活力和生物活性等方面展开阐述。最后,本文讨论了微针介导的细胞疗法的主要挑战和未来前景。
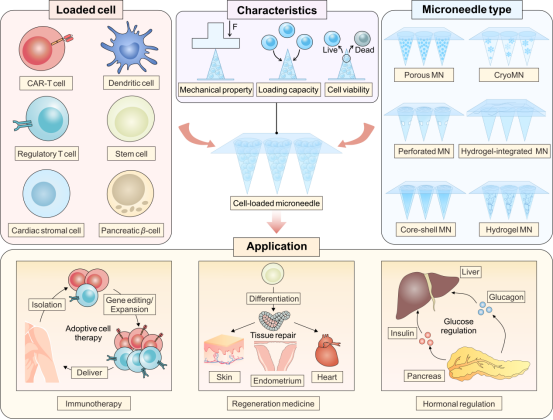
图1 微针介导的细胞递送用于免疫治疗、再生医学和激素调节
细胞制剂近年来作为新兴生物制剂在众多临床应用中取得了突破性进展,包括细胞免疫治疗、干细胞疗法等。然而,CAR-T细胞等免疫细胞虽然能够直接清除靶细胞或引起免疫反应,相比于常规治疗方法已显示出临床优势,但复杂的肿瘤微环境和物理屏障使得免疫细胞在实体肿瘤的治疗应用中受到了限制。
此外,干细胞、胰岛细胞等治疗性细胞在直接注射或手术植入时常伴有组织损伤或免疫排斥反应,通过这些方法递送的治疗性细胞通常具有有限的驻留时间、不理想的归巢效果等。针对这些挑战,作者重点介绍了负载免疫细胞、干细胞、胰岛细胞的微针在免疫治疗、组织再生和激素调节方面的代表性工作。在免疫治疗方面,微针的使用增强了细胞的组织靶向性和浸润,可诱导更强的免疫应答;在组织再生方面,微针通过穿透组织,直接将干细胞运送到目标部位,延长了细胞的驻留时间,并克服全身免疫反应,为移植提供了可行性;在激素调节方面,规避了胰腺细胞治疗中免疫反应和长期疗效相关的问题。
这类基于微针器件的细胞递送平台可以增强细胞的靶向递送、较好地维持细胞活性,以及降低系统毒性,以提升治疗效果。相关技术的转化主要聚焦在细胞稳定性、器件均一性以及大规模生产等方面。
原文链接:
https://onlinelibrary.wiley.com/doi/10.1002/advs.202304124
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言