Biological Psychiatry:配对线索调节多巴胺神经元敏化对决策和可卡因自我给药在不同性别中的影响
2023-09-12 xiongjy MedSci原创 发表于上海
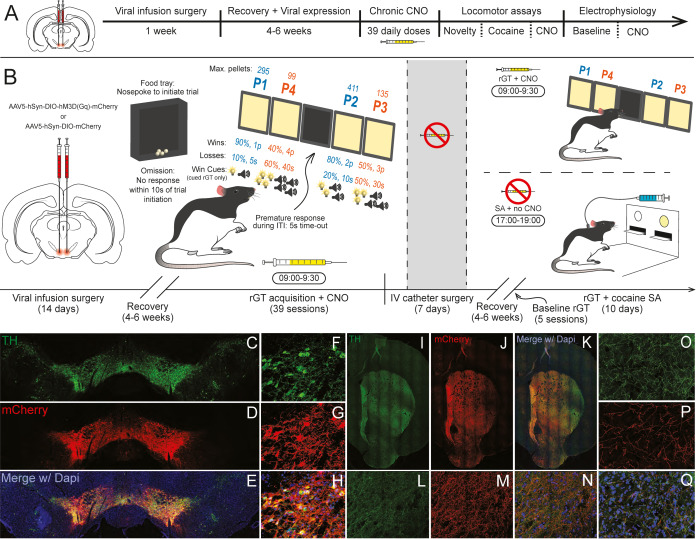
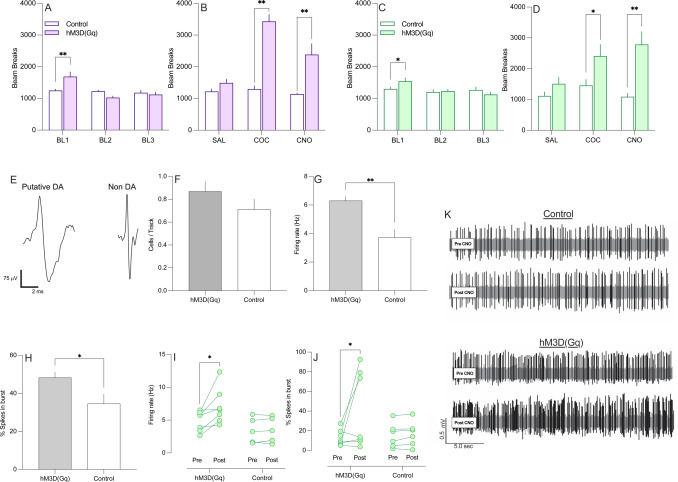
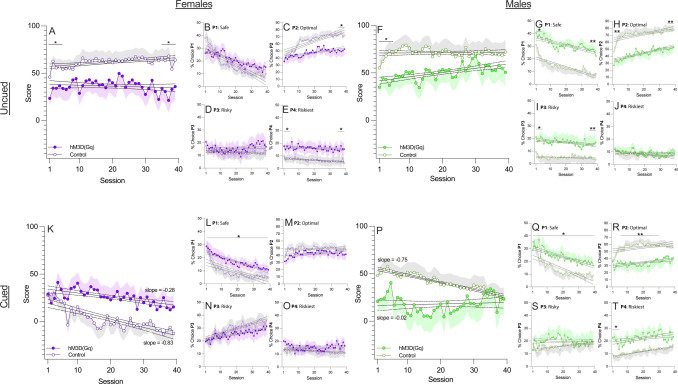
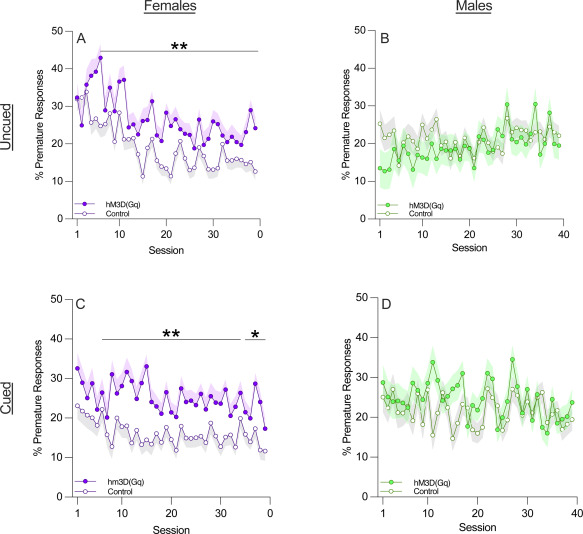
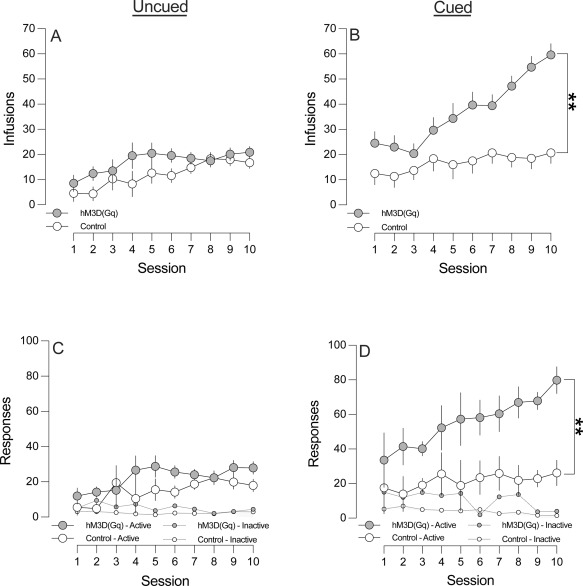
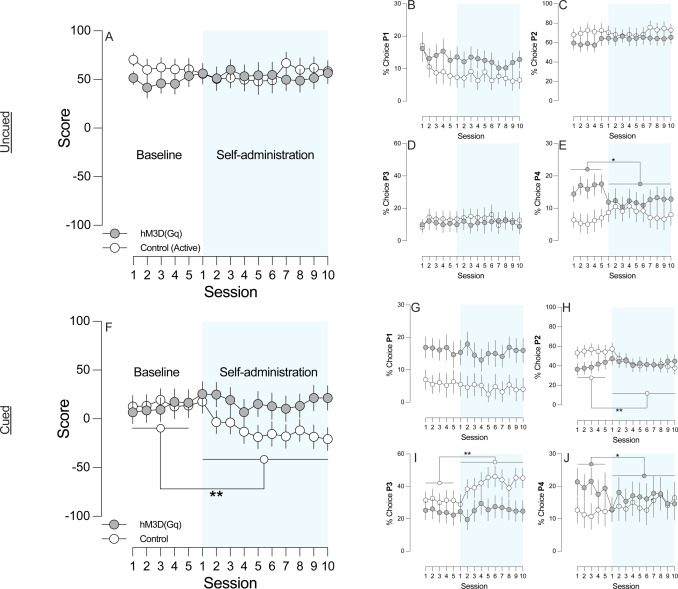
在多巴胺系统水平上,参与重度提示赌博游戏与吸食可卡因之间存在协同作用,这表明存在交叉依赖的途径。女性和男性对多巴胺信号变化反应存在关键差异。

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言