Mol Cancer:山东大学冯强团队揭示了癌症相关成纤维细胞与肿瘤微环境之间的串扰
2023-10-26 医药加学习班 医药加学习班 发表于上海
该研究通过泛肿瘤空间分辨单细胞分析揭示了癌症相关成纤维细胞与肿瘤微环境之间的串扰。
癌症相关成纤维细胞(CAFs)是一种异质性细胞群,在重塑肿瘤微环境(TME)中起着至关重要的作用。
2023年10月13日,山东大学冯强团队在Molecular Cancer在线发表题为“Pan-cancer spatially resolved single-cell analysis reveals the crosstalk between cancer-associated fibroblasts and tumor microenvironment”的研究论文,该研究通过泛肿瘤空间分辨单细胞分析揭示了癌症相关成纤维细胞与肿瘤微环境之间的串扰。
该研究通过对六种常见癌症类型的空间和单细胞转录组学数据的综合分析,确定了四个不同的CAFs功能亚群,并描述了它们的空间分布特征。此外,对另外三种常见癌症类型的单细胞RNA测序(scRNA-seq)数据和两种新生成的罕见癌症类型(即上皮-肌上皮癌(EMC)和粘液表皮样癌(MEC))的scRNA-seq数据集进行分析,扩大了人们对CAF异质性的理解。在空间背景下进行的细胞-细胞相互作用分析强调了基质CAFs (mCAFs)在肿瘤血管生成中的关键作用,以及炎症CAFs (iCAFs)在形成免疫抑制微环境中的关键作用。在接受抗PD-1免疫治疗的乳腺癌(BRCA)患者中,iCAFs显示出促进癌细胞增殖、促进上皮-间质转化(EMT)和促进免疫抑制微环境建立的能力增强。此外,基于iCAFs的评分系统显示黑色素瘤患者的免疫治疗反应显著相关。

肿瘤表现出广泛的异质性,癌细胞与其微环境相互作用,形成复杂的生态系统。癌相关成纤维细胞(Cancer-associated fibroblasts, CAFs)作为肿瘤微环境(tumor microenvironment, TME)中最突出和最丰富的细胞群之一,近年来引起了人们的广泛关注。CAF与基质成分和免疫细胞的复杂相互作用在协调TME重组中起着至关重要的作用,包括血管生成、细胞外基质(ECM)重塑和免疫逃避等过程。
目前,包括免疫治疗和化疗在内的大多数治疗方法在很大程度上忽视了CAFs的关键作用。目前对CAFs和TME成分之间相互作用的理解不足以支持可靠治疗策略的发展。需要进一步的研究来加深对这些相互作用的理解,并为有效的治疗干预铺平道路。
近年来,单细胞转录组学的应用揭示了许多癌症类型中CAFs的异质性,如膀胱癌(BC)、头颈部鳞状细胞癌(HNSCC)、甲状腺乳头状癌(PTC)和肺癌(LC)。此外,最近两项基于单细胞RNA测序(scRNA-seq)的无偏倚研究从泛癌症角度探讨了CAF的异质性和可塑性,并揭示了CAF表型在不同癌症类型中的保守性。尽管scRNA-seq提供了一个前所未有的机会来系统地分析CAFs的异质性,但组织解离过程中空间信息的丢失阻碍了对CAFs和TME之间串扰的研究。最近发展的空间转录组学(ST)可以获得组织切片内的全转录组数据,从而保存细胞的空间位置信息。因此,将scRNA-seq数据与ST数据进行正交整合将有助于确定CAFs的空间分布特征,并进一步剖析CAFs与TME之间的细胞通讯。
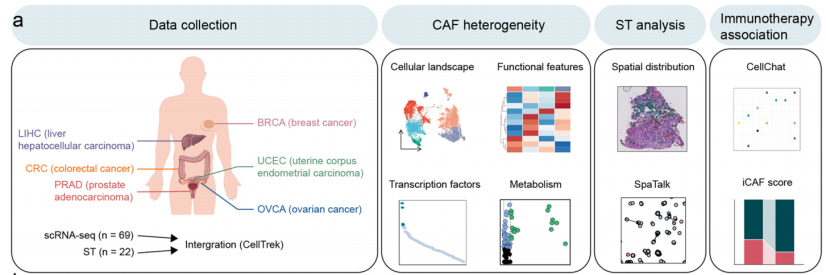
机理模式图(图源自Molecular Cancer)
该研究描绘了六种常见癌症类型中CAFs的格局,并描述了这些亚型的独特功能特征。还分析了另外三种常见肿瘤和两种新测序的罕见肿瘤的scRNA-seq数据,以扩大人们对CAF异质性的理解。通过整合scRNA-seq数据和ST数据生成的跨越6个肿瘤的空间单细胞转录组图谱,包括744,289个细胞,用于描述CAFs的空间分布特征,并表征CAFs与TME之间的复杂相互作用。值得注意的是,基于炎症性CAFs (iCAFs)生成的评分显示与黑色素瘤患者对免疫治疗的反应显著相关。综上所述,该研究为TME中针对CAFs的治疗策略的开发提供了新的见解和指导。
原文链接:
https://doi.org/10.1186/s12943-023-01876-x.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言