【Blood】FORTE研究中多发性骨髓瘤患者MRD由阴性转阳的预测因素
2023-12-31 聊聊血液 聊聊血液 发表于上海
学者对入组卡非佐米 FORTE 研究的 MRD 阴性患者进行分析,包括基线风险特征、给予的治疗和达到 MRD 的时间,以期探索这些因素对MRD转阳风险的影响。研究结果近日发表于《Blood》。
MM中MRD转阳的预测因素
根据报道,使用高效抗多发性骨髓瘤 (MM) 方案后50-80%的 MM 患者可达到骨髓微小残留病 (MRD) 阴性。因此,目前的挑战正在从实现 MRD 阴性转向随着时间的推移而维持 MRD 阴性,因为持续 MRD 阴性是长期结局的更强预测因素。事实上,MRD复阳通常预示着未来复发和结局恶化,但关于 MRD 复阳与复发之间的时间以及预测 MRD 复发的因素(包括基线风险特征和治疗)的可用数据很少。
学者对入组卡非佐米 FORTE 研究的 MRD 阴性患者进行分析,包括基线风险特征、给予的治疗和达到 MRD 的时间,以期探索这些因素对MRD转阳风险的影响。研究结果近日发表于《Blood》。

关键点
Amp(1q)、HRCA≥2个、CTC高水平和至首次 MRD 阴性的时间较长是无法维持MRD 阴性的重要预测因素。
与来那度胺单独给药相比,卡非佐米-来那度胺维持治疗可降低 MRD 转阳的风险。
研究结果
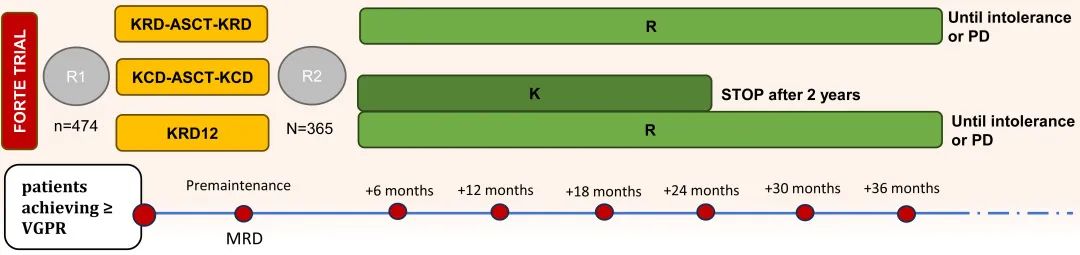
FORTE研究是一项在意大利42个中心开展的随机、开放标签、II期研究,纳入适合移植的18-65岁新诊断多发性骨髓瘤患者。共随机两次:入组时1:1:1随机分配至三个诱导-强化-巩固组之一(KRd+ASCT :KRd X4 +ASCT +KRdX4;KRd12;KCd +ASCT :KCdX4+ ASCT+ KRdX4),巩固治疗后合适患者1:1随机进入维持治疗(来那度胺维持治疗至进展,或KR维持两年)。
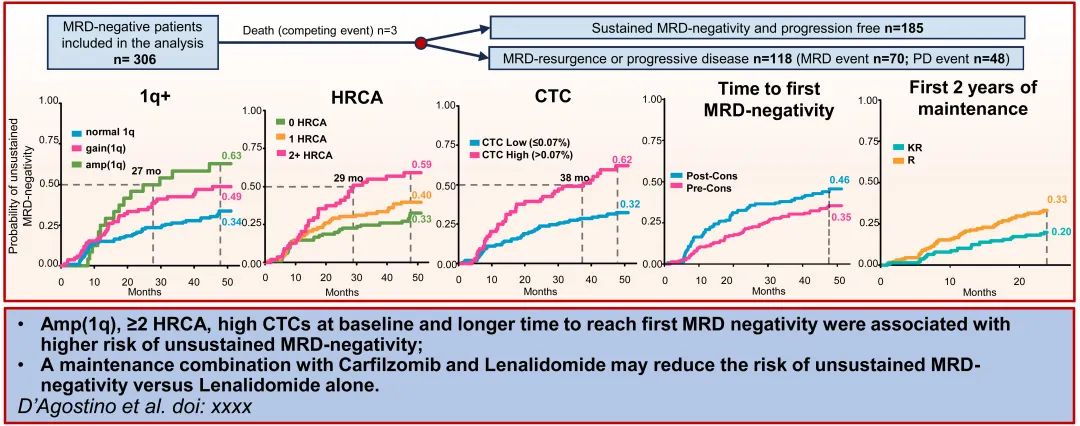
FORTE 研究中共有310/474例 (65%) 入组患者实现MRD 阴性。在 MRD 阴性患者中4例被排除,因为在 MRD 阴性后很快退出试验,并且没有进一步的 MRD/缓解评价,因此分析人群包括306例患者。至首次 MRD 阴性的中位时间为8.9个月。MRD 阴性后中位随访50.4个月后,185/306例 (60%) 患者仍为 MRD 阴性且无进展,118/306例 (39%) 患者MRD 转阳,3例 (1%) 患者死亡,无进展。
在失去 MRD 阴性状态的患者中,42/118例 (36%) 患者1年时持续 MRD 阴性。虽然维持1年MRD 阴性患者的 MRD 复阳可能发生较晚且发生率较低,但仍在这些患者中观察到 MRD 复阳和/或复发,表明两次MRD阴性评价之间间隔1年的时间不足以识别无 MRD 复阳和/或复发的患者。
MRD转阳的患者中,70/118例 (59%) 患者在 PD 前骨髓穿刺样本中的 MRD 检测呈阳性,48/118例 (41%) 患者在骨髓 MRD 阳性前PD。
在 MRD 转阳前PD的48例患者中,22/48例 (46%) 患者在过去6个月内未进行 MRD 评估,而其余26例进行了近期 MRD 评估且为阴性,其中16/26例 (62%) 发生骨骼/髓外复发,无生化PD。
在 PD 前 MRD 转阳的70例患者中,从 MRD 阳性至常规无进展生存期 (PFS) 事件(PD或死亡)的中位时间为22.3个月,而从 MRD 阳性至下次治疗的中位时间为34个月。这种延迟可用于设计重新诱导 MRD 阴性的策略。
国际分期系统 (I vs II/III) 和乳酸脱氢酶无法预测MRD转阳。ISS III 患者仅占全部 MRD 阴性人群的13%,尽管持续 MRD 阴性的4年 CI 为52%,但与 ISS I/II 患者相比无统计学显著差异 (p=0.80)。另一方面,高危细胞遗传学 [del(17p) 和/或t(4;14) 和/或t(14;16)] 患者MRD转阳的风险高于标危患者(HR=1.54,p=0.06;4年CI 54% vs. 36%)。
1q+异常方面,amp(1q) 和gain (1q)与MRD转阳的风险高于正常 1q (4年 CI 分别为63% vs. 49% vs. 34%)。具体而言,amp(1q) 显著增加MRD转阳的风险 (HR=2.07,p=0.02)(图1的panel A)。
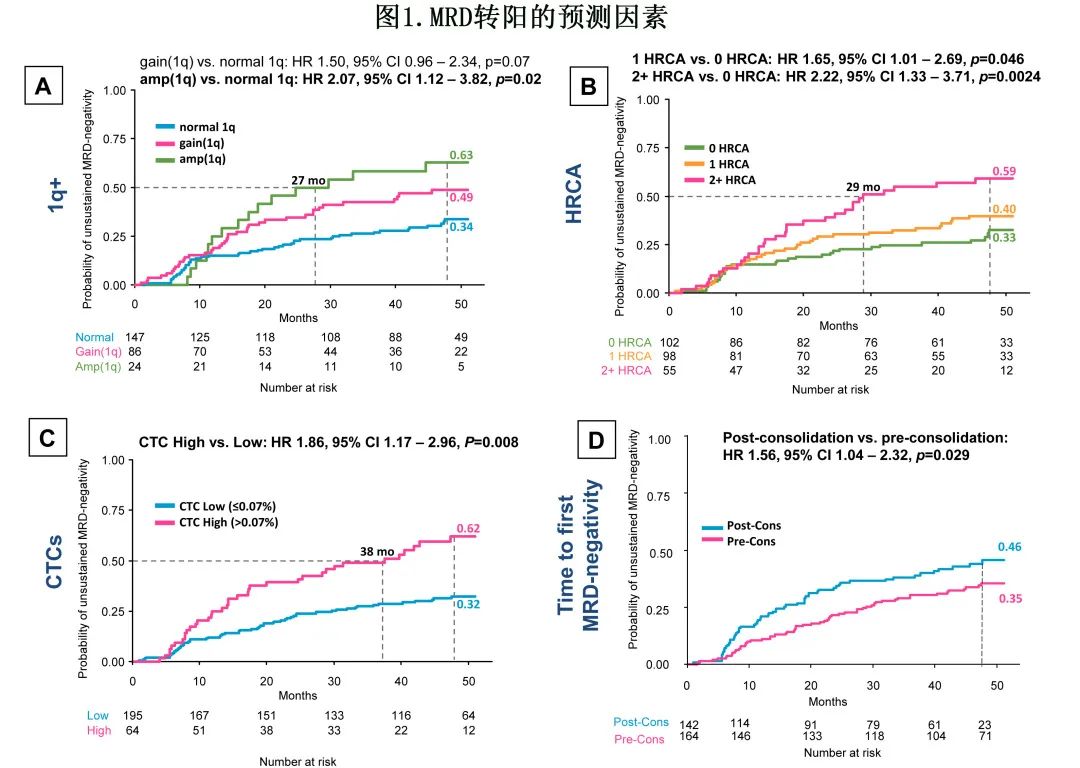
将 1q 纳入高危细胞遗传学异常 (HRCA) 的定义中,存在≥2个HRCA(HR=2.22,p=0.002 vs. 0 HRCA) 或1个HRCA(HR=1.65,p=0.046 vs. 0 HRCA) 也与 MRD 转阳风险显著升高相关(≥2 vs. 1vs. 0个HRCA的4年 CI 分别为59% vs. 40% vs. 33%)(图1的panel B)。
基线时高循环肿瘤细胞 (CTC)(>0.07%)相对于低CTC,预测MRD转阳的风险显著更高(4年CI 62% vs. 32%,HR=1.86,p=0.008)(图1的panel C)。即使使用较低的临界值 (≥0.01%) 定义亚组仍可证实 CTC 的作用。
首次 MRD 阴性的时间也对 MRD 复阳风险有影响。具体而言,巩固治疗开始后达到首次 MRD 阴性预示着MRD转阳的风险高于巩固治疗前首次MRD阴性(4年CI 46% vs. 35%;HR=1.56,p=0.03)(图1的panel D)。
维持治疗前的治疗,KRd + ASCT组患者的 MRD 阴性持续时间有长于 KRd12 组(4年CI 34% vs 43%;HR=0.73,p=0.17)或KCd + ASCT组(4年CI 44%;HR=0.72,p=0.16)的趋势。
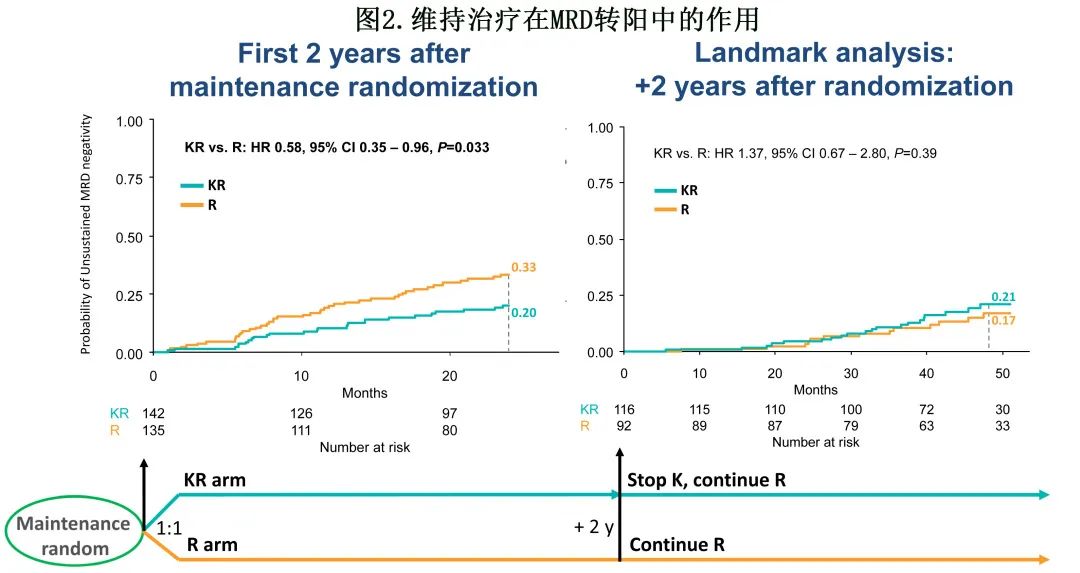
维持治疗方面,KR vs. R具有保护作用的趋势(4年CI 35% vs. 43%,HR=0.75,p=0.15)。但由于 KR 组患者仅在维持治疗的前两年接受卡非佐米,然后继续来那度胺单药治疗,因此进行了两项单独的分析,分开考虑从第二次随机化至卡非佐米停药的阶段(维持治疗的前2年)与卡非佐米停药后的阶段(维持治疗2年后的界标分析)。
在维持治疗的前2年,与单独接受 R 的患者相比,接受 KR 的患者MRD转阳的风险较低(24个月CI 20% vs 33%,HR=0.58,p=0.03),而在治疗2年后的界标分析中该风险变得可重叠(4年CI 17% vs 21%,HR 1.37,p=0.39)(图2)。
总结
对入组FORTE 研究的 MRD 阴性患者进行分析发现,Amp(1q)、HRCA≥2个、CTC高水平和至首次 MRD 阴性的时间较长是无法维持MRD 阴性的重要预测因素;与来那度胺单独给药相比,卡非佐米-来那度胺维持治疗可降低 MRD 转阳的风险。
该研究的结果应在更大的前瞻性患者队列中进行验证,包括含达雷妥尤单抗的联合治疗和新的免疫治疗。此外该数据是在适合移植的新诊断 MM 人群中产生的,应在不适合移植的环境中进行验证。
参考文献
D'Agostino M,et al. Predictors of Unsustained Minimal Residual Disease Negativity in Multiple Myeloma (MM) Patients.Blood . 2023 Dec 4:blood.2023022080. doi: 10.1182/blood.2023022080
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#多发性骨髓瘤# #MRD#
37