JHO:CAR-T治疗61例继发性CNS淋巴瘤的多中心回顾性研究
2023-12-13 聊聊血液 聊聊血液 发表于上海
近日发表一项多中心、回顾性队列研究,评估了61例接受CAR-T治疗的SCNSL患者的结局,也是目前最大样本量的研究。
CAR-T治疗继发性CNS淋巴瘤
复发性大B细胞淋巴瘤(LBCL)累及中枢神经系统(CNS)可能是系统性淋巴瘤继发CNS播散的结果,即继发性CNS淋巴瘤(SCNSL),其预后较差。CAR-T细胞疗法彻底改变了复发或难治性(R/R) LBCL患者的三线治疗和二线治疗,但大多数CAR-T关键研究排除了CNS受累的患者,仅有限的小型回顾性和前瞻性研究纳入CNS受累LBCL患者。
Journal of Hematology & Oncology近日发表一项多中心、回顾性队列研究,评估了61例接受CAR-T治疗的SCNSL患者的结局,也是目前最大样本量的研究。

研究结果
该研究纳入接受CAR-T治疗的成人SCNSL(排除R/R原发CNS淋巴瘤)患者61例,表1为CAR-T治疗前根据复发部位(CNS vs . CNS和全身)分层的患者的关键基线特征。
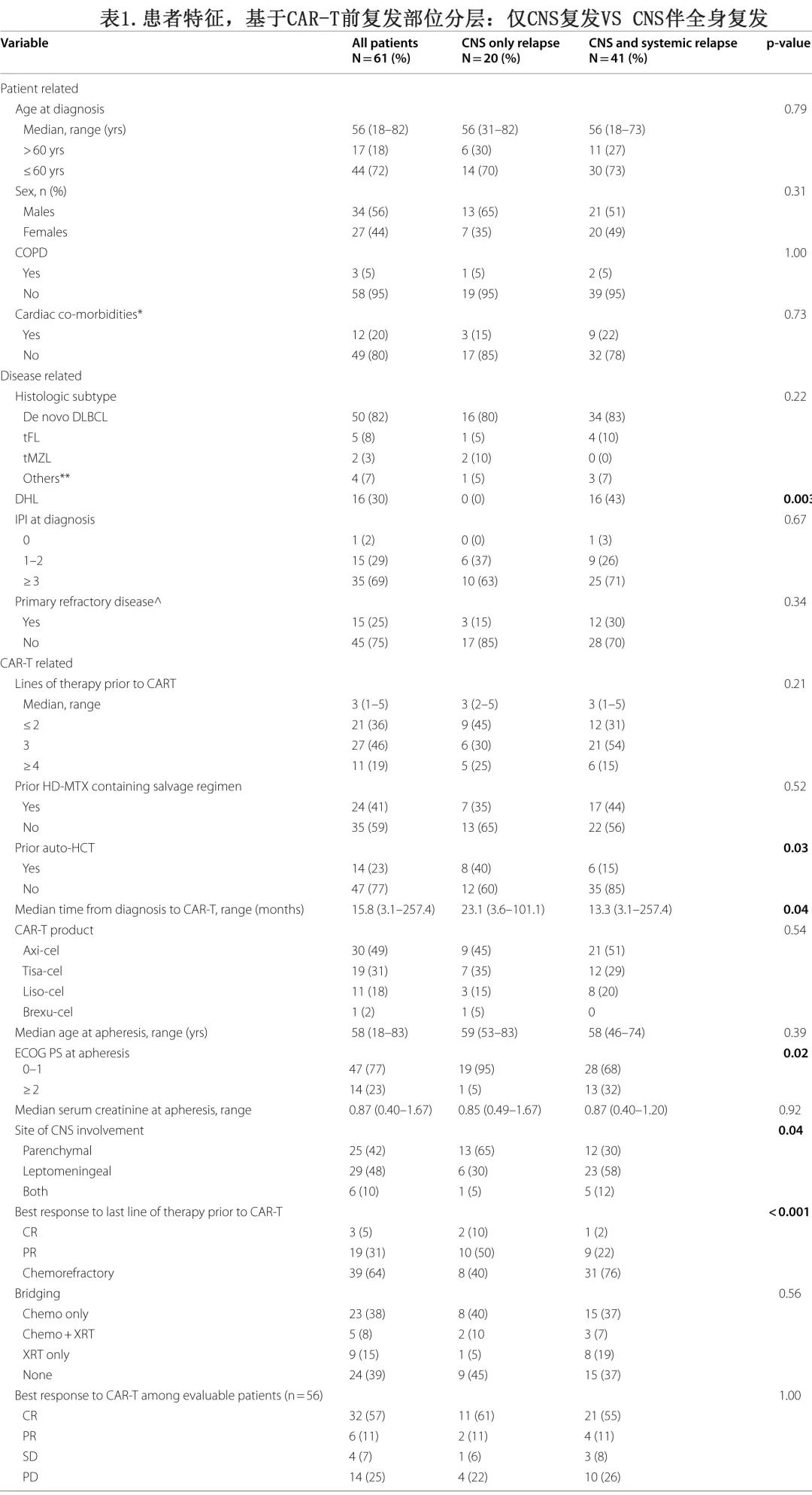
诊断时的中位年龄为56岁,56%为男性。最常见的组织学类型为原发DLBCL(48例,79%),其次为转化型淋巴瘤(7例,11%)。16例患者(30%)为伴有MYC/BCL2和/或BCL6重排的高级别B细胞淋巴瘤(双打击淋巴瘤[DHL])。35例(69%)患者诊断时IPI≥3分。67%(41例)的患者入组时存在全身受累,33%(20例)的患者同时存在全身和CNS受累。在一线(诱导)治疗期间,24例患者接受了大剂量甲氨蝶呤联合全身治疗(嵌入或全身治疗完成后)。
复发/进展时20例仅出现CNS复发,另41例在CAR-T治疗前出现CNS伴全身复发。CAR-T之前的中位治疗线数为3。最常用的CAR-T产品为axicabtagene ciloleucel (axi-cel, n=30, 49%),其次是tisagenlecleucel (tisa-cel, n=19, 31%)和lisocabtagene maraleucel (liso-cel, n=11, 18%)。与仅CNS复发的患者相比,CNS和全身性复发的患者更多为DHL (p=0.003)、既往未接受auto-HCT (p=0.03)、单采时ECOG体能状态≥2 (p=0.02)、软脑膜受累(p=0.04)、从诊断到CAR-T的中位时间较短(p=0.04)及在CAR-T之前为化疗难治性状态(P<0.001)。
研究的总缓解率(ORR)为68%,CR率为57%。在CAR-T治疗前仅有CNS复发(72%/61%)和CNS伴全身复发(66%/55%)的患者之间,ORR和CR率相当(p=1.00)。
任何级别CRS的发生率为70% (n=43),其中7例患者(16%)发生≥3级CRS。57% (n=34)的患者发生所有级别ICANS,其中15例(44%)患者发生≥3级ICANS。在CAR-T治疗前仅有CNS复发的患者与CNS伴全身复发的患者之间,CRS或ICANS的发生率无差异。
评估了达到完全缓解(CR)与未达到CR的患者相关因素。两组的大多数患者(CR组72% [n=23]和非CR组54% [n=13])在CAR-T治疗前均为化疗难治性。与未获得CR的患者相比,获得CR的患者更有可能发生任何级别的CRS(66% vs. 34%,p=0.037)。在多变量分析中,只有经历任何级别CRS的患者(与无CRS相比)获得CR的几率更高(OR=3.9, P=0.047),而接受≥4线治疗的患者(与<4线治疗相比)趋向于在获得CR方面有统计学意义(OR=10.2, p=0.05)。
中位PFS为3.3个月(图1A),6个月和12个月PFS率分别为35%和16%,且各亚组的PFS率与主要分析结果一致;此外不同CAR-T产品的中位PFS无差异。值得注意的是,单采时ECOG PS 0 ~ 1分的患者较≥2分患者有较长的中位PFS,但未达到统计学显著性(分别为3.5个月vs.1.3个月,p=0.06)。多变量分析中未发现与PFS显著较好相关的任何因素。
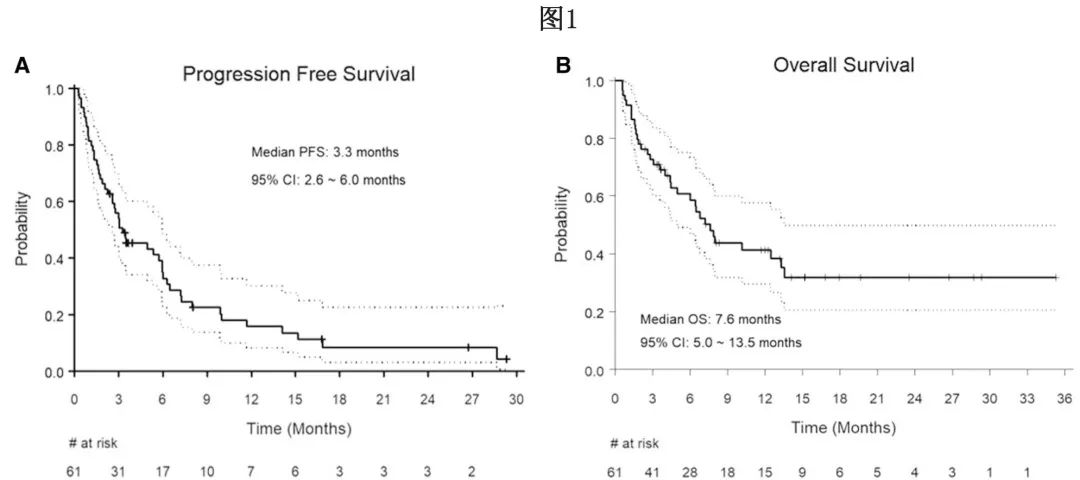
中位随访时间14.1个月,中位OS为7.6个月(图1B), 6个月和12个月OS率分别为59%和41%。各亚组的总生存率与主要分析结果一致,不同CAR-T产品类型的中位OS无差异。值得注意的是,无心脏合并症(7.2个月vs. 4.7个月,p=0.049)和单采时ECOG PS为0 ~ 1分(12.5个月vs. 2.8个月)的患者的中位OS显著长于有心脏合并症且ECOG PS≥2分的患者。虽然仅CNS复发患者(未达到 vs. 6.4个月)的中位OS超过CNS伴全身复发患者,但未达到统计学显著性(p=0.07)。在多变量分析中,仅单采时ECOG评分0-1与较好的OS显著相关(HR=2.56,, p=0.01)。
评估CAR-T治疗后发生CRS (vs.无CRS)风险的变量,只有CAR-T产物在两组间有显著差异(p=0.02):在接受axi-cel治疗(n=30)的患者中,87% (n=26)发生CRS,而接受tisa-cel治疗的患者(n=19)中47% (n=9)发生CRS。评估CAR-T后发生NT (神经毒性,vs.无NT)风险的变量,两组间仅CNS受累部位差异有统计学意义:发生NT的患者较未发生NT的患者有显著较高的软脑膜受累(61% [n=17] vs. 39% [n=11])和软脑膜和实质受累(100% [n=6] vs. 0% [n=0]) (p=0.03)。虽然CAR-T类型产品的NT风险不具备统计学意义(p=0.09),但NT方面观察到类似与CRS的趋势:在axi-cel (n=30)患者中70% (n=21)发生所有级别的NT,而tisa-cel (n=19)和liso-cel (n=10)患者中分别有42% (n=8)和40% (n=4)发生NT。
总结
该多中心回顾性队列研究是迄今为止规模最大的评估接受CAR-T治疗的SCNSL患者的结局,可为探索SCNSL未来细胞治疗方案的研究提供基准,其获得几项重要结果。首先,CAR-T的ORR高(68%),其中大部分缓解为CR(57%)。其次,发生任何级别CRS的患者中CAR-T后达到CR的概率显著较高,但与较好的PFS无关。第三,≥3级CRS的发生率为16%,与无CNS受累的患者一致,但≥3级神经毒性的发生率较高(44%)。第四,与CRS和神经毒性风险增加相关的因素分别包括CAR-T产品类型和CNS受累部位。最后,尽管缓解率高,但缓解并不持久,且PFS和OS较差,表明治疗这一患者人群仍存在挑战,目前急需研究改善SCNSL患者CAR-T治疗效果的策略。
参考文献
Epperla N,et al.Outcomes of patients with secondary central nervous system lymphoma following CAR T‑cell therapy: a multicenter cohort study.J Hematol Oncol . 2023 Nov 9;16(1):111. doi: 10.1186/s13045-023-01508-3.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#CAR-T治疗# #复发性大B细胞淋巴瘤# #继发性CNS淋巴瘤(SCNSL)#
47