Blood:ZUMA-1研究5年随访结果,axi-cel或有治愈潜力
2023-03-02 聊聊血液 聊聊血液 发表于上海
CD19 CAR-T产品Axicabtagene-ciloleucel (axi-cel)在美国最早获批的适应症是既往治疗≥2线的复发/难治性大B细胞淋巴瘤(R/R LBCL),后获批用于一线免疫化疗
ZUMA-1 5年随访
CD19 CAR-T产品Axicabtagene-ciloleucel (axi-cel)在美国最早获批的适应症是既往治疗≥2线的复发/难治性大B细胞淋巴瘤(R/R LBCL),后获批用于一线免疫化疗后12个月内的R/R LBCL。其关键研究为ZUMA-1研究的2期部分,先前报道的ORR为83%,其中CR为58%;安全性也可控,多数SAE发生于输注后早期。随访27.1个月后仍有39%的患者持续缓解,中位OS未达到。其上市后的真实世界分析结果也大致与ZUMA-1研究一致。详细见:Nat Med:Axicabtagene ciloleucel作为高危大B细胞淋巴瘤的一线治疗、NEJM:Axicabtagene Ciloleucel作为大B细胞淋巴瘤二线治疗的效果如何?
近日《Blood》报道了ZUMA-1研究2期中,axi-cel治疗难治性LBCL随访63.1个月的疗效和安全性,结果中位OS为25.8个月,5年OS率为42.6%,5年疾病特异性生存率为51.0%。5年随访结果证实axi-cel可带来持续生存,支持其在部分侵袭性B细胞淋巴瘤患者中的治愈潜力。

ZUMA-1为多中心、单臂、注册1/2期研究,纳入年龄≥18岁、组织学确诊为LBCL(WHO 2008分类;包括DLBCL、PMBCL或转化的FL)。患者患有难治性疾病,定义为对既往末次治疗的最佳反应为疾病进展或稳定,或在自体干细胞移植后12个月内复发。
患者白细胞单采并在第-5天至第-3天接受清淋化疗(氟达拉滨 30 mg/m2/d 和环磷酰胺500 mg/m2/d)。第0天单次静脉输注axi-cel,目标剂量为2 × 106 CAR-T细胞/kg体重。不允许使用桥接治疗。
主要疗效终点为研究者评估的ORR,次要终点包括DOR、PFS、OS、关注的AE的发生率和血液CAR-T细胞水平。本次长期分析中额外的疗效终点包括:EFS、至进展时间、至下次治疗时间和疾病特异性生存。
患者
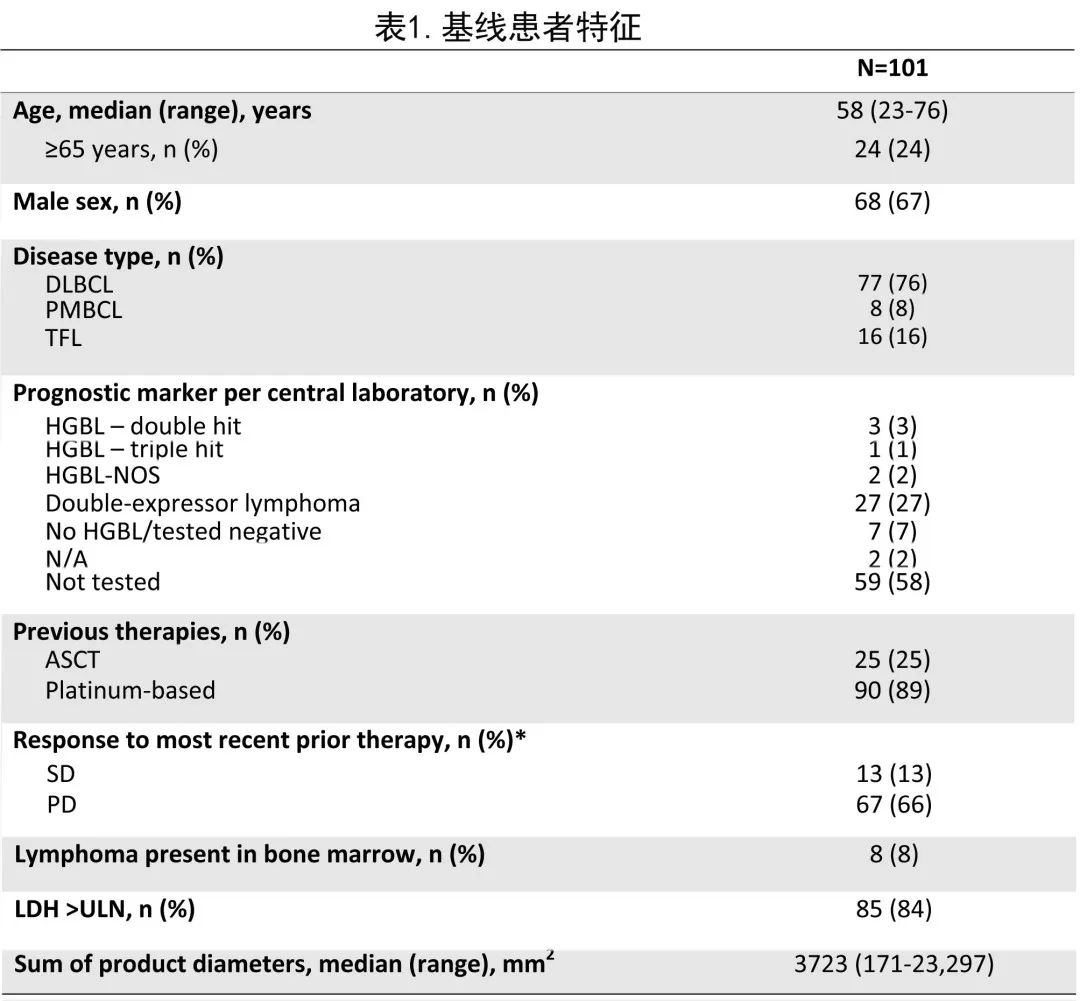
入组了111例 LBCL 患者并进行了白细胞单采,其中101例患者接受了 axi-cel 治疗。治疗患者的中位年龄为58岁(表1)。大多数患者 (84%) 的 LDH 水平高于正常值上限 (LDH > ULN),根据直径总和计算的中位肿瘤负荷为3723 mm。在42例治疗前肿瘤样本可评估的患者中,33例 (79%) 具有不良预后标志物,包括6例高级别 B 细胞淋巴瘤和27例双表达淋巴瘤。
疗效
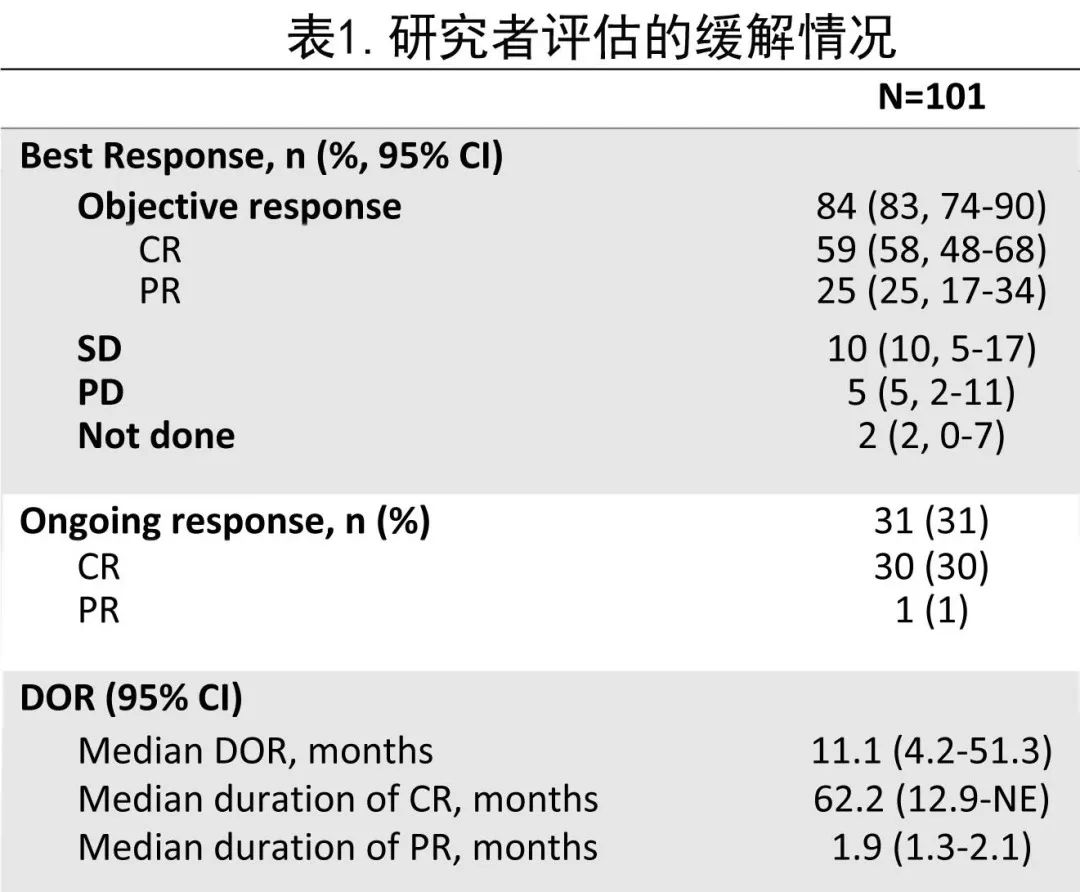
接受 axi-cel 治疗的患者从输注开始计算的中位随访时间为63.1个月。在101例接受 axi-cel 的患者中,研究者评估的 ORR 为83%(n=84;表2),58% (n=59) 达到CR。在所有接受治疗的患者中,中位 DOR 为11.1个月 。数据截止时31例患者 (31%) 的客观缓解仍在持续,30例患者 (30%) 的 CR 仍在持续。相应的,CR患者的中位持续时间为62.2个月,而PR的中位持续时间为1.9个月。在达到 CR 的患者 (n=59) 中,37例 (62.7%) 是在第4周评估时达到CR,22例 (37.3%) 是在第4周评估后达到CR。第4周时达到 CR 患者的中位 DOR 为34.7个月,而第4周后达到 CR 的患者未达到中位DOR。
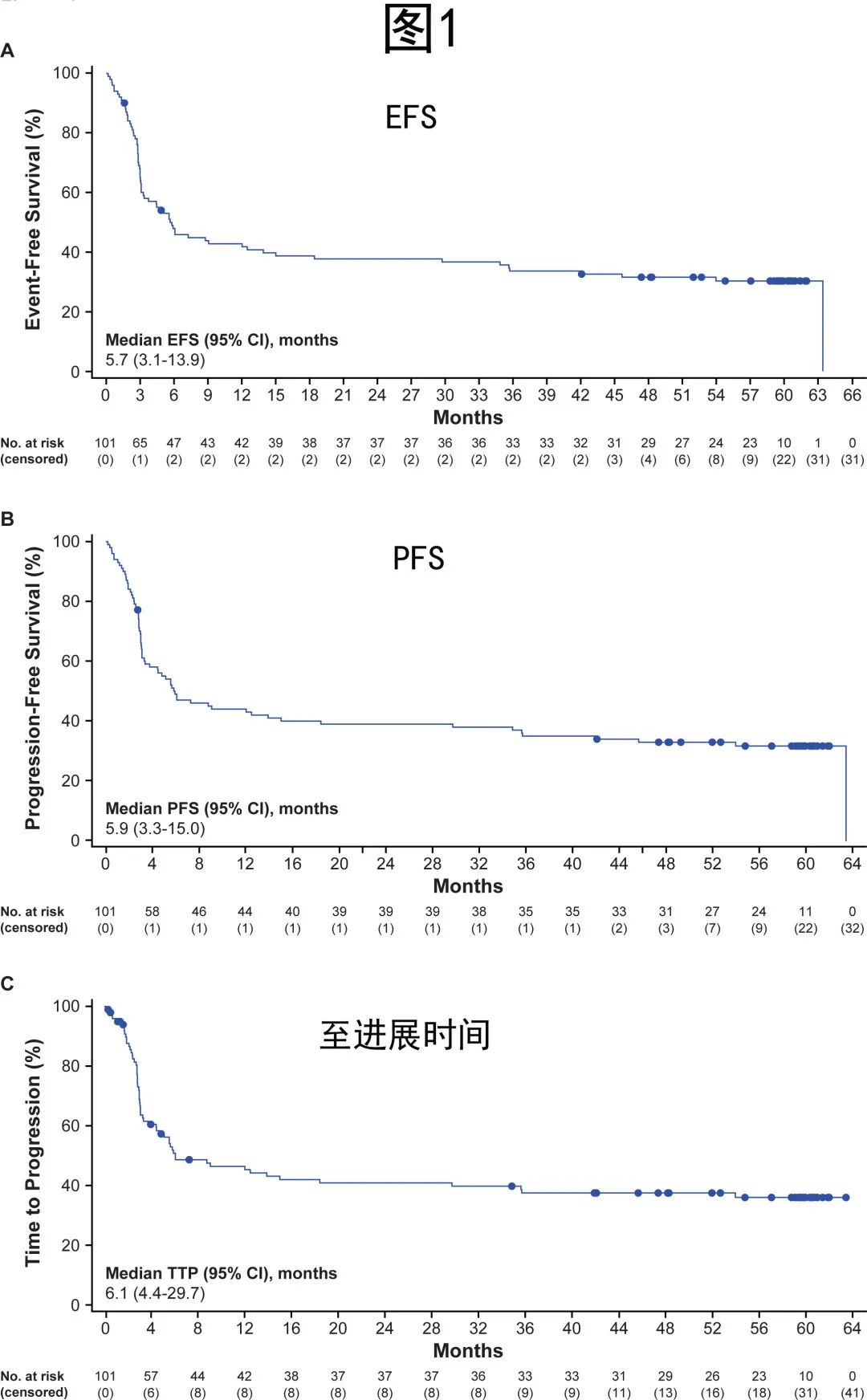
中位 EFS 为5.7个月(图1),估计5年 EFS 率为30.3%。中位 PFS 为5.9个月,5年 PFS 估计值为31.8%。中位至疾病进展时间为6.1个月(图1),中位至下次治疗时间为8.7个月。
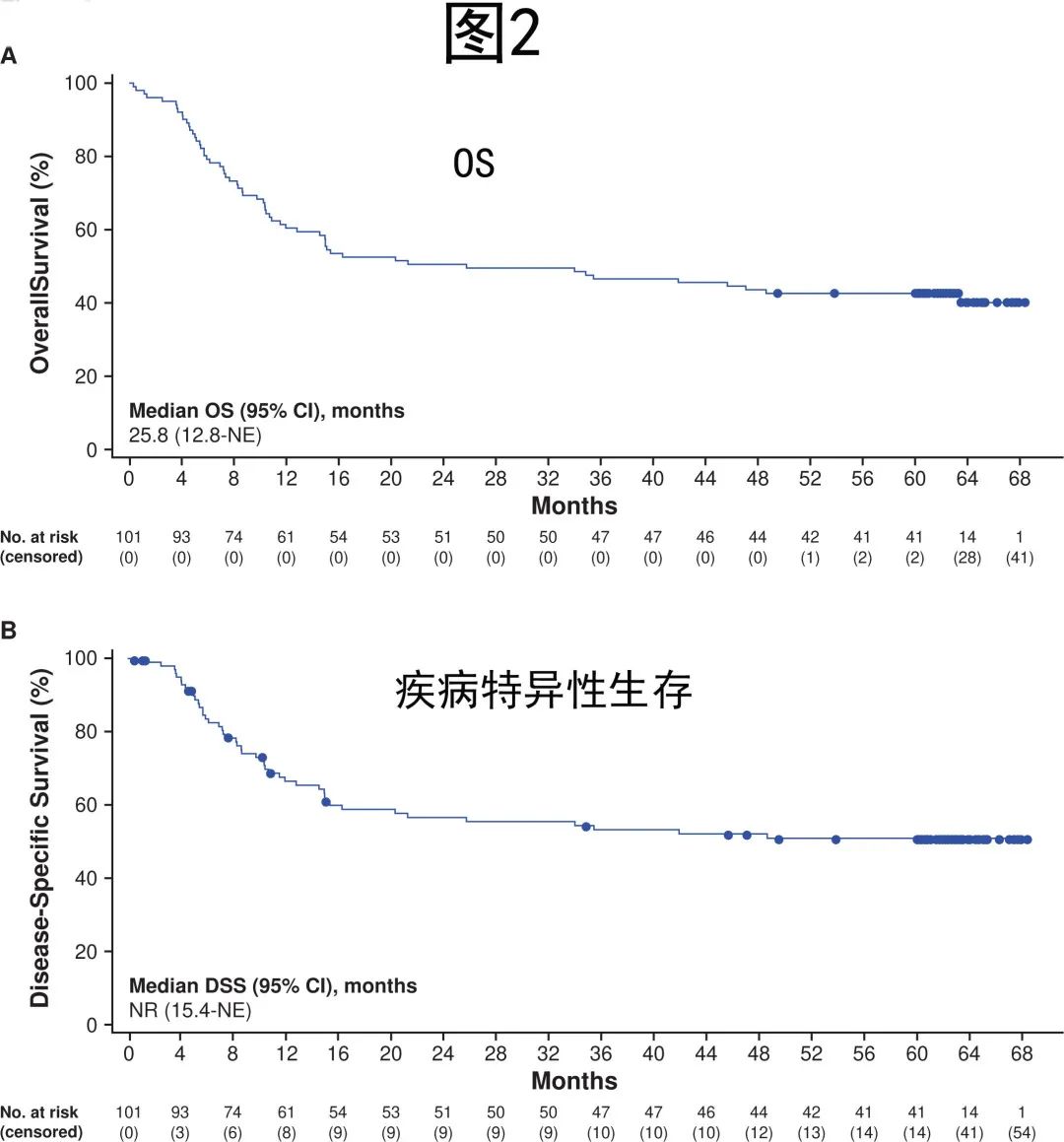
中位 OS 为25.8个月,5年 OS 率为42.6%(图2)。达到 CR 的患者未达到中位OS,5年 OS 率为64.4%。在12个月时发生 (n=57) 和未发生 (n=44) EFS事件的患者中,5年 OS 率分别为5.3%和90.9%;在24个月时发生 (n=62) 和未发生 (n=39) EFS事件的患者中,5年 OS 率分别为11.3%和92.3%。数据截止时42%的治疗患者 (42/101) 仍然存活,其中63%的患者达到CR。中位疾病特异性生存期尚未达到,5年疾病特异性生存率为51.0%。
安全性
随访5年的安全性特征与既往报告基本一致。CRS 94 例 (93%),其中≥3级11例 (11%);1 65例患者 (64%) 发生神经系统事件,其中30例患者 (30%) 发生≥3级事件。在接受 axi-cel 治疗的患者 (n = 101) 中未报告新的安全性信号,并且在2年分析后未报告与 axi-cel 相关的新的SAE。
在所有接受治疗的患者中,59例 (58%) 死亡(表3),主要是由于疾病进展 (n=45),且大多数死亡发生在输注后第一年内 (n=40)。如前所述,4例研究期间患者死于AE(2例与 axi-cel 相关,2例无因果关系),但2年分析数据截止后未报告 AE 导致的死亡。自2年分析以来,仅报告了1例与既往治疗和/或清淋化疗相关的MDS导致的死亡,该患者的LBCL结果为CR。

生物标志物分析
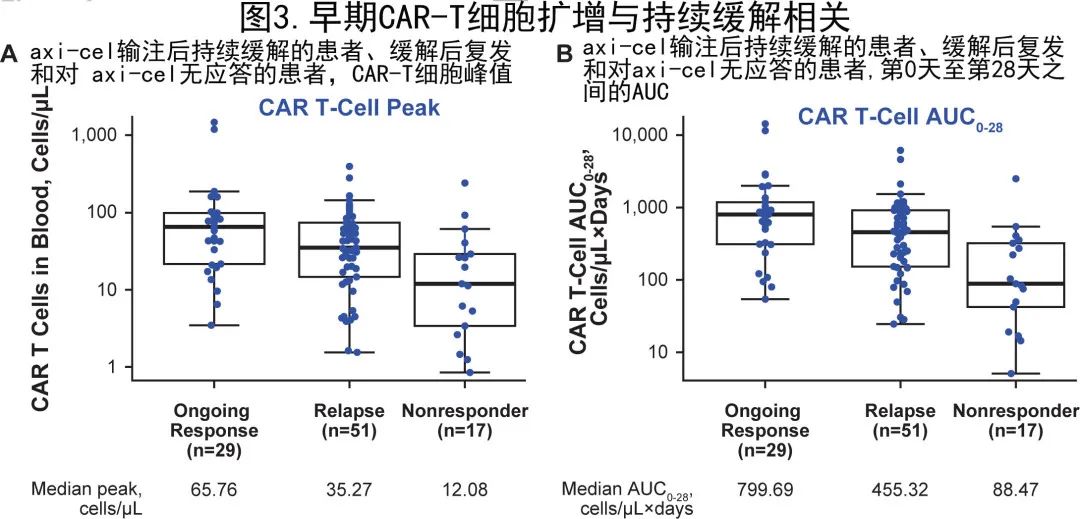
在具有可评估样本的治疗患者 (n=97) 中,输注后60个月时缓解仍持续的患者中位CAR-T细胞峰值水平(65.76个细胞/μL)似乎高于复发(35.27个细胞/μL)或未缓解的患者(12.08个细胞/μL;图3)。此外输注后第0天至第28天的CAR-T细胞曲线下面积(图3)以及根据肿瘤负荷标准化的 CAR T 细胞峰值水平也观察到相似趋势。
对 ZUMA-1 II期研究中关键队列的5年更新分析表明,难治性LBCL患者可达到缓解持续及长期生存,且没有新的安全性信号。5年时所有治疗患者的估计 OS 为43%,而达到CR的患者为64%,尤其重要的是5年疾病特异性生存率为51%,这一结果支持axi-cel在相当大比例患者中具有治愈潜力。
参考文献
Sattva S Neelapu ,et al. 5-Year Follow-Up Supports Curative Potential of Axicabtagene Ciloleucel in Refractory Large B-Cell Lymphoma (ZUMA-1).Blood . 2023 Feb 23;blood.2022018893. doi: 10.1182/blood.2022018893.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言