肿瘤生物学:(12)异质性相互作用和血管生成
2022-09-07 小药说药 网络
肿瘤的特性并不仅仅由单个肿瘤细胞及其携带的基因所决定。癌症实际上是一种组织疾病,我们将这种复杂的组织称为肿瘤。
1前言
到20世纪末,越来越多的证据显示,肿瘤的特性并不仅仅由单个肿瘤细胞及其携带的基因所决定。癌症实际上是一种组织疾病,我们将这种复杂的组织称为肿瘤。
对上皮来源的肿瘤进行组织病理分析显示,其是由很多不同肿瘤的细胞组成的。在一些常见的上皮癌如乳腺癌、结肠癌、胃癌及胰腺癌中,那些组成肿瘤间质的正常细胞客户占到整个肿瘤组织的90%以上。
研究表明,这些正常细胞,特别是上皮癌中的间质细胞使非常活跃的,它们为肿瘤细胞所招募和利用,从而成为其必需的合作者。招募正常细胞的生物学意义非常重要,这有助于肿瘤的生长。这也意味着癌症绝不仅仅是肿瘤细胞内部相互作用的结果。恰恰相反,大多数肿瘤组织中恶变细胞与正常细胞不停地进行交流。
2肿瘤由相互依存的不同类型细胞组成
上皮来源肿瘤组织具有复杂的间质成分,除了恶变的上皮细胞外,多种间质细胞也参与构成肿瘤组织。这些间质细胞包括成纤维细胞、肌纤维细胞、内皮细胞、周皮细胞、平滑肌细胞、脂肪细胞、巨噬细胞、淋巴细胞及肥大细胞。
如同正常组织一样,许多异质性相互作用在该组织形成的肿瘤中也发挥重要作用。肿瘤细胞通过招募邻近的正常组织和远处骨髓中的间质细胞来控制其数量并促进其增殖。另外,间质细胞也可能影响肿瘤上皮细胞的增殖和存活。
在正常组织中,异质性信号通路主要依赖于下列因子间的交换:1)生长因子,如肝细胞生长因子(HGF)、转化生长因子-α(TNF-α)、血小板衍生生长因子(PDGF);2)生长抑制信号,如转化生长因子-β(TGF-β);3)营养因子,如胰岛素样生长因子-1和-2(IGF-1和IGF-2)。
在肿瘤形成以后异质性相互作用依然存在。例如,肿瘤上皮细胞时常释放PDGF,而间质细胞含有相应的受体,同时间质细胞可释放IGF-1,促进周围肿瘤细胞的生长和存活。上皮细胞和间质细胞通过互相调节彼此的数量和位置,确保各亚型细胞在肿瘤和正常组织中保持最佳比例,并处于最佳位置。
3肿瘤:“未愈合的损伤组织”
肿瘤内异质性相互作用的信号传递非常复杂,设计许多信号分子在不同细胞间的交换。有研究者在观察肿瘤组织和愈伤组织结构时,注意到许多信号转导在肿瘤发展和伤口愈合时有惊人的相似性。
伤口愈合过程已被研究得非常深入,当皮肤形成创伤时,血小板凝集并释放一些分子,包括PDGF和TGF-β。伤口会释放血管活性因子,该分子可增加伤口附近血管的渗透性,帮助伤口从血浆中得到纤维蛋白原,后者转化为纤维蛋白,称为血块的支架,成簇的纤维蛋白缠绕在血小板团块周围起止血作用。
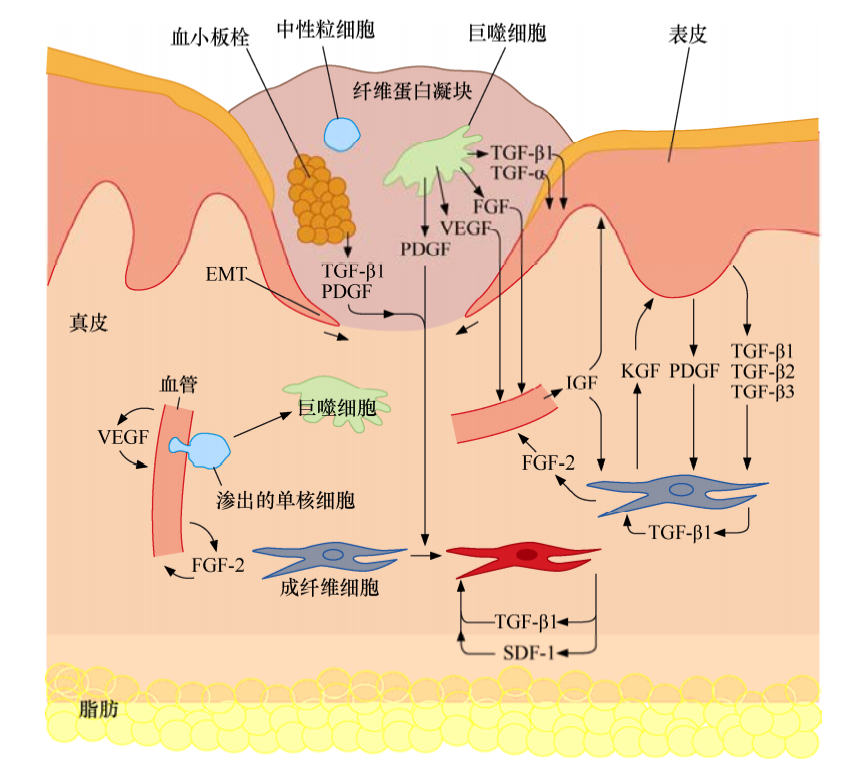
血小板释放的PDGF能吸引成纤维细胞并刺激其增殖。随后血小板衍生的TGF-β激活这些肌成纤维细胞并诱导其分泌基质金属蛋白酶(MMP)。MMP一旦释放,便开始降解胞外基质(ECM)中的特定成分,从而导致两种主要结果:一方面是ECM结构重塑,为新的细胞留出空间;另一方面导致许多黏附与ECM上且处于未激活状态的生长因子的释放,这些因子随后被激活。
血小板释放的和ECM来源的生长因子随后吸引单核细胞和其他类型的吞噬细胞和免疫细胞,渗入伤口位置。这些细胞清理伤口并清除外来物质、细菌及组织碎片,同时释放并激活有丝分裂因子,如成纤维细胞生长因子(FGF)、血管内皮生长因子(VEGF)。这些因子刺激内皮细胞增殖并构建新的毛细血管,即血管生成过程。
当这些事件在愈伤间质部位发生时,此处的上皮细胞也在进行自我更新,其目标是重建位于伤口处的上皮层。为此上皮细胞减少其与ECM、特别是基底膜的黏附。上皮细胞的E-钙黏蛋白表达降低,并常常被替换为N-钙黏蛋白。当表达不同的细胞表面钙黏蛋白后,处于愈伤组织周边的上皮细胞发生形态学改变,使其呈现出成纤维细胞的外观,这种改变称为上皮-间质转化(EMT),使得上皮细胞具有运动能力和侵袭性。
将这一过程同肿瘤细胞与相邻间质细胞的相互作用进行比较,就可发现伤口愈合与肿瘤发生极为相似。这些伤口愈合和肿瘤组织中上皮-间质相互作用所共有的机制在临床应用方面具有重要意义。
4间质细胞活化促进肿瘤发生
一些生物学试验为募集的间质细胞对上皮细胞肿瘤的发生有重要影响提供了更加直接的证据。在一项研究中,通过导入PDGF表达载体使原来非致瘤性的、永生化的角化细胞强制分泌高水平的PDGF。当这些细胞被植入宿主鼠体内时,它们形成了增殖旺盛的肿瘤,这无疑是因为它们可以释放PDGF以招募并激活间质细胞,而间质细胞又与分泌PDGF的角化细胞相互作用,并促进其增殖,最终引发后者的恶性转化。
间质成纤维细胞支持肿瘤生长的重要作用可被另一类试验证明:转化的、弱致瘤性人乳腺上皮细胞(MEC)植入免疫缺陷的宿主小鼠体内需要2个月以上才能形成肿瘤。然而,如果注射前将这些细胞与来自正常乳腺组织的人乳腺间质成纤维细胞混合,只需1/3的时间即可形成肿瘤。这些混合的成纤维细胞明显缩短了MEC从宿主小鼠招募成纤维细胞所需要的时间,缺乏这些成纤维细胞,肿瘤不能生长。
5巨噬细胞和髓系细胞的作用
越来越多的证据显示,肿瘤中大量募集的巨噬细胞在促进肿瘤发展中起着重要作用。骨髓中髓系单核细胞进入大循环,它们被癌细胞募集进入肿瘤:单核细胞一旦安置下来,即被诱导分化为巨噬细胞。这种募集依赖于趋化因子传递的趋化信号。
巨噬细胞一旦定居于肿瘤间质中,即在刺激血管生长中起重要作用。在一些癌症中,如乳腺癌中,产生MCP-1的水平、巨噬细胞存在的数量与各种肿瘤诱导血管生成的水平直接相关。在其他肿瘤中,浸润的肿瘤相关巨噬细胞的密度与微血管密度相关。
肿瘤中的乏氧区吸引着巨噬细胞,它们似乎能很好地耐受乏氧。这些炎性细胞一旦定居于肿瘤的乏氧区,就开始分泌大量的VEGF,并通过内皮细胞、毛细血管和含氧丰富的血液给这一区域供氧,从而减轻缺氧的状况。
此外,与肌成纤维细胞类似,巨噬细胞能够大量分泌基质金属蛋白酶(MMP)。MMP-9主要参与肿瘤进展,由肿瘤相关巨噬细胞(TAM)产生。MMP-9一旦被活化,就会继续裂解细胞外空间中大量重要的蛋白底物。在特定的侵袭性癌中,包括乳腺癌、膀胱癌和卵巢癌,TAM已被证明是该酶的主要来源。
髓系细胞中还有第二种促进肿瘤侵袭的细胞。这些未成熟骨髓细胞(iMC)在小鼠的结直肠癌模型中研究的最为清楚。iMC聚集于肿瘤侵袭的前沿,分泌基质金属蛋白酶MMP-2和MMP-9,协助肿瘤细胞向下面的组织层侵袭。
6肿瘤的血管生成
与正常组织相似,肿瘤需要接近循环系统才能生长和生存。早在20世纪50年代中期,病理学家就注意到肿瘤优先生长在血管周围。人们发现距离血管0.2mm之外的肿瘤细胞不再生长,而再远处的肿瘤则会死亡。
乏氧不是细胞远离循环系统所付出的唯一代价。除获取氧气之外,细胞还需要与血管系统进行有效的相互作用以获取营养,并排泄代谢废物和二氧化碳。因此,肿瘤需要在不同的发展阶段,调整脉管系统的布局。
VEGF的产生是由可利用的氧气控制的。因此,许多类型的细胞通过VHL蛋白与其同伴的作用,估量其自身细胞内储备的氧压。在乏氧条件下,这个蛋白复合物允许功能性HIP-1α和HIF-1β与转录因子聚集,转录因子反过来驱动大量基因表达,这些基因的表达产物可以促进血管生成。
HIF-1诱导产生的最关键的产物之一是血管生成因子VEGF,该分子的产生依赖于肿瘤的类型及其进展的阶段,与肿瘤细胞、巨噬细胞、肌成纤维细胞有关。事实上,有两种结构相关、功能相似的蛋白,称为VEGF-A和VEGF-B。
与许多其他生长因子类似,VEGF是酪氨酸激酶受体VEGFR的配体。相似地,另一个重要的血管生成因子,碱性成纤维细胞生长因子(bFGF),与内皮细胞表达额同源受体结合。内皮细胞一旦受到这些血管生成因子的刺激,就发生增殖并使其胞质变形以构建毛细血管圆柱状的细胞壁。这些毛细血管可以穿透现存的组织层,想局部血管生成因子的高浓度部位移动。
血管生成实际上远比上述描述复杂得多。这个复杂的形态发生过程除了起主要作用的VEGF外,还涉及许多其他因子,包括多种形式的TGF-β、碱性成纤维生长因子(尤其是FGF2)、白介素8、血管生成素、血管生成因子和PDGF。而且,除内皮细胞外,一些不同类型的细胞也有助于毛细血管和大血管形成。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#相互作用#
43
#互作#
55
#生物学#
62