PD-L1高表达III-IV期胸腺鳞癌获益新辅助免疫联合化疗,实现病理完全缓解
2024-05-04 苏州绘真医学 苏州绘真医学 发表于上海
本研究的目的是评估PD-1抑制剂联合化疗转化治疗对胸腺鳞状细胞癌患者的有效性和安全性。
胸腺癌是一种罕见的纵隔恶性肿瘤,目前缺乏标准治疗方案。手术是传统治疗的重要组成部分,放疗和化疗的潜在价值仍存在争议。然而,有相当数量的患者确诊时已处于晚期,这给通过手术干预实现完全切除带来了挑战,通常导致预后不良。鉴于免疫疗法在各种流行癌症中的抗肿瘤作用,某些研究已应用免疫治疗并显示出对晚期或复发性胸腺癌病例的良好疗效。然而,与其它类型肿瘤相比,胸腺癌免疫治疗引起的不良反应发生率明显更高,其中严重和致命的并发症尤为突出。因此,迫切需要解决胸腺癌患者接受免疫治疗的关键问题。本文报告了两名根据Masaoka-Koga分期系统诊断为III-IV期胸腺鳞状细胞癌的患者,接受PD-1抑制剂联合化疗转化治疗的情况。本研究的目的是评估PD-1抑制剂联合化疗转化治疗对胸腺鳞状细胞癌患者的有效性和安全性。该队列中有两名患者,一名患有III期疾病,另一名患有IV期疾病,被认为不适合进行前期手术切除。穿刺病理证实胸腺鳞状细胞癌的诊断。两名患者均接受了PD-1抑制剂联合化疗的转化治疗。两名患者均观察到肿瘤缩小,从而成功完成手术。术后病理显示无肿瘤细胞残余,表明病理完全缓解。值得注意的是,没有患者在免疫治疗后出现 3 级或更高级别的免疫治疗相关不良反应。PD-1抑制剂联合化疗以及手术治疗改善了Masaoka-Koga III-IV期胸腺鳞状细胞癌患者的疗效和安全性,代表了这一疾病的一种潜在新型治疗替代方案。
背 景
胸腺瘤是一种罕见的、起源于胸腺上皮的肿瘤,在恶性肿瘤中的患病率为 0.2-1.5%。根据胸腺肿瘤中上皮细胞与淋巴细胞的相对比例,世界卫生组织(WHO)将胸腺瘤分为低级别胸腺瘤(A型和AB型)、高级别胸腺瘤(B1、B2和B3型)和胸腺癌(C型)。过去,恶性胸腺瘤和胸腺癌的治疗方式相似,主要以手术切除作为主要治疗方式。然而,相当多的患者肿瘤浸润至心包、无名静脉(innominate vein,也称头臂静脉)、上腔静脉等重要结构,直接通过手术进行完全切除具有挑战性。此外,胸腺癌术后放疗和化疗的疗效并不令人满意。尽管日本的一项II期临床研究表明仑伐替尼对不可切除的胸腺癌患者有效,但客观缓解率仅为 38%。因此,晚期患者的预后是较差的。鉴于胸腺癌的发病率低且缺乏标准治疗方案,寻找更有效的方法来提高患者预后至关重要。近年来,免疫检查点抑制剂(ICIs)在治疗包括胸腺肿瘤在内的各类癌症中表现出显著的抗肿瘤作用。
程序性细胞死亡配体1(PD-L1)在多种实体瘤中高表达,可作为ICI的有效生物标志物。据观察,恶性胸腺瘤和胸腺癌细胞表现出PD-L1高表达,表明免疫疗法可能是胸腺肿瘤的一种有前景的治疗选择。然而,应该指出的是,胸腺瘤通常与自身免疫性疾病相关,并且给予程序性细胞死亡蛋白1(PD-1)抑制剂可能会因自身免疫系统激活而导致严重的免疫相关不良事件(irAE)。B型胸腺瘤,无论其风险状况如何,病理成分中都含有淋巴细胞。这部分淋巴细胞可能会过度激活,从而诱发自身免疫损伤,甚至危及生命。相反,胸腺鳞状细胞癌表现出鳞状上皮病理学特征并且缺少淋巴细胞。因此,与胸腺瘤相比,irAE的发生率要低得多。先前的研究表明,恶性胸腺瘤和胸腺鳞状细胞癌在免疫治疗的疗效和不良事件方面存在显著差异,特别是严重的irAE。因此,胸腺瘤和胸腺癌的区别治疗,特别是在治疗方案(如ICI治疗)的选择上,是有必要的。
病例1
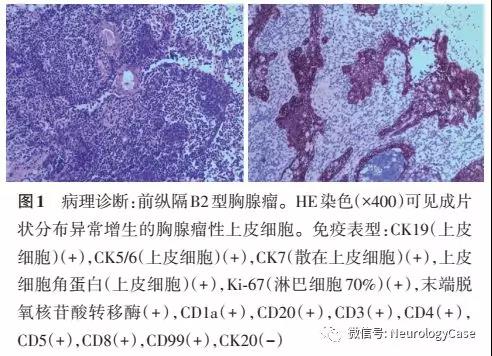
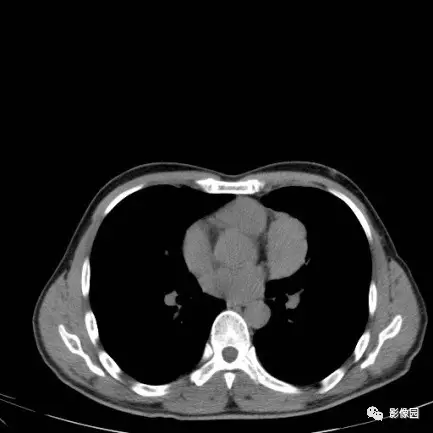
患者男,39 岁,收治于重庆医科大学第三附属医院,病史一年,患者主诉左侧间歇性胸痛,近 2 个月内加重。患者未表现出眼部或四肢无力、吞咽困难或呼吸困难,并否认任何胸腺肿瘤家族史(表1)。胸部CT扫描显示,左前上纵隔肿瘤大小为 72×67 mm,密度不均匀,强化明显。肿瘤紧邻升主动脉和肺动脉,并且左头静脉和臂静脉存在充盈缺损。还检测到肝转移。根据Masaoka-Koga分期系统,患者属于IV期,排除了直接手术干预。CT引导下穿刺活检病理证实低分化鳞癌的诊断,PD-L1肿瘤比例评分(TPS)为 75%。使用PD-1检查点抑制剂(信迪利单抗 200 mg)、白蛋白结合紫杉醇(240 mg/m2)和卡铂(AUC=5)联合治疗 4 个周期后,CT检查证明肿瘤大小消退至 44×36 mm。此外,与之前的影像结果相比,肿瘤与升主动脉、肺动脉、左头静脉和臂静脉界限清晰(表2)。根据实体瘤疗效评估标准(RECIST v1.1),治疗结果被归类为部分缓解(PR)。PET-CT评估了肿瘤的活动状态:除了肝脏病变外,没有明显的转移灶。经过MDT会诊,患者接受了肿瘤消退治疗,计划进行完整的切除手术。在获得患者知情同意后,研究人员进行了中央胸骨切开术。在整个手术过程中,观察到肿瘤与肺动脉和主动脉非常接近,但易于分离。此外,研究人员发现肿瘤已浸润心包,包括纵隔肿瘤切除和部分心包切除。术后组织病理学显示纵隔组织内纤维组织增生,伴有胆固醇晶体的存在和显著炎症细胞浸润。局部观察到大量泡沫细胞存在,明显不存在恶性细胞。总之,患者获得了全面的病理缓解(pCR,图1)。患者在手术后接受了两个周期的信迪利单抗作为辅助治疗。术后第 3、6 和 12 个月进行了随访评估,胸部增强CT扫描没有肿瘤复发或转移的证据(图2)。该患者在用药后出现了许多不良反应,包括脱发、恶心和关节疼痛,这些似乎与化疗药物有关。此外,在初始药物治疗周期后患者出现短暂性、由免疫介导的肝炎,主要表现为胆红素水平升高(间接胆红素:12.0 µmol/L,参考值1.7–10.2 µmol/L)。根据与ICI相关的irAE管理指南,这种不良反应被分类为I级。患者在接受保肝治疗后完全康复,在后续治疗中未出现复发。还观察到短暂的免疫相关性心肌损伤,表现为心肌肌钙蛋白I水平轻度升高(心肌肌钙蛋白I 0.187 ng/mL,参考值 0-0.03 ng/mL),心电图检查结果不显著。治疗后,患者的心肌肌钙蛋白I水平恢复正常,并且后续没有升高,消除了使用PD-1抑制剂的任何影响。此外,短暂性甲状腺功能亢进表现为血清T4水平轻微升高(总甲状腺素T4 156.78 nmol/L,参考值 73.74–137.15 nmol/L),无需治疗干预即可自行缓解(表3)。
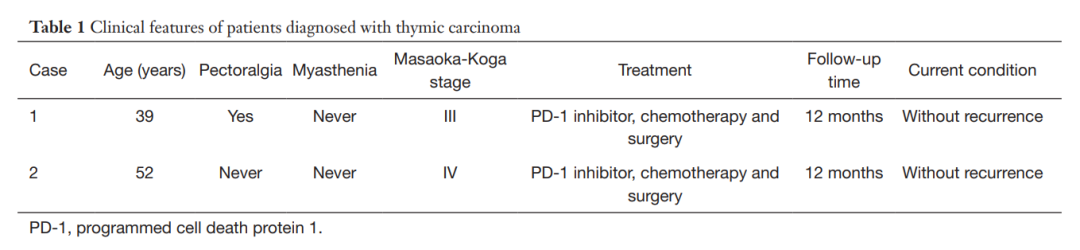
▲表1 胸腺癌患者临床特征

▲表2 胸腺癌影像学特征
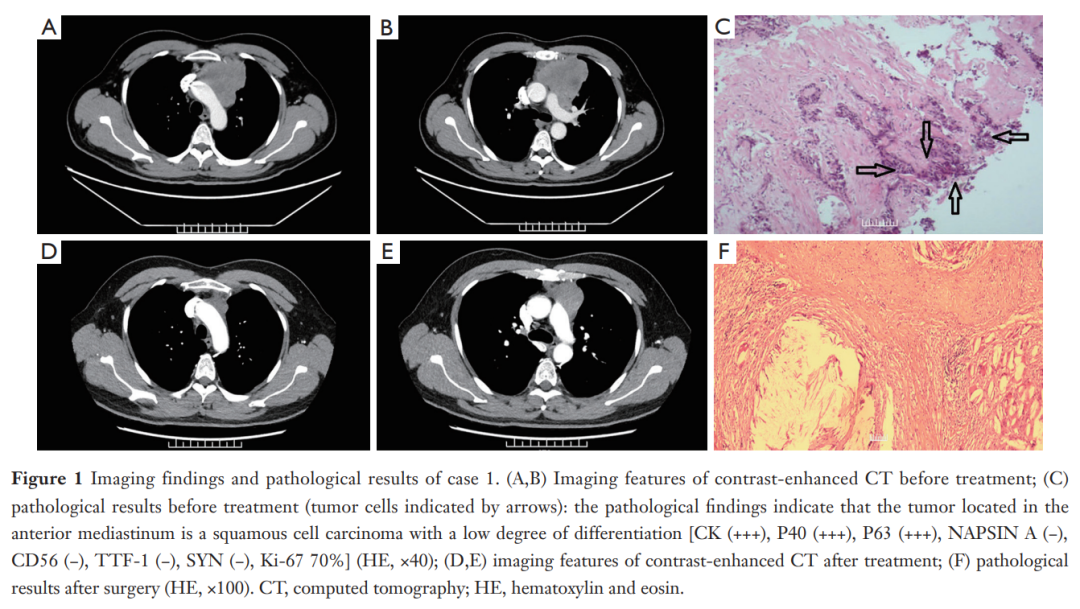
▲图1 病例1的影像学结果和病理检查结果

▲图2 病例1治疗时间线
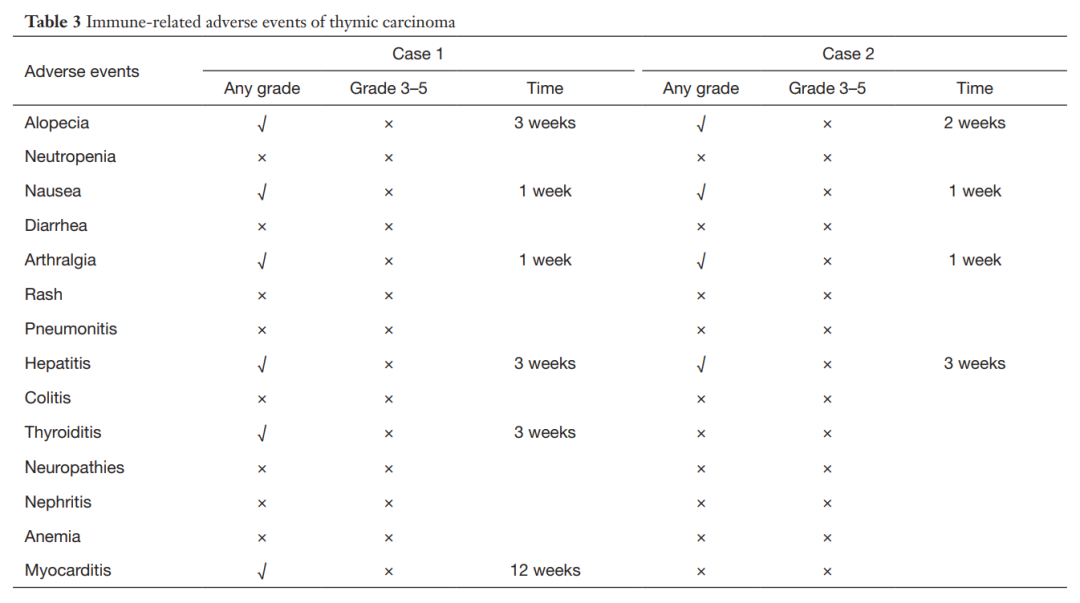
▲表3 胸腺癌免疫相关不良事件
病例2
患者女,52 岁,收治于重庆医科大学附属第三医院,入院 6 天前经CT检查发现罹患纵隔肿瘤。患者没有表现出任何眼部或全身肌肉无力,也没有胸腺肿瘤家族史(表1)。胸部CT显示左前纵隔有一肿瘤,大小 57×58 mm,轻微强化,浸润心包、左锁骨下动脉、左无名静脉、胸主动脉。根据Masaoka-Koga分期系统,分类为III期,无法直接手术切除纵隔肿瘤。穿刺活检病理学鉴定肿瘤为低级别鳞状细胞癌,PD-L1 TPS为 85%。在白蛋白结合紫杉醇(240 mg/m2)联合卡铂(AUC=5)和信迪利单抗(200 mg)治疗 4 个周期后,CT扫描显示肿瘤缩小至 11×28 mm,并且与外周动脉和心包分离(表2)。根据RECIST v1.1指南,治疗结果被归类为部分缓解(PR)。经过多学科讨论后,制定的治疗计划实现肿瘤缩小,可完全切除。因发现肿瘤侵犯左无名静脉及心包,患者同意手术,随后行胸骨正中切开术进行纵隔肿瘤切除、部分心包切除术,并部分切除左无名静脉。术后病理分析显示纵隔肿瘤组织有慢性炎症细胞浸润坏死,病理完全缓解(pCR,图3)。患者在手术后接受了两个周期的信迪利单抗作为辅助治疗(图4)。术后第 3 个月、6 个月和 12 个月进行了随访,胸部增强CT扫描未发现肿瘤复发或转移。患者出现了化疗相关的不良反应,包括脱发、恶心和关节疼痛。此外,患者在第 1 个周期后出现短暂性免疫相关性肝炎,主要表现为丙氨酸转氨酶水平轻度升高(参考值 7.0-40.0 U/L)。然而,通过适当的保肝治疗,肝功能恢复正常,随后的治疗,包括使用PD-1抑制剂,并未受到影响(表3)。
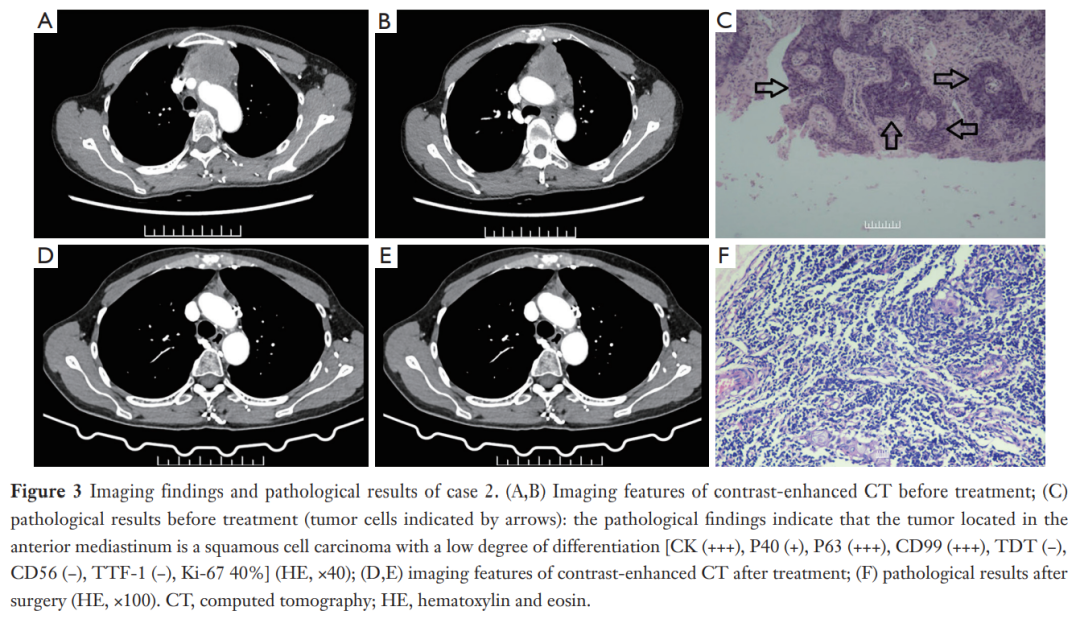
▲图3 病例2影像学结果和病理检查结果
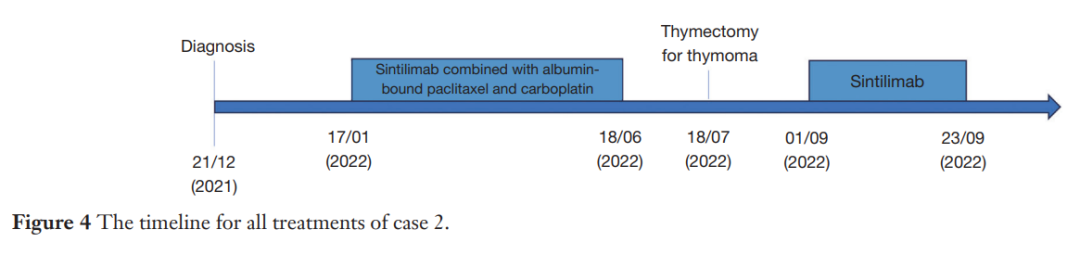
▲图4 病例2治疗时间线
多学科团队讨论
胸腺瘤和胸腺癌
胸腺癌和高级别胸腺瘤都是起源于胸腺上皮的肿瘤,但它们表现出不同的临床、病理和组织学特征。胸腺癌是一种罕见的起源于胸腺的恶性肿瘤,其发病率明显低于胸腺瘤。一项研究报道,胸腺癌约占所有胸腺瘤的 10%-15%。胸腺癌的临床表现与恶性胸腺瘤非常相似,症状包括胸痛、背痛、胸闷以及上腔静脉阻塞等肿瘤压迫体征。然而,与胸腺瘤相比,胸腺癌与重症肌无力的相关性较低。影像学检查结果表明,胸腺癌更容易侵入较大的血管和心包,导致心包积液和淋巴结肿大。在本文研究队列中,两名患者都没有明显的肿瘤或重症肌无力家族史。一名患者报告出现胸痛,而另一名患者在例行体检时偶然发现胸腺癌。影像学分析显示肿瘤显著增强,并具有侵袭性行为。确诊时,肿瘤已侵犯心包、主动脉、肺动脉干等。病例1也有明显的肝转移。这些临床特征与既往报告一致。重要的是,胸腺癌和胸腺瘤表现出独特的病理特征。胸腺鳞状细胞癌是胸腺癌最常见的组织学亚型。胸腺鳞癌的细胞与实体鳞癌相似,没有淋巴细胞浸润或典型的胸腺组织特征。胸腺癌和胸腺瘤的不同病理亚型导致免疫治疗的疗效和相关不良反应发生率存在差异。
免疫治疗疗效
ICI因其显著的抗肿瘤作用而在各种实体瘤的治疗中得到了广泛的应用。在众多潜在的生物标志物中,PD-L1表达水平已成为可靠且有效的指标。源自免疫器官的胸腺肿瘤通常表现出较高水平的PD-L1表达。这一观察结果为胸腺肿瘤患者实施免疫治疗策略提供了令人信服的理由。Giaccone等人的一项开创性II期临床试验研究了PD-1抑制剂帕博利珠单抗对复发性胸腺癌的疗效。结果显示,中位随访时间 20 个月时,客观缓解率(ORR)为 22.5%。值得注意的是,1 名患者(3%)获得完全缓解,8 名患者(20%)获得部分缓解。此外,21 名患者(53%)病情稳定,只有 27% 患者出现疾病进展。平均缓解时间为 22.4 个月。总研究人群的中位无进展生存期(PFS)为 4.2 个月,中位总生存期(OS)为 24.9 个月。引人注目的是,PD-L1高表达患者PFS长达 25 个月,与PD-L1低表达或阴性患者(2.9 个月)形成鲜明对比。随后在韩国进行了一项研究,旨在调查帕博利珠单抗(一种ICI)对既往接受过治疗的晚期胸腺肿瘤患者的治疗效果。研究结果显示,只有 27% 的患者出现疾病进展,这与之前在美国进行的一项研究的结果相印证。这些研究结果证实了PD-1抑制剂治疗胸腺癌的强大治疗潜力。在本文研究队列中,两名患者接受了PD-1抑制剂联合化疗。根据RECIST评估标准,两名患者均表现出部分缓解,并经手术病理证实病理完全缓解,这在以往的放疗方法中是罕见的。鉴于早期研究的令人信服的结果,加上本文研究中观察到的显著治疗反应,可以推断,免疫疗法和化疗的结合对于有效治疗胸腺鳞状细胞癌具有重要价值。
安全性
必须考虑针对胸腺肿瘤的抗肿瘤治疗疗效以及PD-1抑制剂相关严重不良反应的可能性。不良事件发生率的升高可能归因于胸腺作为免疫器官的免疫性质。既往研究提供了证据,表明与其它癌症相比,胸腺肿瘤患者irAE的发生率有所增加,特别是(但不限于)重症肌无力、致死性心肌炎和其它严重反应。潜在的机制主要涉及胸腺肿瘤上皮影响CD4+和CD8+淋巴细胞分化的能力,以及胸腺瘤中功能性胸腺髓质的缺失。因此,自身反应性T细胞逃避循环系统内的捕获,从而引发自身免疫现象。未成熟T淋巴细胞的存在在胸腺恶性肿瘤自身免疫的发展中发挥着至关重要的作用。与缺少未成熟免疫细胞的胸腺瘤患者相比,胸腺鳞状细胞癌患者在使用PD-1抑制剂治疗后发生自身免疫性疾病的风险较低。例如,美国的一项试验报告称,三名胸腺瘤患者出现严重肌炎或心肌炎,10% 的病例出现严重肝炎,一例患者罕见出现重症肌无力,而此类事件在使用PD-1抑制剂治疗的胸腺鳞癌患者中并不常见。同样,韩国的一项研究表明,15.4% 的胸腺癌患者出现严重肝功能损伤,而胸腺瘤患者的发生率明显更高,为 71.6%。一项单独的研究表明,与胸腺鳞状细胞癌或其它类型的恶性肿瘤相比,胸腺瘤病例在免疫治疗后重症肌无力和严重心肌炎恶化的发生率分别为 5% 和 57%。该证据表明,与胸腺瘤患者相比,胸腺癌患者严重irAE的发生率和严重程度显著降低。在本文队列中,两名胸腺鳞癌患者接受了PD-1抑制剂联合化疗的转化治疗,不良反应发生率为 100%。这些不良反应大多数为I级,例如恶心、脱发和皮疹。值得注意的是,两名患者均出现短暂性肝损伤,病例1出现轻度心肌损伤和甲状腺损伤。然而,通过适当的对症治疗,这些情况完全缓解,并且在后续后续治疗中没有复发。重要的是,两名患者均未出现3级不良反应,也没有不良反应需要停药。这些发现强烈表明,使用PD-1抑制剂治疗胸腺鳞状细胞癌具有较高的安全性。
医师讨论
多学科团队讨论并评估了本文的两个案例。初步评估显示,两名患者都不符合确诊后立即进行手术干预的条件。因此在讨论后采用了包含西妥昔单抗以及白蛋白结合紫杉醇和卡铂的治疗方案。在该治疗方案之后,在两名患者中均观察到了肿瘤降期,满足手术候选资格的要求。迄今为止,关于此类患者通过手术切除可行性仍存在争议。
肿瘤内科医师表示,既往用于胸腺肿瘤的主要治疗方法是手术、放疗和化疗。根据目前的研究结果,胸腺肿瘤患者可能会从免疫疗法和化疗的结合中取得生存获益。但需要注意的是,胸腺肿瘤可能与自身免疫性疾病相关,且与其它肿瘤相比,免疫治疗后出现irAE的概率和严重程度更高。因此,免疫治疗后应监测irAE的发生情况。
胸外科医师表示,与常见肺癌的胸外科手术类似,无法手术的患者可以接受新辅助免疫治疗联合化疗来降低肿瘤分期,以满足手术切除的标准。本文两个病例在术前免疫治疗和化疗后观察到肿瘤明显消退,没有发生严重的免疫相关不良反应,因此建议手术干预。术后,决定进行辅助免疫治疗或维持化疗,是否需要放疗将取决于病理评估。
专家观点
1.B型胸腺瘤适合免疫治疗吗?
专家意见1:Fabrizio Minervini博士表示,目前没有数据支持在B型胸腺瘤患者的新辅助或辅助治疗中使用免疫治疗。
专家意见2:Georgina Planas博士表示,胸腺上皮肿瘤的特征是胸腺上皮细胞异常,参与免疫耐受的基因(AIRE、FEZF2 和 MHC II类)表达异常,同时伴有胸腺结构改变。在这种情况下,阴性选择(negative selection,此过程是T细胞获得中枢免疫耐受的重要机制)受到损伤,导致自身反应性T细胞释放。这一事实使患者容易产生自身免疫以及PD-L1高表达,因为这些自身反应性T细胞通过释放干扰素γ(IFN-γ)和上调PD-L1表达来改变胸腺上皮细胞的抗原表达。另一方面,免疫疗法已被证明对PD-L1高表达和高肿瘤突变负荷(TMB-H)的肿瘤有效,这两者都是已确认的预测ICI疗效的生物标志物。含有丰富淋巴细胞成分的胸腺肿瘤(B1型和B2型)更容易与自身免疫性疾病相关,无论是在确诊前还是确诊后。不同的试验证实,irAE在接受免疫疗法治疗的复发性B型胸腺瘤中更为常见。例如,Cho等人报道,在 7 名胸腺瘤患者中有 5 名(71%)报告了 3 级或更高的irAE,在 26 名胸腺癌患者中有 4 名(15%)报告了 3 级或更高的irAE。因此,由于免疫相关不良事件发生率较高,B1/B2型胸腺瘤不应进行免疫治疗,在多学科肿瘤委员会未充分披露风险的情况下,不应跨适应症进行免疫治疗。
专家意见3:Katsuhiro Okuda博士表示,B型胸腺瘤不适合使用免疫疗法。因为胸腺瘤可能并发自身免疫性疾病,如重症肌无力、红细胞再生障碍、丙种球蛋白血症等。此外,B型胸腺瘤肿瘤的一部分被淋巴细胞浸润,限制了免疫治疗的效果。
专家意见4:Naoki Ozeki博士表示,胸腺瘤通常与自身免疫性疾病相关,使用PD-1抑制剂可能会刺激免疫系统,导致危及生命的irAE。然而,最近的一项研究认识到免疫疗法是治疗B3胸腺瘤和胸腺癌的相对安全且具有一定疗效的方法。
2.为什么胸腺鳞癌适合免疫治疗?
专家意见1:Fabrizio Minervini博士表示,胸腺上皮肿瘤高水平表达PD-1和PD-L1(范围 18%-100%),Masaoka 分期和组织学亚型之间存在显著差异。通常,PD-1和PD-L1在胸腺癌高表达,而非胸腺瘤。美国国家综合癌症网络指南(2022 v2版)建议将帕博利珠单抗作为胸腺癌患者的二线治疗。
专家意见2:Georgina Planas博士表示,尽管胸腺瘤的PD-L1表达率很高,但它们的TMB是所有成人癌症中最低的。胸腺癌具有较高的TMB,并且是缺少淋巴细胞的肿瘤,因此它们对免疫治疗具有良好的反应,且irAE比例较低。
专家意见3:Katsuhiro Okuda博士表示,胸腺鳞状细胞癌与肺鳞状细胞癌具有相似的特征,除了完全手术切除外没有有效的治疗方法,因此认为它是免疫联合化疗的良好候选者。这可能是一个很好的指征,特别是对于PD-L1蛋白高表达的病例。
专家意见4:Naoki Ozeki博士表示,胸腺鳞状细胞癌PD-L1高表达,这与PD-1和PD-L1抗体的阳性反应有关。显然,ICIs对于治疗胸腺鳞状细胞癌有效。然而,尽管与其它肿瘤相比,胸腺鳞状细胞癌的肿瘤突变负荷较低,但它仍然存在一定的自身免疫毒性风险。
3.胸腺癌患者免疫治疗应重点关注哪些不良反应?
专家意见1:Fabrizio Minervini博士表示,根据目前的文献,接受ICI治疗的患者中有 15%-60% 会发生免疫相关不良事件。不良事件可能会影响任何器官。最常见的不良反应是重症肌无力、肌炎、心肌炎、红斑、腹泻、甲状腺炎、肺炎和关节疼痛。
专家意见2:Georgina Planas博士表示,正如Ballman等人指出的那样,ICIs在大多数晚期胸腺癌患者中似乎具有良好的安全性。与帕博利珠单抗相关的常见irAE包括疲劳、厌食、胸壁疼痛、咳嗽、腹泻和转氨酶升高,但大约 15% 的患者经历了严重的irAE,包括肌炎、心肌炎、重症肌无力和肝炎。因此,人们对肌肉相关或神经肌肉的自身免疫毒性发展倾向似乎了解甚少。在这种情况下,需要进行密切的随访和监测。
专家意见3:Katsuhiro Okuda博士表示,由于胸腺癌免疫治疗的不良反应,应该警惕irAE,就像治疗其它器官肿瘤(包括肺癌)一样。由于肿瘤的位置和大小,预计在治疗前会有肌肉紧绷或血液循环问题,因此需要注意及早发现心肌炎,如果不及时治疗可能致命。
专家意见4:Naoki Ozeki博士表示,胸腺癌患者的免疫治疗应优先处理最严重的不良反应,例如心肌炎、肌炎、重症肌无力、肾炎和自身免疫性疾病等其它严重后果。
结 论
由于胸腺鳞状细胞癌的患病率相对较低,现有的治疗方式仍然有限。与胸腺瘤相比,ICIs 在胸腺鳞状细胞癌的治疗中表现出卓越的疗效和更高的安全性。重要的是,胸腺鳞状细胞癌中与ICI相关的严重和致命不良事件的发生率明显低于胸腺瘤。因此,免疫疗法与化疗相结合,然后进行手术干预,为III-IV期胸腺鳞癌患者提供了一种新颖且有前景的治疗途径。
参考文献:
Li D, Minervini F, Planas G, Okuda K, Ozeki N, Zou Y. Stage III-IV thymic squamous cell carcinoma in complete pathological remission achieved with thymic cancer rep after immunotherapy combined with chemotherapeutic conversion therapy: a report of two cases from real-world data. Gland Surg. 2024 Jan 29;13(1):117-127. doi: 10.21037/gs-23-488. Epub 2024 Jan 19. PMID: 38323230; PMCID: PMC10839697.

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#胸腺瘤# #PD-1抑制剂# #胸腺鳞癌#
11