Cell Rep:尹玉新/吕丹团队发现肿瘤免疫抵抗因子PTIR1并揭示相关肿瘤免疫耐受新机制
2023-11-08 BioMed科技 BioMed科技 发表于威斯康星
首次鉴定到天然免疫应答蛋白RIG-I的新亚型PTIR1分子,研究显示,多种肿瘤组织可以特异性诱导产生PTIR1,其通过影响MHC-I-肿瘤抗原肽复合体在肿瘤细胞表面的表达。
肿瘤免疫治疗作为近年来癌症研究的热点备受人们的关注,然而仅有不到五分之一的肿瘤患者对目前的免疫治疗有反应。此外,即便病人经治疗后得到初步缓解,随后部分肿瘤又会复发,表现出对免疫治疗的耐药,这些都是肿瘤免疫治疗面临的挑战。因此需要进一步研究肿瘤抵抗免疫系统的机制、探索新的药物靶点、开发更为有效的治疗方案和策略。
2023年11月7日,北大-清华生命科学联合中心、北京大学基础医学院尹玉新课题组以及吕丹课题组在Cell Reports杂志上联合发表了题为PTIR1 acts as an isoform of RIG-I and promotes tumor immune resistance through activation of UCHL5的文章,首次鉴定到天然免疫应答蛋白RIG-I的新亚型PTIR1分子,研究显示,多种肿瘤组织可以特异性诱导产生PTIR1,其通过影响MHC-I-肿瘤抗原肽复合体在肿瘤细胞表面的表达,从而促进肿瘤免疫逃逸以及免疫耐受。

RIG-I作为一种重要的模式识别受体,在宿主天然免疫应答中发挥重要作用。然而关于其在肿瘤发生发展过程中作用的研究相对不多。本次研究发现,在干扰素刺激条件下,编码RIG-I基因可发生RNA可变性剪接,从而产生一个可以促进肿瘤免疫逃逸的小分子亚型,根据其功能将其命名为PTIR1 (Promotor of Tumor Immune Resistance 1)。研究者进一步采用包括蛋白质谱在内的多种研究手段,发现该亚型可以翻译成一种定位于细胞质的蛋白质。临床研究发现,PTIR1可以在包括肠癌、肺癌、乳腺癌以及前列腺癌中被特异性诱导表达,并发现PTIR1的表达和肿瘤的不良预后密切相关。不仅如此,表达PTIR1的肿瘤细胞对包括免疫检查点阻断治疗在内的多种免疫疗法产生极强的耐药能力。研究采用Alpha-FOLD对PTIR1分子结构进行分析,发现其晶体结构和蛋白酶体泛素受体ADRM1极为类似,后续的研究发现PTIR1可以通过调控去泛素化酶UCHL5,进而调控肿瘤细胞中免疫蛋白酶体的活性,最终影响肿瘤抗原的加工以及呈递过程。此外,研究者还鉴定到ADAR1-p110蛋白在诱导RNA可变性剪接以及PTIR1表达的过程中发挥的关键功能。
综上所述,该研究鉴定到一种重要的免疫负调控因子PTIR1,发现其可以通过影响抗原加工与呈递过程,限制T细胞对肿瘤细胞的靶向杀伤作用。相反,抑制PTIR1的表达以及功能,可以增强T细胞对肿瘤细胞的识别,改善宿主的免疫监视能力。因此,PTIR1的发现为探索肿瘤免疫逃逸机理提供了新途径,该研究为肿瘤免疫治疗提供了潜在的新型药物靶点。
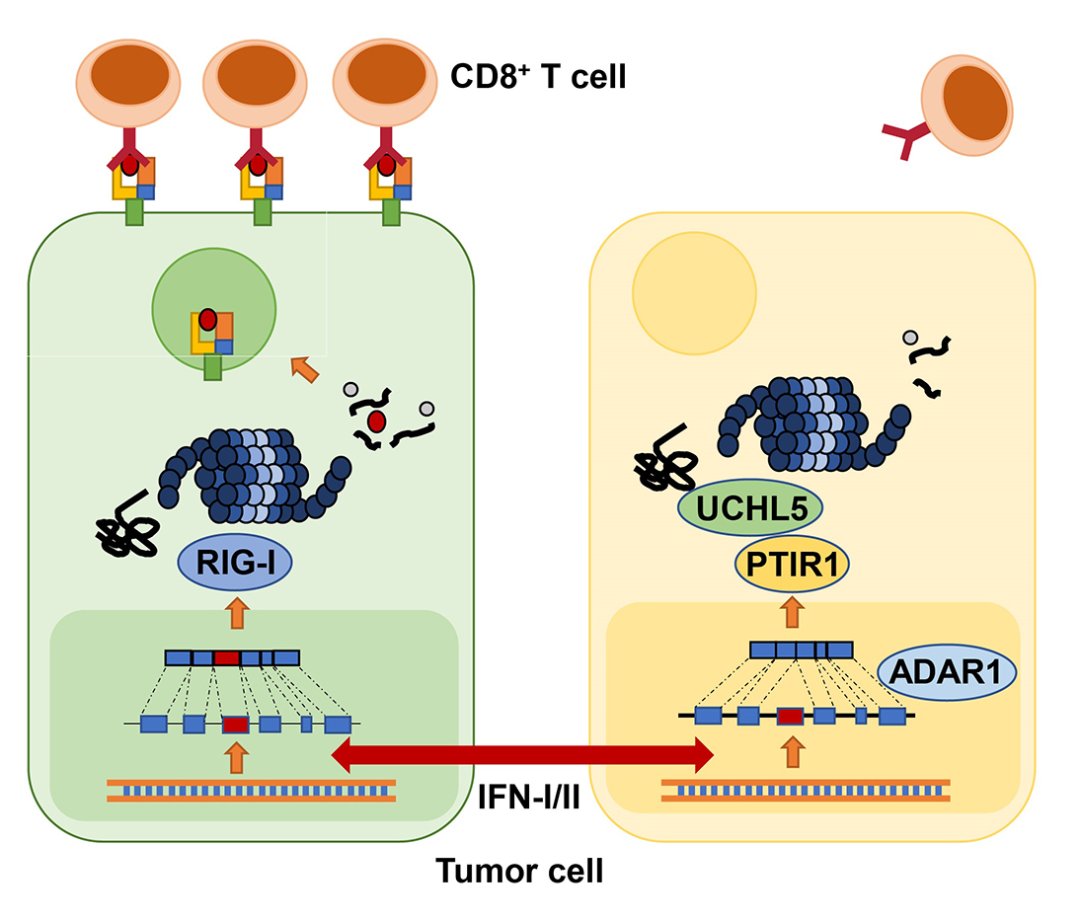
ADAR1-PTIR1-UCHL5信号通路参与促进肿瘤免疫耐药能力的形成
北京大学基础医学院博士研究生宋佳、北京大学基础医学院刘扬博士、殷悦以及王慧为该论文的共同第一作者,北京大学系统生物医学研究所尹玉新教授、吕丹研究员为共同通讯作者。
原文链接:
https://www.sciencedirect.com/science/article/pii/S2211124723014006
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









肿瘤免疫治疗作为近年来癌症研究的热点备受人们的关注
32